(1)SiH4是一种无色的气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O,已知室温下2g SiH4自燃放出热量89.2kJ,其热化学方程式为:_______
(2)已知60g C(s)与高温水蒸气反应制取CO和H2时吸收657.5kJ热量,写出热化学方程式_____________ 。
(3)某次发射火箭,用气态N2H4(肼)在NO2气体中燃烧,生成N2、液态H2O。已知:
① N2(g)+2O2(g)=2NO2(g) ΔH1=+67.2kJ/mol
② N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH2=-534kJ/mol,
假如都在相同状态下,请写出发射火箭反应的热化学方程式。_______ 。
(4)利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如下图所示的原电池,回答下列问题:
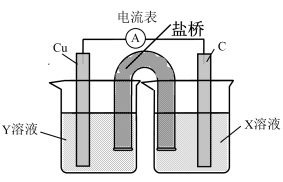
①写出正极电极反应式:___________ ;
②图中X溶液是_______ ,铜电极发生___________ 反应(填“氧化”或“还原”)。
③盐桥中的_____ (填“阳”、“阴”)离子向X溶液方向移动。
(2)已知60g C(s)与高温水蒸气反应制取CO和H2时吸收657.5kJ热量,写出热化学方程式
(3)某次发射火箭,用气态N2H4(肼)在NO2气体中燃烧,生成N2、液态H2O。已知:
① N2(g)+2O2(g)=2NO2(g) ΔH1=+67.2kJ/mol
② N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH2=-534kJ/mol,
假如都在相同状态下,请写出发射火箭反应的热化学方程式。
(4)利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如下图所示的原电池,回答下列问题:

①写出正极电极反应式:
②图中X溶液是
③盐桥中的
更新时间:2019-10-20 12:18:02
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氯及其化合物在工农业生产,生活中有着重要作用。
(1)1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图:

请写出NO2和CO反应的热化学方程式______________________________________ 。
(2)在一定体积的密闭容器中,进行如下反应:N2(g)+3H2(g) 2NH3(g)+Q(Q>0),其化学平衡常数K与温度T的关系如下表:
2NH3(g)+Q(Q>0),其化学平衡常数K与温度T的关系如下表:
比较K1、K2的大小:K1_______ K2(填“>”、“=”或“<”);判断该反应达到化学平衡状态的依据是____ (选填序号)。
a.2v(H2)正=3 v (NH3)逆 b.2 v (N2)正= v (H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)盐酸肼( N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。盐酸肼第1步水解反应的离子方程式为___________________________ ;盐酸肼水溶液中各离子浓度的关系正确的是____ (填序号)。
a.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
b.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
c.2 c(N2H62+)+ c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
d.2 c(N2H62+) +2 c([N2H5•H2O]+)+2c([N2H4·2H2O)= c(Cl-)
(1)1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图:

请写出NO2和CO反应的热化学方程式
(2)在一定体积的密闭容器中,进行如下反应:N2(g)+3H2(g)
 2NH3(g)+Q(Q>0),其化学平衡常数K与温度T的关系如下表:
2NH3(g)+Q(Q>0),其化学平衡常数K与温度T的关系如下表:| T/K | 298 | 398 | 498 | … |
| K(mol•L-1)2 | 4.1×106 | K1 | K2 | … |
比较K1、K2的大小:K1
a.2v(H2)正=3 v (NH3)逆 b.2 v (N2)正= v (H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)盐酸肼( N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。盐酸肼第1步水解反应的离子方程式为
a.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
b.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
c.2 c(N2H62+)+ c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
d.2 c(N2H62+) +2 c([N2H5•H2O]+)+2c([N2H4·2H2O)= c(Cl-)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO2和液态水时放出56kJ热量,则该条件下反应的热化学反应方程式为_______ 。
(2)将等物质的量的A、B混合于2L的密闭容器中,发生反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后测得D的浓度为0.5mol/L,c(A):c(B)=3∶5,C的平均反应速率是0.1mol·L-1·min-1。
①反应开始前充入容器中的B的物质的量为_______ 。
②B的平均反应速率为_______ 。
③A的转化率是_______
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电解质溶液中OH-离子向_______ 移动(填“电极a”或 “电极b”)。
②电极a的电极反应式_______ 。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO2和液态水时放出56kJ热量,则该条件下反应的热化学反应方程式为
(2)将等物质的量的A、B混合于2L的密闭容器中,发生反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后测得D的浓度为0.5mol/L,c(A):c(B)=3∶5,C的平均反应速率是0.1mol·L-1·min-1。
①反应开始前充入容器中的B的物质的量为
②B的平均反应速率为
③A的转化率是
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电解质溶液中OH-离子向
②电极a的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】(1)已知下列两个热化学方程式:
H2(g)+ 1/2O2(g) H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1
C2H4(g)+ 3O2(g) 2CO2(g)+2H2O(l) ΔH=-1411.0 kJ·mol-1
2CO2(g)+2H2O(l) ΔH=-1411.0 kJ·mol-1
实验测得H2和C2H4的混合气体共5 mol,完全燃烧生成液态水时放热4242kJ,则混合气体中H2和C3H8的体积比是____________ 。
(2)已知下列热化学方程式:
①CH3COOH(l) + 2O2(g) 2CO2(g) + 2H2O(l) ΔH1=-870.3 kJ·mol-1;
2CO2(g) + 2H2O(l) ΔH1=-870.3 kJ·mol-1;
②C(s) + O2(g) CO2(g) ΔH2=-393.5 kJ·mol-1;
CO2(g) ΔH2=-393.5 kJ·mol-1;
③H2(g)+1/2 O2(g) H2O(l) ΔH3=-285.8 kJ·mol-1。
H2O(l) ΔH3=-285.8 kJ·mol-1。
则反应2C(s)+2H2(g)+O2(g) CH3COOH(l)的ΔH为
CH3COOH(l)的ΔH为______________ kJ·mol-1。
(3)已知下列反应: ①SO2(g)+2OH-(aq) SO32-(aq)+H2O(l) ΔH1
SO32-(aq)+H2O(l) ΔH1
②ClO- (aq)+ SO32- (aq) SO42- (aq)+Cl-(aq) ΔH2
SO42- (aq)+Cl-(aq) ΔH2
③CaSO4(s) Ca2+(aq)+ SO42- (aq) ΔH3 则反应
Ca2+(aq)+ SO42- (aq) ΔH3 则反应
SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq) CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=_____________ 。
(4)已知:①碳的燃烧热ΔH1= a kJ·mol-1
②S(s)+2K(s) K2S(s) ΔH2=b kJ·mol-1
K2S(s) ΔH2=b kJ·mol-1
③2K(s)+N2(g)+3O2(g) 2KNO3(s) ΔH3=c kJ·mol-1
2KNO3(s) ΔH3=c kJ·mol-1
黑火药爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s) K2S(s)+N2(g)+3CO2(g) ΔH=
K2S(s)+N2(g)+3CO2(g) ΔH= ______________ kJ·mol-1
(5)①2O2(g)+N2(g) N2O4(l) ΔH1 = a
N2O4(l) ΔH1 = a
②N2(g)+2H2(g) N2H4(l) ΔH2=b ③O2(g)+2H2(g)
N2H4(l) ΔH2=b ③O2(g)+2H2(g) 2H2O(g) ΔH3=c
2H2O(g) ΔH3=c
则反应2N2H4(l)+N2O4(l) 3N2(g)+4H2O(g) ΔH4=
3N2(g)+4H2O(g) ΔH4=___________________ 。
H2(g)+ 1/2O2(g)
 H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1C2H4(g)+ 3O2(g)
 2CO2(g)+2H2O(l) ΔH=-1411.0 kJ·mol-1
2CO2(g)+2H2O(l) ΔH=-1411.0 kJ·mol-1实验测得H2和C2H4的混合气体共5 mol,完全燃烧生成液态水时放热4242kJ,则混合气体中H2和C3H8的体积比是
(2)已知下列热化学方程式:
①CH3COOH(l) + 2O2(g)
 2CO2(g) + 2H2O(l) ΔH1=-870.3 kJ·mol-1;
2CO2(g) + 2H2O(l) ΔH1=-870.3 kJ·mol-1;②C(s) + O2(g)
 CO2(g) ΔH2=-393.5 kJ·mol-1;
CO2(g) ΔH2=-393.5 kJ·mol-1;③H2(g)+1/2 O2(g)
 H2O(l) ΔH3=-285.8 kJ·mol-1。
H2O(l) ΔH3=-285.8 kJ·mol-1。则反应2C(s)+2H2(g)+O2(g)
 CH3COOH(l)的ΔH为
CH3COOH(l)的ΔH为(3)已知下列反应: ①SO2(g)+2OH-(aq)
 SO32-(aq)+H2O(l) ΔH1
SO32-(aq)+H2O(l) ΔH1②ClO- (aq)+ SO32- (aq)
 SO42- (aq)+Cl-(aq) ΔH2
SO42- (aq)+Cl-(aq) ΔH2③CaSO4(s)
 Ca2+(aq)+ SO42- (aq) ΔH3 则反应
Ca2+(aq)+ SO42- (aq) ΔH3 则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)
 CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=
CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=(4)已知:①碳的燃烧热ΔH1= a kJ·mol-1
②S(s)+2K(s)
 K2S(s) ΔH2=b kJ·mol-1
K2S(s) ΔH2=b kJ·mol-1③2K(s)+N2(g)+3O2(g)
 2KNO3(s) ΔH3=c kJ·mol-1
2KNO3(s) ΔH3=c kJ·mol-1黑火药爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)
 K2S(s)+N2(g)+3CO2(g) ΔH=
K2S(s)+N2(g)+3CO2(g) ΔH= (5)①2O2(g)+N2(g)
 N2O4(l) ΔH1 = a
N2O4(l) ΔH1 = a ②N2(g)+2H2(g)
 N2H4(l) ΔH2=b ③O2(g)+2H2(g)
N2H4(l) ΔH2=b ③O2(g)+2H2(g) 2H2O(g) ΔH3=c
2H2O(g) ΔH3=c则反应2N2H4(l)+N2O4(l)
 3N2(g)+4H2O(g) ΔH4=
3N2(g)+4H2O(g) ΔH4=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】已知反应 是可逆反应。设计如图装置(
是可逆反应。设计如图装置( 均为石墨电极),分别进行下述操作:
均为石墨电极),分别进行下述操作:

①向B烧杯中逐滴加入浓盐酸。②向B烧杯中逐滴加入 溶液。结果发现电流表指针均发生偏转。
溶液。结果发现电流表指针均发生偏转。
(1)①过程中 棒上发生的反应为
棒上发生的反应为_________ ;
②过程中 棒上发生的反应为
棒上发生的反应为___________ 。
(2)操作②过程中,盐桥中的 移向
移向_________ 烧杯溶液(填“A”或“B”)。
资料: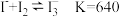 。向
。向 一定浓度的
一定浓度的 溶液中加入
溶液中加入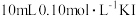 溶液,达平衡后,相关微粒浓度如下:
溶液,达平衡后,相关微粒浓度如下:
(3)a=________________ 。该平衡体系中除了含有 和
和 外,判断溶液是否一定还含有其他含碘微粒
外,判断溶液是否一定还含有其他含碘微粒______________ (填“是”或“否”)。
(4)已知:甲醇与水蒸气重整制氢可直接用于燃料电池。
反应:
反应: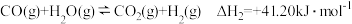
则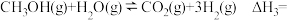
______________ 
(5)已知:25℃时,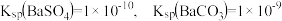 。医学上进行消化系统的X射线透视时,常使用
。医学上进行消化系统的X射线透视时,常使用 作内服造影剂。胃酸酸性很强(pH约为1),但服用大量
作内服造影剂。胃酸酸性很强(pH约为1),但服用大量 仍然是安全的,
仍然是安全的, 不溶于酸的原因是(用溶解平衡原理解释):
不溶于酸的原因是(用溶解平衡原理解释):_________ 。误服少量 ,应尽快用大量的一定浓度的
,应尽快用大量的一定浓度的 溶液给患者洗胃,忽略洗胃过程中
溶液给患者洗胃,忽略洗胃过程中 溶液浓度的变化,要使残留在胃液中的
溶液浓度的变化,要使残留在胃液中的 浓度为
浓度为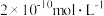 ,应服用的
,应服用的 溶液的最低浓度为
溶液的最低浓度为_______  。
。
 是可逆反应。设计如图装置(
是可逆反应。设计如图装置( 均为石墨电极),分别进行下述操作:
均为石墨电极),分别进行下述操作:
①向B烧杯中逐滴加入浓盐酸。②向B烧杯中逐滴加入
 溶液。结果发现电流表指针均发生偏转。
溶液。结果发现电流表指针均发生偏转。(1)①过程中
 棒上发生的反应为
棒上发生的反应为②过程中
 棒上发生的反应为
棒上发生的反应为(2)操作②过程中,盐桥中的
 移向
移向资料:
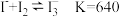 。向
。向 一定浓度的
一定浓度的 溶液中加入
溶液中加入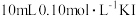 溶液,达平衡后,相关微粒浓度如下:
溶液,达平衡后,相关微粒浓度如下:| 微粒 |  |  |  |
浓度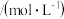 |  |  | a |
(3)a=
 和
和 外,判断溶液是否一定还含有其他含碘微粒
外,判断溶液是否一定还含有其他含碘微粒(4)已知:甲醇与水蒸气重整制氢可直接用于燃料电池。
反应:

反应:
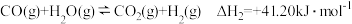
则
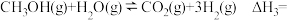

(5)已知:25℃时,
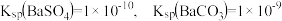 。医学上进行消化系统的X射线透视时,常使用
。医学上进行消化系统的X射线透视时,常使用 作内服造影剂。胃酸酸性很强(pH约为1),但服用大量
作内服造影剂。胃酸酸性很强(pH约为1),但服用大量 仍然是安全的,
仍然是安全的, 不溶于酸的原因是(用溶解平衡原理解释):
不溶于酸的原因是(用溶解平衡原理解释): ,应尽快用大量的一定浓度的
,应尽快用大量的一定浓度的 溶液给患者洗胃,忽略洗胃过程中
溶液给患者洗胃,忽略洗胃过程中 溶液浓度的变化,要使残留在胃液中的
溶液浓度的变化,要使残留在胃液中的 浓度为
浓度为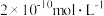 ,应服用的
,应服用的 溶液的最低浓度为
溶液的最低浓度为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】乙炔可用于照明、焊接及切割金属,也是制备乙醛、苯、合成橡胶等的基本原料。甲烷催化裂解是工业上制备乙炔的方法之一、回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(l) △H1= - 572 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H2= - 2600 kJ/mol
CH4(g)+2O2(g)=CO2(g)+ 2H2O(l) △H 3= - 885 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g) △H=___________ kJ/mol。
(2)某科研小组利用固体催化工艺进行CH4裂解制备C2H2。
①用 和
和 分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
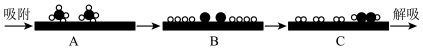
从“吸附”到“解吸”过程中,能量状态最高的是___________ 。 (填标号),理由是___________ 。
②在恒容密闭容器中充入a mol甲烷,测得单位时间内在固体催化剂表面CH4的转化率a(CH4)随温度t0℃/C的关系如图甲所示,t0℃后a(CH4)急剧下降的原因可能是___________ 。

(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/℃)的关系如图乙所示。
①在某温度下,向V L恒容密闭容器中充入0.12 mol CH4,若只发生反应:2CH4(g) C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为
C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为___________ (结果保留两位有效数字)。
②T℃时,反应2CH4(g) C2H2(g)+ 3H2(g)的压强平衡常数Kp=
C2H2(g)+ 3H2(g)的压强平衡常数Kp=___________ Pa2。
(1)已知:2H2(g)+O2(g)=2H2O(l) △H1= - 572 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H2= - 2600 kJ/mol
CH4(g)+2O2(g)=CO2(g)+ 2H2O(l) △H 3= - 885 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g) △H=
(2)某科研小组利用固体催化工艺进行CH4裂解制备C2H2。
①用
 和
和 分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
从“吸附”到“解吸”过程中,能量状态最高的是
②在恒容密闭容器中充入a mol甲烷,测得单位时间内在固体催化剂表面CH4的转化率a(CH4)随温度t0℃/C的关系如图甲所示,t0℃后a(CH4)急剧下降的原因可能是

(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/℃)的关系如图乙所示。
①在某温度下,向V L恒容密闭容器中充入0.12 mol CH4,若只发生反应:2CH4(g)
 C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为
C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为②T℃时,反应2CH4(g)
 C2H2(g)+ 3H2(g)的压强平衡常数Kp=
C2H2(g)+ 3H2(g)的压强平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】利用甲烷还原SO2可以减轻环境污染,实现硫的回收。
已知:①甲烷的燃烧热为890kJ•mol﹣1;
②S(s)+O2(g)=SO2(g)△H=﹣216kJ•mol﹣1
③H2O(1)=H2O(g)△H=+44kJ•mol﹣1
(1)CH4(g)+2SO2(g) 2S(s)+CO2(g)+2H2O(g) △H=
2S(s)+CO2(g)+2H2O(g) △H=___________ 。
(2)某温度下,向容积为2L的密闭容器中充入1.0molCH4和2.0molSO2,发生反应CH4(g)+2SO2(g) 2S(s)+CO2(g)+2H2O(g),CH4、CO2、SO2的物质的量随反应时间的变化情况如图所示。
2S(s)+CO2(g)+2H2O(g),CH4、CO2、SO2的物质的量随反应时间的变化情况如图所示。
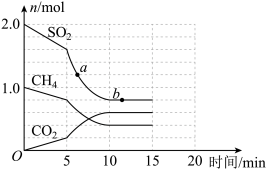
①反应开始至达到平衡时,平均反应速率v(H2O)=___________ ;该温度下,该反应的平衡常数K=___________ 。
②5min时,改变的外界条件可能是___________ (填字母)。
A.升高温度 B.降低温度 C.加入催化剂 D.充入CH4(g)
③a、b点的逆反应速率:V逆(a)___________ (填“大于”、“小于”或“等于”)V逆(b),原因是 ___________ 。
(3)一定温度下,向某密容器中充入一定量的CH4和SO2发生反应CH4(g)+2SO2(g) 2S(s)+CO2(g)+2H2O(g)。
2S(s)+CO2(g)+2H2O(g)。
①若该容器容积恒定,则下列物理量不再改变时,一定能说明反应达到平衡状态的是___________ (填字母)。
A.m(S) B. C.CH4和CO2的浓度之和 D.容器中气体的密度
C.CH4和CO2的浓度之和 D.容器中气体的密度
②该温度下,欲提高SO2的平衡转化率,可采取的措施有___________ (任答两条,下同);欲缩短反应达到平衡所需的时间,可采取的措施有 ___________ 。
已知:①甲烷的燃烧热为890kJ•mol﹣1;
②S(s)+O2(g)=SO2(g)△H=﹣216kJ•mol﹣1
③H2O(1)=H2O(g)△H=+44kJ•mol﹣1
(1)CH4(g)+2SO2(g)
 2S(s)+CO2(g)+2H2O(g) △H=
2S(s)+CO2(g)+2H2O(g) △H=(2)某温度下,向容积为2L的密闭容器中充入1.0molCH4和2.0molSO2,发生反应CH4(g)+2SO2(g)
 2S(s)+CO2(g)+2H2O(g),CH4、CO2、SO2的物质的量随反应时间的变化情况如图所示。
2S(s)+CO2(g)+2H2O(g),CH4、CO2、SO2的物质的量随反应时间的变化情况如图所示。
①反应开始至达到平衡时,平均反应速率v(H2O)=
②5min时,改变的外界条件可能是
A.升高温度 B.降低温度 C.加入催化剂 D.充入CH4(g)
③a、b点的逆反应速率:V逆(a)
(3)一定温度下,向某密容器中充入一定量的CH4和SO2发生反应CH4(g)+2SO2(g)
 2S(s)+CO2(g)+2H2O(g)。
2S(s)+CO2(g)+2H2O(g)。①若该容器容积恒定,则下列物理量不再改变时,一定能说明反应达到平衡状态的是
A.m(S) B.
 C.CH4和CO2的浓度之和 D.容器中气体的密度
C.CH4和CO2的浓度之和 D.容器中气体的密度②该温度下,欲提高SO2的平衡转化率,可采取的措施有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】利用铝与空气中的氧气发生反应,可设计为原电池,实现化学能转化为电能,实验装置如图:_______ ;发生的电极反应式是:_______ ,②消耗27g铝时,转移的电子数为:_______ mol。
(2)如图为甲烷燃料电池原理示意图。_______ ,当电路中累计有2mol电子通过时,消耗的氧气体积为(在标准状况下)_______ L。
(3)我国科学家开发Ni-N-C(Cl)催化剂实现高效催化CO2还原制备CO。装置如图所示(采用阳离子交换膜)。总反应为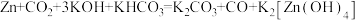 。其中正极反应式为
。其中正极反应式为_______ ,溶液中离子的移动顺序为_______ 。

(2)如图为甲烷燃料电池原理示意图。

(3)我国科学家开发Ni-N-C(Cl)催化剂实现高效催化CO2还原制备CO。装置如图所示(采用阳离子交换膜)。总反应为
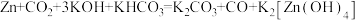 。其中正极反应式为
。其中正极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果:
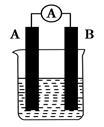
分析上述实验,回答下列问题:
(1)实验2中电流由________ 极流向________ 极(填“A”或“B”)。
(2)实验6中电子由B极流向A极,表明负极是________ (填“镁”或“铝”)电极。
(3)实验5表明________(填字母序号,下同)。
(4)分析上表有关信息,下列说法不正确的是________。

| 实验序号 | A | B | 烧杯中的液体 | 灵敏电流表指针是否偏转 |
| 1 | Zn | Zn | 乙醇 | 无 |
| 2 | Zn | Cu | 稀硫酸 | 有 |
| 3 | Zn | Cu | 稀硫酸 | 无 |
| 4 | Zn | Cu | 苯 | 无 |
| 5 | Cu | C | 氯化钠溶液 | 有 |
| 6 | Mg | Al | 氢氧化钠溶液 | 有 |
(1)实验2中电流由
(2)实验6中电子由B极流向A极,表明负极是
(3)实验5表明________(填字母序号,下同)。
| A.铜在潮湿空气中不会被腐蚀 |
| B.铜的腐蚀是自发进行的 |
| A.金属活动顺序表中,活泼性强的金属一定作负极 |
| B.失去电子的电极是负极 |
| C.烧杯中的液体必须是电解质溶液 |
| D.原电池中,浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属) |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】人类生活、工业生产往往产生大量含碳、氮、硫的废弃气体,合理再利用或转化上述气体,变废为宝成为人们共同关注的课题。
已知:2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g) N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) ∆H1<0
N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) ∆H1<0
②N2O2(g)+O2(g) 2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) ∆H2<0
2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) ∆H2<0
请回答下列问题:
(1)反应2NO(g)+O2(g) 2NO2(g)的∆H=
2NO2(g)的∆H=________________ (用含∆H1和∆H2的式子表示)。一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________ 。
(2)决定2NO(g)+O2(g) 2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1
2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________ E2(填“>”、“<”或“=”)。
(3)反应N2O4(g) 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2),其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图1所示。在图中标出的点中,能表示该反应达到平衡状态的两个点是
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2),其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图1所示。在图中标出的点中,能表示该反应达到平衡状态的两个点是________________ 。
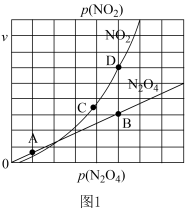
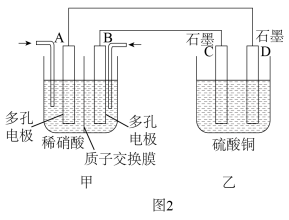
(4)若将NO2与O2通入图2所示装置的甲烧杯中,D电极上有红色物质析出,则A电极处通入的气体为________ (填化学式),A电极的电极反应式为____________________________ ;一段时间后,若乙中需加0.2 mol Cu(OH)2使溶液复原,则转移的电子数为________ 。
(5)已知25 ℃时由Na2SO3和NaHSO3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为________________________________ (已知25 ℃时,H2SO3的电离平衡常数Ka1=1×10-2,Ka2=1×10-7)。
已知:2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:①2NO(g)
 N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) ∆H1<0
N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) ∆H1<0②N2O2(g)+O2(g)
 2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) ∆H2<0
2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) ∆H2<0请回答下列问题:
(1)反应2NO(g)+O2(g)
 2NO2(g)的∆H=
2NO2(g)的∆H= 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=(2)决定2NO(g)+O2(g)
 2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1
2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1(3)反应N2O4(g)
 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2),其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图1所示。在图中标出的点中,能表示该反应达到平衡状态的两个点是
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2),其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图1所示。在图中标出的点中,能表示该反应达到平衡状态的两个点是

(4)若将NO2与O2通入图2所示装置的甲烧杯中,D电极上有红色物质析出,则A电极处通入的气体为
(5)已知25 ℃时由Na2SO3和NaHSO3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为
您最近一年使用:0次



