根据下列实验现象或要求写离子方程式(描述现象的,需要写出所有涉及的离子方程式。非特殊说明,书写离子方程式)
| 实验现象 | 离子方程式 |
| 1.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 | |
| 2.制备氢氧化铁胶体的化学方程式 | |
| 3.二氧化硫使酸性高锰酸钾溶液褪色 | |
| 4.Fe3O4溶于稀硝酸 | |
| 5.氯化亚铁溶液通入少量氯气,变为黄色溶液,加入过量碘化钾溶液,溶液颜色加深,继续加入NaOH溶液,出现白色沉淀,且颜色不断加深至红褐色。 | |
| 6.澄清石灰水中通入CO2出现白色沉淀,继续通入二氧化碳,沉淀溶解,加热后又出现白色沉淀。 | |
| 7.三氯化铝溶液中加逐滴加入NaOH溶液,先出现白色沉淀,然后溶解,再通入CO2至刚开始出现沉淀。 | |
| 8.NH4Al(SO4)2溶液与Ba(OH)2溶液物质的量1∶2混合 | |
| 9.FeI2与Cl2物质的量1∶2反应 | |
| 10.Ba(OH)2中加入硫酸铝溶液,至沉淀质量不再改变。再加入过量NaHCO3溶液,又出白色沉淀。 | |
| 11.生产硫化钠大多采用无水芒硝(Na2SO4)—碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式 | |
| 12.温度高于200 ℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4∶1),写出该反应的化学方程式 | |
| 13.湿法制备高铁酸钾(K2FeO4)的过程为,在氢氧化铁固体中加入KClO和KOH的混合液。写出该过程的离子方程式并配平。 |
19-20高三上·宁夏石嘴山·阶段练习 查看更多[3]
宁夏石嘴山市第三中学2020届高三上学期第一次适应性(开学)考试化学试题(已下线)第二节 离子反应(二)-2020-2021学年高一化学必修第一册课时同步练(新人教)9.2.1反应的合理选择(课后)-2019苏教版必修2课前课中课后
更新时间:2019/09/07 21:27:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求完成下列填空:
(1)高中化学中常见物质:①盐酸②二氧化碳③熔融氯化钠④小苏打⑤铜⑥硫酸钡。
上述物质中能导电的是_____ ,属于电解质的是____ 。
(2)写出硫酸钡的电离方程式____ 。
(3)写出下列反应的离子方程式:
①小苏打溶液中加入盐酸____ 。
②向氢氧化钡溶液中加入硫酸氢钠溶液至钡离子恰好完全沉淀____ 。
(1)高中化学中常见物质:①盐酸②二氧化碳③熔融氯化钠④小苏打⑤铜⑥硫酸钡。
上述物质中能导电的是
(2)写出硫酸钡的电离方程式
(3)写出下列反应的离子方程式:
①小苏打溶液中加入盐酸
②向氢氧化钡溶液中加入硫酸氢钠溶液至钡离子恰好完全沉淀
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列10种物质:①钠;②纯醋酸;③氨气;④浓盐酸;⑤NaOH溶液;⑥NaHSO4固体;⑦熔融的NaCl;⑧氢氧化铁胶体;⑨高锰酸钾粉末。回答下列问题:
(1)上述物质中能导电的___________ (填序号,下同);属于电解质的有___________ 。
(2)⑥属于___________ (填“酸”、“碱”或“盐"),⑤与⑥在溶液中反应的离子方程式为___________ 。
(3)④和⑨混合发生反应KMnO4+HCl(浓)→MnCl2+Cl2↑+KCl+H2O(未配平),配平反应方程式___________ ,其中氧化剂与还原剂的个数比为___________ 。
(4)写出制备⑧的化学方程式___________ 。
(1)上述物质中能导电的
(2)⑥属于
(3)④和⑨混合发生反应KMnO4+HCl(浓)→MnCl2+Cl2↑+KCl+H2O(未配平),配平反应方程式
(4)写出制备⑧的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据酸碱的质子理论,“凡是能给出质子( )的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:①
)的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥HClO,⑦
,⑥HClO,⑦ ,⑧
,⑧ 。
。
(1)只属于酸的微粒是:_______ ;属于两性的微粒是:_______ 。(填标号)。
(2)写出⑤和⑥反应的离子方程式_______ 。
(3)经检测某工业废水显酸性,且废水中含有大量 、
、 和上述③、⑦、⑧离子。
和上述③、⑦、⑧离子。
a.下列离子中不可能大量存在该废水的是_______ (填标号)。
A. B.
B. C.
C. D.
D.
b.将该废水调节至碱性;废水中存在的离子产生的现象是_______ 。
(4)用流程图表示除去粗盐水中 、
、 、
、 离子的方案设计。
离子的方案设计。
(可选用试剂有:稀盐酸、稀硫酸、 溶液、
溶液、 溶液、NaOH溶液。)
溶液、NaOH溶液。)
_______ 。
 )的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:①
)的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥HClO,⑦
,⑥HClO,⑦ ,⑧
,⑧ 。
。(1)只属于酸的微粒是:
(2)写出⑤和⑥反应的离子方程式
(3)经检测某工业废水显酸性,且废水中含有大量
 、
、 和上述③、⑦、⑧离子。
和上述③、⑦、⑧离子。a.下列离子中不可能大量存在该废水的是
A.
 B.
B. C.
C. D.
D.
b.将该废水调节至碱性;废水中存在的离子产生的现象是
(4)用流程图表示除去粗盐水中
 、
、 、
、 离子的方案设计。
离子的方案设计。(可选用试剂有:稀盐酸、稀硫酸、
 溶液、
溶液、 溶液、NaOH溶液。)
溶液、NaOH溶液。)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.邢是邢台古老的地名,在甲骨文中就有记载,当时被称作“井”。在悠久的历史传承中,邢台地区产生了众多精美的文物,请回答下列问题:
i.商“耳为父癸”铭兽首鎏兽面纹铜爵 ;汉错金四神几何纹长颈铜壶
;汉错金四神几何纹长颈铜壶
ii.一种火法炼铜的方法:采富含孔雀石【主要成分为Cu2(OH)2CO3】的矿石,与木炭共热,反应方程式为 。
。
(1)Cu2(OH)2CO3属于___________ (填“酸”、“碱”或“盐”),该反应中化合价升高的元素为___________ (填名称)。
II.含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。某含氮废水中 浓度为1.86×10-2g/L,现采用铝还原法来将
浓度为1.86×10-2g/L,现采用铝还原法来将 还原为N2。
还原为N2。
(2) 中氮元素的化合价为
中氮元素的化合价为___________ 。
(3)配平下列有关反应的化学方程式___________ 。
(4)上述反应中,还原剂是___________ ,被还原的元素是___________ 。
(5)有上述废水100m3,若要完全处理所含的 ,则需消耗金属铝的质量为
,则需消耗金属铝的质量为___________ g。
i.商“耳为父癸”铭兽首鎏兽面纹铜爵
 ;汉错金四神几何纹长颈铜壶
;汉错金四神几何纹长颈铜壶
ii.一种火法炼铜的方法:采富含孔雀石【主要成分为Cu2(OH)2CO3】的矿石,与木炭共热,反应方程式为
 。
。(1)Cu2(OH)2CO3属于
II.含氮废水不仅会引起水体富营养化而导致黑臭,而且对人群及其他生物产生毒害作用。某含氮废水中
 浓度为1.86×10-2g/L,现采用铝还原法来将
浓度为1.86×10-2g/L,现采用铝还原法来将 还原为N2。
还原为N2。(2)
 中氮元素的化合价为
中氮元素的化合价为(3)配平下列有关反应的化学方程式

(4)上述反应中,还原剂是
(5)有上述废水100m3,若要完全处理所含的
 ,则需消耗金属铝的质量为
,则需消耗金属铝的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:___________ 。
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为___________ 。
(3)已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。若有64gCu被氧化,则被还原的HNO3的物质的量是___________ 。
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为___________ 。
(5)含有10个电子,9个质子的微粒___________ 。(至少2个)
(6)用电子式表示MgCl2的形成过程___________ 。
(7)配平___________
Mn2++PbO2+H+→MnO +Pb2++H2O
+Pb2++H2O
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为
(3)已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。若有64gCu被氧化,则被还原的HNO3的物质的量是
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
(5)含有10个电子,9个质子的微粒
(6)用电子式表示MgCl2的形成过程
(7)配平
Mn2++PbO2+H+→MnO
 +Pb2++H2O
+Pb2++H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,完成下面题目。
(1)铅在蓄电池时发生的电池反应式为放电 ,正极反应式为
,正极反应式为_______ 。
(2) 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_
,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移________ 摩尔电子。
(3)将铝片和铜片用连接,插入硝酸中,原电池,正极为_______ (填入“铜”或“ 铝”,下同)将其插件烧成原电池,将其作为答案_______ 。
(4)锂电池的体积小、性能好,是常用的一次电池。该电池反应原理如图所示,其中电解质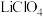 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成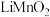 。
。

①外电路的电子方向是由_______ (填字母,下同)极流向_______ 极。
②电池正极反应式为_______ 。
③ 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(1)铅在蓄电池时发生的电池反应式为放电
 ,正极反应式为
,正极反应式为(2)
 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_
,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_(3)将铝片和铜片用连接,插入硝酸中,原电池,正极为
(4)锂电池的体积小、性能好,是常用的一次电池。该电池反应原理如图所示,其中电解质
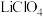 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成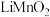 。
。
①外电路的电子方向是由
②电池正极反应式为
③
 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将一定质量的镁铝合金全部溶于100 mL某浓度的盐酸中。向所得溶液中滴加
5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如右
图所示。则盐酸的物质的量浓度为____ 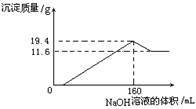
5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如右
图所示。则盐酸的物质的量浓度为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠、铝、铁是三种重要的金属。请回答:
(1)三种金属与同浓度盐酸反应,反应最慢的是___ (填选项)。
a.钠 b.铝 c.铁
(2)金属钠与水发生反应的离子方程式为___ ;(填选项)
a.2Na +2H2O=2NaOH+H2↑
b.2Na+2H2O=2Na++2OH-+H2↑
c.2Na +2H2O=2Na++2OH-+O2↑
(3)可观察到的实验现象正确的是__ (填选项)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(4)填写a、b、c化学式并书写①的化学方程式(a、b、c均为含Al化合物);
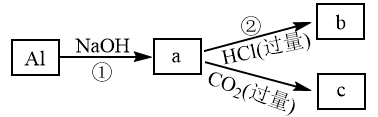
a:___ ,b:___ ,c:___ ;
①____________ ;
(5)Fe跟Cl2在一定条件下反应,所得产物为___ 。
(6)将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成__ 色。
b.向另一支试管中滴加NaOH溶液,产生__ 色沉淀。
(1)三种金属与同浓度盐酸反应,反应最慢的是
a.钠 b.铝 c.铁
(2)金属钠与水发生反应的离子方程式为
a.2Na +2H2O=2NaOH+H2↑
b.2Na+2H2O=2Na++2OH-+H2↑
c.2Na +2H2O=2Na++2OH-+O2↑
(3)可观察到的实验现象正确的是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(4)填写a、b、c化学式并书写①的化学方程式(a、b、c均为含Al化合物);

a:
①
(5)Fe跟Cl2在一定条件下反应,所得产物为
(6)将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,产生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如下图。回答下列问题:

(1)写出OA段和BC段反应的离子方程式:
OA:___________ ; BC:_____________ ;
(2)原Mg-Al合金的质量是_____________ 。
(3)原HCl溶液的物质的量浓度是________________ 。
(4)所加NaOH溶液的物质的量浓度是____________ 。

(1)写出OA段和BC段反应的离子方程式:
OA:
(2)原Mg-Al合金的质量是
(3)原HCl溶液的物质的量浓度是
(4)所加NaOH溶液的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】制备FeCl3的反应路径:以铁为原料制备FeCl3可以有多种路径,请写出各条路径中有关的化学方程式:
(1)Fe→FeCl3:_______ 。
(2)Fe→FeCl2→FeCl3:_______ 、_______ 。
(3)Fe→Fe2O3→FeCl3::_______ 、_______ 。
(1)Fe→FeCl3:
(2)Fe→FeCl2→FeCl3:
(3)Fe→Fe2O3→FeCl3::
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某兴趣小组把学生做完实验后的废液(含氯化钠、氯化铁、氯化铜等)进行集中处理,过程如下:
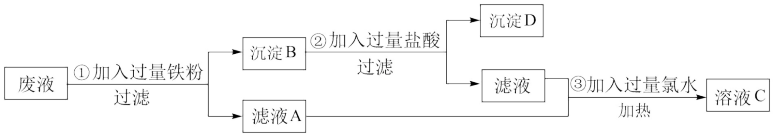
(1)沉淀D的化学式为______
(2)反应③中氯水属于______ (填“氧化剂”或“还原剂”)。
(3)写出①反应中的离子方程式______
(4)溶液C中的溶质是______

(1)沉淀D的化学式为
(2)反应③中氯水属于
(3)写出①反应中的离子方程式
(4)溶液C中的溶质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将铁粉、铜粉、FeCl3溶液和CuCl2 溶液混合于某容器中充分反应(假定容器不参与反应)。试判断下列情况下,容器中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有的离子是________ ,铜单质______ ( 填“一定”或“可能”)存在。
(2)若CuCl2有剩余,则容器中还可能有的离子为________ ,铜单质______ ( 填“一定”或“可能”)存在。
(3)若FeCl3和CuCl2 都有剩余,则容器中不可能有的单质是______ ,Fe2+_____ (填“一定”或“可能”)存在。
(4)将6 g铁粉加入200 mL Fe2(SO4)3 和CuSO4的混合溶液中,充分反应得到200 mL 0.5 mol/L FeSO4溶液和5.2 g固体沉淀物,则原Fe2(SO4)3 和CuSO4的混合溶液中Fe2(SO4)3的物质的量浓度为________ 。
(1)若铁粉有剩余,则容器中不可能有的离子是
(2)若CuCl2有剩余,则容器中还可能有的离子为
(3)若FeCl3和CuCl2 都有剩余,则容器中不可能有的单质是
(4)将6 g铁粉加入200 mL Fe2(SO4)3 和CuSO4的混合溶液中,充分反应得到200 mL 0.5 mol/L FeSO4溶液和5.2 g固体沉淀物,则原Fe2(SO4)3 和CuSO4的混合溶液中Fe2(SO4)3的物质的量浓度为
您最近一年使用:0次



