钠、铝、铁是三种重要的金属。请回答:
(1)三种金属与同浓度盐酸反应,反应最慢的是___ (填选项)。
a.钠 b.铝 c.铁
(2)金属钠与水发生反应的离子方程式为___ ;(填选项)
a.2Na +2H2O=2NaOH+H2↑
b.2Na+2H2O=2Na++2OH-+H2↑
c.2Na +2H2O=2Na++2OH-+O2↑
(3)可观察到的实验现象正确的是__ (填选项)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(4)填写a、b、c化学式并书写①的化学方程式(a、b、c均为含Al化合物);
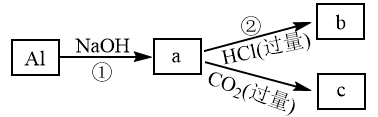
a:___ ,b:___ ,c:___ ;
①____________ ;
(5)Fe跟Cl2在一定条件下反应,所得产物为___ 。
(6)将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成__ 色。
b.向另一支试管中滴加NaOH溶液,产生__ 色沉淀。
(1)三种金属与同浓度盐酸反应,反应最慢的是
a.钠 b.铝 c.铁
(2)金属钠与水发生反应的离子方程式为
a.2Na +2H2O=2NaOH+H2↑
b.2Na+2H2O=2Na++2OH-+H2↑
c.2Na +2H2O=2Na++2OH-+O2↑
(3)可观察到的实验现象正确的是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(4)填写a、b、c化学式并书写①的化学方程式(a、b、c均为含Al化合物);

a:
①
(5)Fe跟Cl2在一定条件下反应,所得产物为
(6)将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,产生
更新时间:2019-12-29 13:46:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列反应的离子方程式:
(1)钠与水反应___________ 。
(2)氯气与水反应___________ 。
(3)二氧化氮溶于水___________ 。
(4)铜与稀硝酸反应___________ 。
(1)钠与水反应
(2)氯气与水反应
(3)二氧化氮溶于水
(4)铜与稀硝酸反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钠和铝是两种重要的金属。请回答:
(1)将一小块金属钠投入水中,可观察到的实验现象是_____________ (填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(2)铝与氢氧化钠溶液反应的离子方程式为__________________________________ 。
(1)将一小块金属钠投入水中,可观察到的实验现象是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(2)铝与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
(1)金属与水的反应
①Na的原子结构示意图是___________ 。
②钠与水反应的化学方程式是___________ 。
③钠与水的反应放出热量的现象是___________ 。
④钠、镁与水均能反应,通过比较反应的难易程度,可知钠的金属性强于镁。
(2)钠、钾失火时,可用不同的灭火剂灭火。如金属钠失火,可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因___________ 。
(3)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3的说法中,正确的是___________ (填字母)。
a.Na2CO3和NaHCO3的溶液均显碱性
b.相同温度下,NaHCO3的溶解度大于Na2CO3
c.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
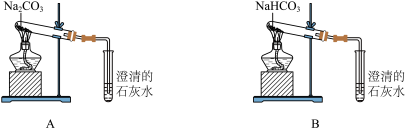
(4)按下图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是________ 。
(1)金属与水的反应

①Na的原子结构示意图是
②钠与水反应的化学方程式是
③钠与水的反应放出热量的现象是
④钠、镁与水均能反应,通过比较反应的难易程度,可知钠的金属性强于镁。
(2)钠、钾失火时,可用不同的灭火剂灭火。如金属钠失火,可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因
(3)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3的说法中,正确的是
a.Na2CO3和NaHCO3的溶液均显碱性
b.相同温度下,NaHCO3的溶解度大于Na2CO3
c.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
(4)按下图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________ (用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式:_____________ 。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是______________ 。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式:________________ 。
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为
(2)写出锌和氢氧化钠溶液反应的化学方程式:
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请按要求完成下列各题。
(1)将2mol•L-1Al2(SO4)3和0.2mol•L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=___ mol•L-1.若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2mol•L-1稀硫酸,计算需要量取___ mL的浓硫酸。(读到小数点后一位)
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是___ ,混合气体的平均摩尔质量是___ 。
(3)还原铁粉与高温水蒸气反应的化学方程式:___ 。
(4)除去Mg粉中的Al粉的试剂是___ ,反应的离子方程式为:___ 。
(1)将2mol•L-1Al2(SO4)3和0.2mol•L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是
(3)还原铁粉与高温水蒸气反应的化学方程式:
(4)除去Mg粉中的Al粉的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐( 主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:

(1)请写出镓(与铝同主族的第四周期元素)的原子结构示意图_________ 。
(2)为尽量少引入杂质,试剂①应选用______ (填标号)。理由是______________ 。
A.HCl溶液 B.H2SO4 溶液 C.氨水 D.NaOH溶液
(3)沉淀B的化学式为________ ;将少量明矾溶于水,溶液呈弱酸性,其原因是________ (用离子方程式表示)。
(4)科学研究证明NaAlO2 在水溶液中实际上是Na[Al(OH)4](四羟基合铝酸钠),易拉罐溶解过程中主要反应的化学方程式为___________________ 。
(5)常温下,等pH的NaAlO2 和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=__________ 。
(6)已知室温下,Kw=10×10-14,Al(OH)3 AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________ 。

(1)请写出镓(与铝同主族的第四周期元素)的原子结构示意图
(2)为尽量少引入杂质,试剂①应选用
A.HCl溶液 B.H2SO4 溶液 C.氨水 D.NaOH溶液
(3)沉淀B的化学式为
(4)科学研究证明NaAlO2 在水溶液中实际上是Na[Al(OH)4](四羟基合铝酸钠),易拉罐溶解过程中主要反应的化学方程式为
(5)常温下,等pH的NaAlO2 和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=
(6)已知室温下,Kw=10×10-14,Al(OH)3
 AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
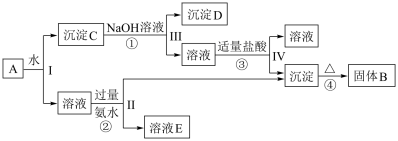
【推荐1】为探究含结晶水的化合物X(含四种元素,摩尔质量为 )的组成和性质,某兴趣小组设计并完成如下实验:
)的组成和性质,某兴趣小组设计并完成如下实验:

回答下列问题:
(1)化合物X的化学式为___________ ,气体E的电子式为____________ 。
(2)固体X隔绝空气受热分解的化学方程式为____________ 。
(3)写出溶液A和溶液B反应生成白色沉淀Z的离子方程式_________________ 。
 )的组成和性质,某兴趣小组设计并完成如下实验:
)的组成和性质,某兴趣小组设计并完成如下实验:
回答下列问题:
(1)化合物X的化学式为
(2)固体X隔绝空气受热分解的化学方程式为
(3)写出溶液A和溶液B反应生成白色沉淀Z的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钠、铝、铁是三种重要的金属。请回答:
(1)钠元素的金属活动性比铝的________ (填“强”或“弱”)。
(2)将一小块金属钠投入水中,发生反应的离子方程式为____________ ;可观察到的实验现象是________ (填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)呼吸面具的原理:________________ ,_______________________ 。
(4)填写a、b、c化学式并书写①、②的离子方程式(a、b、c均为含Al化合物);
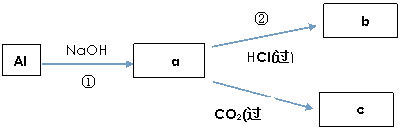
a:____________ ,b:_____________ ,c:____________ ;
①____________________________________________ ;
②____________________________________________ ;
(1)钠元素的金属活动性比铝的
(2)将一小块金属钠投入水中,发生反应的离子方程式为
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)呼吸面具的原理:
(4)填写a、b、c化学式并书写①、②的离子方程式(a、b、c均为含Al化合物);

a:
①
②
您最近一年使用:0次