酸雨是过度燃烧煤和石油,生成硫、氮的氧化物,溶于水生成硫酸和硝酸的缘故,某次雨水分析数据如下:c(SO42-)=2.6×10-5mol/L,c(Cl-)=8.0×10-6mol/L,c(NH4+)=3.0×10-6mol/L,c(Na+)=1.0×10-6mol/L,c(NO3-)=2.4×10-5mol/L,则此次酸雨的pH接近于(lg8=0.9)( )
| A.6.5 | B.5 | C.4 | D.4.5 |
更新时间:2019-09-27 17:12:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法错误的是
A.一定温度下,水、稀酸、稀碱溶液中 相等 相等 |
B.常温下,将 的醋酸溶液稀释至 的醋酸溶液稀释至 ,稀释后溶液体积大于原溶液体积的10倍 ,稀释后溶液体积大于原溶液体积的10倍 |
C.常温下,pH相等的下列溶液:a. 、b. 、b. 、c. 、c. ,其物质的量浓度由小到大排列顺序为: ,其物质的量浓度由小到大排列顺序为: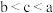 |
D.用酸式滴定管量取 的盐酸溶液,开始时平视读数,结束时仰视读数,会使所量液体体积偏大 的盐酸溶液,开始时平视读数,结束时仰视读数,会使所量液体体积偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是( )
| A.95℃纯水的pH<7,说明加热可导致水呈酸性 |
| B.pH=3的醋酸溶液,稀释至10倍后pH=4 |
| C.将AlCl3溶液蒸干并灼烧 得到的固体为Al2O3 |
| D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验原理或实验操作正确的是( )
| A.用蒸馏水湿润的pH试纸测量某溶液的pH=10 |
| B.用10 mL量筒量取0.50 mol·L-1 H2SO4溶液5.50mL |
| C.向铁钉上镀铜时,铁钉连接直流电源的正极 |
| D.盛装Na2CO3溶液的试剂瓶要使用胶塞 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验能达到相应实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 在5mL 0.005mol/L FeCl3和5mL 0.1mol/L KSCN的混合溶液中,加入饱和FeCl3溶液,溶液的红色加深 | 验证浓度对化学平衡的影响 |
| B | 室温下,用pH试纸测定浓度为0.1mol·L-1 NaClO溶液和0.1mol·L-1 CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| C | 常温下,测得浓度均为0.1mol/L溶液的pH:NaA>NaB | 证明常温下的Ka:HA<HB |
| D | 等体积、pH均为2的HA和HB两种酸分别与足量Zn反应,HA放出的H2多 | 证明HA是强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.常温下pH=2的HA溶液与pH=12的BOH等体积混合,溶液pH>7,则BOH为强碱 |
| B.pH=1的盐酸和pH=12的MOH溶液等体积混合后,恰好完全反应,所用盐酸的浓度等于MOH溶液的浓度 |
| C.升高温度,0.1 mol/L的氢氧化钠溶液pH减小,碱性减弱 |
D.相同温度下,pH相等的氨水和NaOH溶液,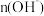 相等 相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列溶液中离子浓度的大小顺序正确的是( )
| A.1mL1mol/L的氨水与10mL0.1mol/L的盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.10mL 0.1mol/LCH3COOH溶液与5mL0.2mol/LNaOH溶液混合:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| C.10mL 0.1mol/LNH4Cl溶液与5mL0.2mol/LNaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| D.10mL 0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】设NA为阿伏加 德罗常数的值。下列说法中正确的是( )
| A.标况下22.4L HF中电子总数为10NA |
| B.已知CH2═CH2(g)+H2(g) ==== CH3CH3(g)∆H= -137.0 kJ/mol,乙烯与H2加成时放出68.5 kJ热量时,反应过程中被破坏的碳原子之间共用电子对数目为NA |
| C.25℃,1LpH=1的盐酸和1LpH=1的醋酸溶液混合,混合后所得溶液中H+数目为0.2NA(混合后溶液体积变化忽略不计) |
| D.1molICl、1molCl2分别与足量水反应,转移电子数目均为1NA |
您最近一年使用:0次

 )
)

