(1)在铝表面除去氧化膜,物理方法可用_________ ,化学方法可将其浸入氢氧化钠溶液,发生反应的化学方程式为:_________ ;
(2)将除去氧化膜的铝迅速用蒸馏水清洗干净,立即插入硝酸汞溶液片刻,发生反应的离子方程式为:__________________ ;取出铝片用滤纸吸去表面溶液,铝片上出现的“黑斑”是_________ ;
(3)将此铝放置于空气中,“黑斑”边会长出“白毛”,此物质是_________ .
(4)此实验证明了( )
A.氧化铝都是十分坚硬的晶体 B.铝是较活泼的金属,可以被空气中氧气氧化
C.铝表面的氧化膜有保护作用 D.铝是很不活泼的金属,不可以被氧气氧化
(2)将除去氧化膜的铝迅速用蒸馏水清洗干净,立即插入硝酸汞溶液片刻,发生反应的离子方程式为:
(3)将此铝放置于空气中,“黑斑”边会长出“白毛”,此物质是
(4)此实验证明了
A.氧化铝都是十分坚硬的晶体 B.铝是较活泼的金属,可以被空气中氧气氧化
C.铝表面的氧化膜有保护作用 D.铝是很不活泼的金属,不可以被氧气氧化
更新时间:2019-11-03 09:42:19
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】根据所学知识,回答下列问题:
(1)CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。CH3OH的摩尔质量是___ g∙mol−1;标准状况下,5.6LCO2的物质的量是___ mol,质量是___ g。
(2)等物质的量的Na、Mg、Al、Fe分别与足量的稀盐酸反应,同温同压下,产生气体的体积之比为___ 。
(3)可用氢氧化钠溶液除去铁粉中含有的少量铝粉杂质,写出该除杂反应的化学方程式:___ 。
(4)NaNO2有咸味,有毒。NaNO2加热到320°C以上会分解,生成一氧化氮、二氧化氮和氧化钠,写出此反应的化学方程式并用双线桥法标明电子转移的方向和数目:___ ,反应中被氧化的元素和被还原的元素的物质的量之比为___ 。工业上可用NH4Cl处理含NaNO2的废液,该转化反应可生成无污染的N2,反应中氧化剂和还原剂的物质的量之比为___ 。
(1)CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。CH3OH的摩尔质量是
(2)等物质的量的Na、Mg、Al、Fe分别与足量的稀盐酸反应,同温同压下,产生气体的体积之比为
(3)可用氢氧化钠溶液除去铁粉中含有的少量铝粉杂质,写出该除杂反应的化学方程式:
(4)NaNO2有咸味,有毒。NaNO2加热到320°C以上会分解,生成一氧化氮、二氧化氮和氧化钠,写出此反应的化学方程式并用双线桥法标明电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】以下是对金属及其化合物的讨论,请根据要求回答问题:
(1)写出钠与水发生反应的离子方程式:_________________ 。
(2)在空气中往FeCl2 溶液中滴入NaOH溶液,观察到的现象是__________ 。
(3)铝与足量的硫酸溶液反应,生成标准状况下的气体3.36L,则反应中消耗的铝的质量为______ 。
(1)写出钠与水发生反应的离子方程式:
(2)在空气中往FeCl2 溶液中滴入NaOH溶液,观察到的现象是
(3)铝与足量的硫酸溶液反应,生成标准状况下的气体3.36L,则反应中消耗的铝的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)金属钠着火时,不能用水灭火,原因是_______ (用离子方程式表示)。
(2)常温下铁遇水不反应,但在高温条件下二者能发生反应,书写二者反应的化学方程式___ 。
(3)热水瓶用久后,瓶胆内常附着一层水垢(主要成分是CaCO3),用食醋能较好的清除,其原理是_______ (用离子方程式表示)。
(4)铝合金材料在生活生产中应用广泛,如铝合金门窗、飞机外壳、航空航天等,且具有密度小、易加工、不易腐蚀等优点,Al与氢氧化钠溶液反应的离子方程式为___ 。
(5)设计实验检验实验室用KClO3和MnO2制取氧气后的产物中是否存在Cl-____ 。
(1)金属钠着火时,不能用水灭火,原因是
(2)常温下铁遇水不反应,但在高温条件下二者能发生反应,书写二者反应的化学方程式
(3)热水瓶用久后,瓶胆内常附着一层水垢(主要成分是CaCO3),用食醋能较好的清除,其原理是
(4)铝合金材料在生活生产中应用广泛,如铝合金门窗、飞机外壳、航空航天等,且具有密度小、易加工、不易腐蚀等优点,Al与氢氧化钠溶液反应的离子方程式为
(5)设计实验检验实验室用KClO3和MnO2制取氧气后的产物中是否存在Cl-
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业制备无水AlCl3的流程如下:

氯化炉中通入O2的目的是___________

氯化炉中通入O2的目的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氧化铝是一种典型的两性氧化物,既能与酸反应,又能与碱溶液反应。
(1)氧化铝与硫酸反应的化学方程式是____________ ,离子方程式是________________ 。
(2)氧化铝与烧碱溶液反应的化学方程式是_______________ ,离子方程式是________________ 。
(3)若使等质量的氧化铝溶解,消耗硫酸与氢氧化钠的物质的量之比是__________ 。
(1)氧化铝与硫酸反应的化学方程式是
(2)氧化铝与烧碱溶液反应的化学方程式是
(3)若使等质量的氧化铝溶解,消耗硫酸与氢氧化钠的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学是一门实用性很强的科学,请根据题意用化学式填空:
(1)钠有多种化合物,其中俗称“纯碱”的是___________
(2)铁有多种氧化物,其中为黑色且具有磁性的是___________
(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了___________ 保护内层金属
(4)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用。已知“84”消毒液的制备原理为___________ (填写化学方程式);其在使用前须在空气中放置一段时间的原因是___________ (用离子方程式表示)
(1)钠有多种化合物,其中俗称“纯碱”的是
(2)铁有多种氧化物,其中为黑色且具有磁性的是
(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了
(4)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用。已知“84”消毒液的制备原理为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】简要回答下列问题。洗涤铝制炊具为什么不宜使用酸性或碱性的洗涤剂_______________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学是一门实用性很强的自然科学。请根据题意填空:
(1)铝制易拉罐的表面有一层氧化膜,主要成分是Al2O3。它与盐酸和氢氧化钠溶液反应都生成盐和水,则Al2O3属于______ 氧化物。(填“酸性”、“碱性” 或“两性”)
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是______ 。(填“食盐”或“纯碱”)。
(3)碳酸钠和碳酸氢钠用途很多,其中可以焙制蛋糕的是______ 。(填“碳酸钠”或“碳酸氢钠”)
(4)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是______ (填“Na2O”或“Na2O2”)
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是______ 。(填“FeO”、“ Fe2O3”或“Fe3O4”)
(1)铝制易拉罐的表面有一层氧化膜,主要成分是Al2O3。它与盐酸和氢氧化钠溶液反应都生成盐和水,则Al2O3属于
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是
(3)碳酸钠和碳酸氢钠用途很多,其中可以焙制蛋糕的是
(4)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】金属及其化合物应用广泛,回答下列问题。
(1)运载火箭和载人飞船上使用的铝材属于_______ (填“纯铝”或“铝合金”),生产可用NaOH溶液除去铝材表面的天然氧化膜,反应的离子方程式是_______ 。
(2)服用维生素C可将人体中的Fe3+转化成Fe2+,这说明维生素C具有_______ (填“还原”或“氧化")性。
(3)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示这一处理过程的原理:_______ 、_______ ;处理过程中需定期添加的原料是_______ (填名称)。
(4)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应,写出反应的离子方程式_______ 。
(5)铁与水蒸气的反应的化学方程式是_______ 。当有16.8g铁粉参加反应时,生成的气体在标准状况下的体积是_______ 。
(6)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是_______ ,反应化学方程式为_______ 。
(1)运载火箭和载人飞船上使用的铝材属于
(2)服用维生素C可将人体中的Fe3+转化成Fe2+,这说明维生素C具有
(3)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示这一处理过程的原理:
(4)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应,写出反应的离子方程式
(5)铁与水蒸气的反应的化学方程式是
(6)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求完成下列问题。
(1)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式: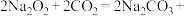
________ ;
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是___________ (填“食盐”或“纯碱”)。
(3)向盛有FeCl3溶液的试管中,滴加几滴KSCN溶液,溶液显___________ 色;
(4)Al2O3能溶于酸或强碱溶液生成盐和水,它是一种___________ (填“酸性”“碱性”或“两性”)氧化物;
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是___________ (填字母代号)。
A.FeO B.Fe2O3 C.Fe3O4
(1)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式:
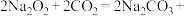
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是
(3)向盛有FeCl3溶液的试管中,滴加几滴KSCN溶液,溶液显
(4)Al2O3能溶于酸或强碱溶液生成盐和水,它是一种
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
A.FeO B.Fe2O3 C.Fe3O4
您最近一年使用:0次



