某盐酸的密度为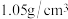 ,HCl的质量分数为
,HCl的质量分数为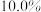 ,试计算:
,试计算:
(1)该盐酸的物质的量浓度是多少?(小数点后保留两位)_________
(2)在足量的该盐酸溶液中,加入镁粉和铝粉混合物 ,充分反应共生成
,充分反应共生成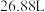 气体(标准状况),求混合物中镁和铝的质量各为多少?
气体(标准状况),求混合物中镁和铝的质量各为多少?____________ ,_______________
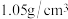 ,HCl的质量分数为
,HCl的质量分数为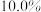 ,试计算:
,试计算:(1)该盐酸的物质的量浓度是多少?(小数点后保留两位)
(2)在足量的该盐酸溶液中,加入镁粉和铝粉混合物
 ,充分反应共生成
,充分反应共生成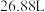 气体(标准状况),求混合物中镁和铝的质量各为多少?
气体(标准状况),求混合物中镁和铝的质量各为多少?
更新时间:2019-11-04 19:44:43
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】标况下 VL 氨气溶于 1L 水中制得密度为d g/cm3 的氨水,为计算氨水的物质的量浓度,完成下列空格(要有计算过程)。
①氨水的体积_______ L。
②氨水的物质的量浓度______ mol/L。
①氨水的体积
②氨水的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将10.6gNa2CO3粉末投入500mL一定浓度的硫酸溶液中,恰好完全反应。求:
(1)标准状况下收集到CO2气体体积为___________ 。
(2)硫酸溶液的物质的量浓度为___________ 。
(1)标准状况下收集到CO2气体体积为
(2)硫酸溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】硫化氢与浓硫酸发生如下反应:H2S+H2SO4(浓)→S↓+SO2↑+2H2O加热条件下,单质硫与浓硫酸又会发生如下反应:S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
计算:
(1)若98%浓硫酸可表示为H2SO4•aH2O,则a=__ ;若要把该浓硫酸转化为H2SO4•H2O,则98%浓硫酸与加入水的质量比为_____ 。
(2)一定条件下,将0.1mol H2S气体通入足量浓硫酸中,生成b mol SO2,则 b的取值范围是_______ 。
(3)在50mL、4.0mol/L的NaOH溶液中,通入H2S气体并充分反应,然后,小心蒸发,得到不含结晶水的白色固体.通入H2S的物质的量为x mol,生成的白色固体的质量为7.9g,通过计算确定白色固体的可能成分及每种成分的质量(结果保留一位小数)_______ 。
 3SO2↑+2H2O
3SO2↑+2H2O计算:
(1)若98%浓硫酸可表示为H2SO4•aH2O,则a=
(2)一定条件下,将0.1mol H2S气体通入足量浓硫酸中,生成b mol SO2,则 b的取值范围是
(3)在50mL、4.0mol/L的NaOH溶液中,通入H2S气体并充分反应,然后,小心蒸发,得到不含结晶水的白色固体.通入H2S的物质的量为x mol,生成的白色固体的质量为7.9g,通过计算确定白色固体的可能成分及每种成分的质量(结果保留一位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】有硫酸,硫酸亚铁、硫酸铁的混合溶液 ,已知溶液中各阳离子的物质的量浓度相等,
,已知溶液中各阳离子的物质的量浓度相等, 的物质的量浓度为
的物质的量浓度为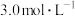 。
。
请计算:
(1)硫酸的物质的量浓度为________  。
。
(2)理论上此溶液最多可溶解铁粉的质量为________ g。
 ,已知溶液中各阳离子的物质的量浓度相等,
,已知溶液中各阳离子的物质的量浓度相等, 的物质的量浓度为
的物质的量浓度为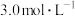 。
。请计算:
(1)硫酸的物质的量浓度为
 。
。(2)理论上此溶液最多可溶解铁粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积的关系如图所示(不考虑CO2在水中的溶解)。
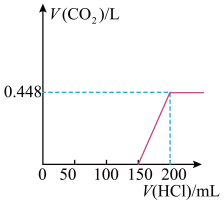
(1)写出 0~150mL 段发生反应的离子方程式为:____________ ;150mL ~200mL段发生反应的离子方程式为:___________________ ;
(2)所用盐酸的物质的量浓度为_______________ ;
(3)将上述氢氧化钠固体样品溶于水,所形成溶液的溶质为___________ 、_________ (写化学式),其物质的量分别为 ____________ 、_______________ 。

(1)写出 0~150mL 段发生反应的离子方程式为:
(2)所用盐酸的物质的量浓度为
(3)将上述氢氧化钠固体样品溶于水,所形成溶液的溶质为
您最近一年使用:0次

 无土栽培用的营养液中含有
无土栽培用的营养液中含有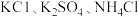 三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:
 的物质的量浓度为
的物质的量浓度为 ,含
,含 的质量为
的质量为 的物质的量为
的物质的量为 的浓度
的浓度 随溶液体积
随溶液体积 变化的曲线如图乙所示,则
变化的曲线如图乙所示,则


