下列说法中可以说明密闭容器中的反应: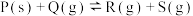 在恒温下已达平衡状态的是
在恒温下已达平衡状态的是
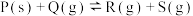 在恒温下已达平衡状态的是
在恒温下已达平衡状态的是| A.反应容器内压强不随时间变化而变化 |
| B.R和S的生成速率相等 |
| C.反应容器内P、Q、R、S四者共存 |
| D.反应容器内总物质的量不随时间变化而变化 |
18-19高三·浙江·期中 查看更多[1]
(已下线)【新东方】高中化学173
更新时间:2019/11/11 08:41:53
|
相似题推荐
单选题
|
适中
(0.65)
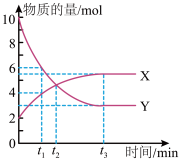
【推荐1】一定温度下,2L的密闭容器中,X、Y、Z三种气体的物质的量随反应时间的变化曲线如图所示,10s时达到平衡。下列说法不正确的是
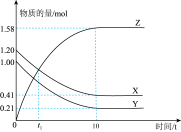
A.从反应开始到10s内,用Z的浓度变化表示的平均反应速率为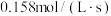 |
| B.t1s时,Z和X浓度相等,正反应速率大于逆反应速率 |
| C.当X的物质的量不再随时间而变化,此时正、逆反应速率相等,但不为零 |
D.反应的化学方程式为: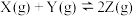 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定温度下将1molCO和1molH2O (g)通入一个密闭容器中反应:CO(g)+H2O(g)  CO2(g)+H2(g),达到平衡后CO2的物质的量为0.67mol,再通入4molH2O (g)达到平衡后CO2的物质的量可能是
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.67mol,再通入4molH2O (g)达到平衡后CO2的物质的量可能是
 CO2(g)+H2(g),达到平衡后CO2的物质的量为0.67mol,再通入4molH2O (g)达到平衡后CO2的物质的量可能是
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.67mol,再通入4molH2O (g)达到平衡后CO2的物质的量可能是| A.等于0.6mol | B.等于lmol | C.大于lmol | D.等于0.94mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】起始体积相等的Ⅰ、Ⅱ容器中分别充入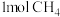 和
和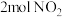 ,发生反应:
,发生反应: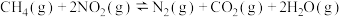 。实验如下:
。实验如下:
下列大小比较中,正确的是
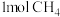 和
和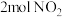 ,发生反应:
,发生反应: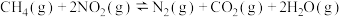 。实验如下:
。实验如下:| 容器 | Ⅰ | Ⅱ |
| 反应条件 | 恒温恒容 | 恒温恒压 |
| 气体密度 |  (Ⅰ) (Ⅰ) |  (Ⅱ) (Ⅱ) |
 平衡转化率 平衡转化率 |  (Ⅰ) (Ⅰ) |  (Ⅱ) (Ⅱ) |
| 达到平衡所用时间 | t(Ⅰ) | t(Ⅱ) |
| 气体平均摩尔质量 | M(Ⅰ) | M(Ⅱ) |
A. (Ⅰ)> (Ⅰ)> (Ⅱ) (Ⅱ) | B.t(Ⅰ)>t(Ⅱ) | C. (Ⅰ)> (Ⅰ)> (Ⅱ) (Ⅱ) | D.M(Ⅰ)<M(Ⅱ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一个绝热恒容的密闭容器中发生可逆反应:mA(g)+nB(g) pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明该反应达到平衡状态的是
pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明该反应达到平衡状态的是
| A.体系的压强不再改变 | B.混合气体的密度不再改变 |
| C.v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q | D.体系的温度不再变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】可以证明可逆反应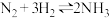 已达到平衡状态的是
已达到平衡状态的是
①其他条件不变时,混合气体平均相对分子质量不再改变
②一个 键断裂的同时,有3个
键断裂的同时,有3个 键断裂
键断裂
③恒温恒容时,体系压强不再改变
④ 的体积分数都不再改变
的体积分数都不再改变
⑤恒温恒容时,混合气体密度保持不变
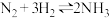 已达到平衡状态的是
已达到平衡状态的是①其他条件不变时,混合气体平均相对分子质量不再改变
②一个
 键断裂的同时,有3个
键断裂的同时,有3个 键断裂
键断裂③恒温恒容时,体系压强不再改变
④
 的体积分数都不再改变
的体积分数都不再改变⑤恒温恒容时,混合气体密度保持不变
| A.全部 | B.①③④⑤ | C.③⑤ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上常用煤和水为原料经过多步反应制得氢气,其中一步反应原理为CO(g)+H2O(g) CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是
CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是
 CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是
CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是| A.单位时间内消耗1mol的H2O同时生成1mol的H2 |
| B.两个H—O断裂的同时有两个C=O断裂 |
| C.反应容器内的气体密度不再发生变化 |
| D.混合气体的相对分子质量不再发生变化 |
您最近一年使用:0次

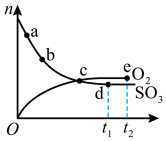
 SiHCl3(g)+H2(g)。不能表明该反应达到平衡状态的是
SiHCl3(g)+H2(g)。不能表明该反应达到平衡状态的是

