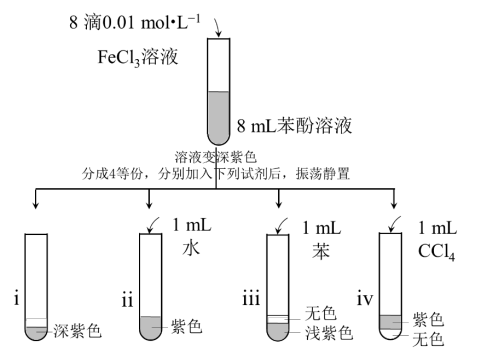
下列实验方案正确且能达到实验目的是( )


| A.用图1装置制取并收集乙酸乙酯 |
| B.用图2装置除去CO2气体中的HCl杂质 |
| C.用图3装置检验草酸晶体中是否含有结晶水 |
| D.用图4装置可以完成“喷泉实验” |
更新时间:2019-10-23 17:19:46
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | ①将湿润的红色石蕊试纸靠近试管口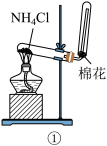 | 试纸不变色 |  受热不分解 受热不分解 |
| B | ②中振荡后静置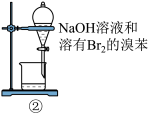 | 下层液体颜色变浅 |  溶液可除去溶在溴苯中的 溶液可除去溶在溴苯中的 |
| C | ③旋开活塞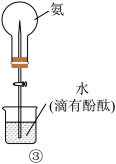 | 观察到红色喷泉 |  极易溶于水,氨水显碱性 极易溶于水,氨水显碱性 |
| D | ④闭合开关K,形成原电池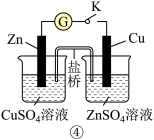 | Zn极上有红色固体析出 | 锌的金属性比铜强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】用圆底烧瓶收集NH3后进行喷泉实验。对实验现象的分析正确的是


| A.烧瓶中形成喷泉,说明NH3与H2O发生了反应 |
| B.烧瓶中剩余少量气体,能证明NH3的溶解已达饱和 |
C.烧瓶中溶液为红色的原因是:NH3+H2O NH3•H2O NH3•H2O NH NH +OH- +OH- |
| D.烧瓶中溶液露置在空气中一段时间后pH下降,能证明氨水具有挥发性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】中学常见的某反应的化学方程式为a+b→c+d+H2O(未配平,条件略去)。下列叙述不正确的是()
| A.若a是铁,b是稀硝酸(过量),且a可溶于c溶液中。则a与b反应的离子方程式为Fe+4H++NO3-=Fe3++NO↑+2H2O |
| B.若c,d均为气体,且都能使澄清石灰水变浑浊,则将混合气体通入溴水中,橙色褪去,其褪色过程的离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br- |
| C.若c是无色刺激性气味的气体,其水溶液呈弱碱性。在标准状况下用排空气法收集c气体得平均摩尔质量为20g·mol-1的混合气体进行喷泉实验。假设溶质不扩散,实验完成后所得溶液的物质的量浓度约为0.056mol·L-1 |
| D.若a是造成温室效应的主要气体之一,c、d均为钠盐,参加反应的a、b物质的量之比为4:5,则上述反应的离子方程式为4CO2+5OH-=CO32+3HCO3-+H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】化学实验如果设计或操作不当,可能看不到预期的现象。下列关于实验现象的分析不正确的是
| 选项 | A | B | C | D |
| 装置 | 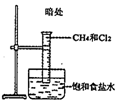 甲烷与氯气反应 | 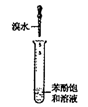 苯酚与溴水反应 | 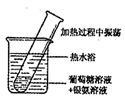 银镜反应 | 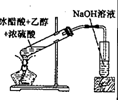 制备乙酸乙酯 |
| 现象 | 量筒中未出现油状液体 | 试管中未看到白色沉淀 | 试管中有黑色沉淀,但未出现银镜 | NaOH溶液中未看到油状液体 |
| 原因 | 甲烷与氯气未反应 | 苯酚浓度较大 | 反应未生成单质银 | 产物水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列选项中除杂试剂或操作正确的是
选项 | 物质(杂质) | 除杂试剂或操作 |
A | 甲烷(丙烯) | 酸性高锰酸钾溶液 |
B | 乙酸乙酯(乙醇) | 浓硫酸、乙酸、加热 |
C | 二氧化硫(乙烯) | 溴水 |
D | 蛋白质溶液(NaCl) | 渗析 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某固体粉末由NaCl、NaBr、(NH4)2CO3、Na2SO3、Na2SO4中的一种或几种组成,取该固体粉末wg进行如下实验(所加试剂均足量):
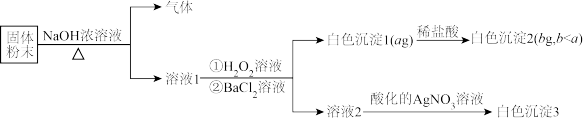
根据实验结果,下列有关说法正确的是

根据实验结果,下列有关说法正确的是
| A.原固体粉末中含有NaCl |
| B.若溶液1中只加BaCl2溶液,则生成的白色沉淀1的质量小于或等于a g |
| C.原固体粉末中必含有(NH4 )2CO3、Na2SO3 |
| D.测定出白色沉淀3的质量可以确定原固体粉末的组成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】鉴别NaCl、NaBr、NaI可以选用的试剂是
| A.碘水、淀粉溶液 | B.溴水、淀粉溶液 | C.氯水、CCl4 | D.溴水、CCl4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】某强酸性无色溶液中可能含表中离子中的若干种离子。
实验I:取少量该强酸性溶液A进行如图实验。
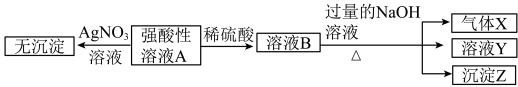
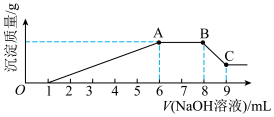
实验II:为了进一步确定该溶液的组成,取100mL原溶液A,向该溶液中滴加1mol•L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
回答下列问题:
(1)不进行实验就可以推断出,表中的离子一定不存在的有_______ 种。
(2)气体X的电子式为_______ ,沉淀Z的化学式为_______ 。
(3)写出实验II的图示中BC段对应反应的离子方程式:_______ 。
(4)A点对应的固体质量为_______ g。
(5)通过实验I可以确定该溶液中一定存在的阴离子是_______ 。推算该溶液中阴离子的浓度为_______ mol•L-1。
| 阳离子 | Mg2+、NH 、Ba2+、Al3+、Fe2+ 、Ba2+、Al3+、Fe2+ |
| 阴离子 | SiO 、MnO 、MnO 、Cl⁻、NO 、Cl⁻、NO 、CO 、CO |

实验II:为了进一步确定该溶液的组成,取100mL原溶液A,向该溶液中滴加1mol•L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。

回答下列问题:
(1)不进行实验就可以推断出,表中的离子一定不存在的有
(2)气体X的电子式为
(3)写出实验II的图示中BC段对应反应的离子方程式:
(4)A点对应的固体质量为
(5)通过实验I可以确定该溶液中一定存在的阴离子是
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列装置或操作能达到目的的是


| A.装置①用于测定生成氢气的速率 |
| B.装置②依据褪色快慢比较浓度对反应速率的影响 |
| C.装置③依据U形管两边液面的高低判断Na和水反应的热效应 |
| D.装置④依据出现浑浊的快慢比较温度对反应速率的影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】向AlCl3、FeCl2、FeCl3的混和溶液中逐滴加入NaOH溶液,达到除去Fe2+、Fe3+的目的,以下推断正确的是
已知:①Fe(OH)2为絮状,不易从溶液中除去;
②Fe(OH)3、Fe(OH)2、Al(OH)3沉淀的生成与溶解的pH列于下表。
已知:①Fe(OH)2为絮状,不易从溶液中除去;
②Fe(OH)3、Fe(OH)2、Al(OH)3沉淀的生成与溶解的pH列于下表。
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 完全沉淀 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.7 | 3.7 | — | — |
| Fe(OH)2 | 7.6 | 9.6 | ||
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| A.为了达到目的,首先应在溶液中加入双氧水或氯水将Fe2+氧化为Fe3+ |
| B.加入NaOH溶液,调节溶液的pH在9.6以上就能达到实验目的 |
| C.本实验产生沉淀的顺序为Fe(OH)3→Al(OH)3→Fe(OH)2 |
| D.实验中生成的Fe(OH)2迅速变为灰绿色,最终变为红褐色沉淀 |
您最近一年使用:0次


 的作用是防止倒吸
的作用是防止倒吸 H3Fe(OC6H5) 6 + 3H+,其中H3Fe(OC6H5) 6显紫色。实验如下:
H3Fe(OC6H5) 6 + 3H+,其中H3Fe(OC6H5) 6显紫色。实验如下: