写出下列反应的离子方程式:
(1)氢氧化钠溶液与氯化铁溶液:___ 。
(2)盐酸与硝酸银溶液:__ 。
(3)氯气溶于水:___ 。
(4)过氧化钠与水作用:__ 。
(1)氢氧化钠溶液与氯化铁溶液:
(2)盐酸与硝酸银溶液:
(3)氯气溶于水:
(4)过氧化钠与水作用:
更新时间:2019-11-25 08:44:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】对于数以千万计的化学物质,分类法的作用几乎是无可替代的。
(1)纯净物根据其组成和性质可进行如下分类,该分类方法属于___________ 。

(2)现有下列物质:①NaCl晶体 ②液态 HCl ③CaCO3固体 ④CO2⑤铜 ⑥稀硫酸 ⑦酒精。上述物质中能导电的是___________ (填序号,下同),属于电解质的是___________ 。
(3)某化学兴趣小组对下列四组物质进行研究。
A组: HCl、H2SO4、H2CO3、HNO3
B组:Na2CO3、NaNO3、AgNO3、Ba( NO3)2
C组:FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe( OH)3胶体
D组:NaOH、KOH、 Ba(OH)2、Fe2O3
①填写下列空白:
②写出上表中“不属于该类别的物质”间发生反应的离子方程式:
某物质的溶液+ Na2CO3→气体:___________ ;
某物质的溶液+ Fe2O3:___________ 。
(1)纯净物根据其组成和性质可进行如下分类,该分类方法属于

(2)现有下列物质:①NaCl晶体 ②液态 HCl ③CaCO3固体 ④CO2⑤铜 ⑥稀硫酸 ⑦酒精。上述物质中能导电的是
(3)某化学兴趣小组对下列四组物质进行研究。
A组: HCl、H2SO4、H2CO3、HNO3
B组:Na2CO3、NaNO3、AgNO3、Ba( NO3)2
C组:FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe( OH)3胶体
D组:NaOH、KOH、 Ba(OH)2、Fe2O3
①填写下列空白:
| 组别 | A组 | B组 | C组 | D组 |
| 分类标准 | 含氧酸 | 硝酸盐 | 分散系 | |
| 不属于该类别的物质 | HCl | Na2CO3 | Fe2O3 |
②写出上表中“不属于该类别的物质”间发生反应的离子方程式:
某物质的溶液+ Na2CO3→气体:
某物质的溶液+ Fe2O3:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列十种物质:①H2②铝③CaO固体④熔化的KNO3⑤NaHSO4固体⑥Ba(OH)2固体⑦氢氧化铁胶体⑧氨水⑨纯硝酸⑩Al2(SO4)3固体
(1)上述物质中属于电解质的是________________ (填序号),上述状态下的物质中能导电的有___________ ,上述状态下的电解质不能导电的有____________________ 。
(2)⑩在水中的电离方程式为_____________________________ 。
(3)上述物质中有两种物质的溶液之间可发生离子反应H++OH-=H2O,该离子反应对应的化学方程式为___________________________________________________ 。
(4)少量的CO2通入⑥的溶液中反应的离子方程式为____________________________ 。
(5)将⑥的溶液逐滴加入⑤的溶液中,恰好使溶液中的SO 沉淀完全的离子方程式为
沉淀完全的离子方程式为_________________________________________ 。
(1)上述物质中属于电解质的是
(2)⑩在水中的电离方程式为
(3)上述物质中有两种物质的溶液之间可发生离子反应H++OH-=H2O,该离子反应对应的化学方程式为
(4)少量的CO2通入⑥的溶液中反应的离子方程式为
(5)将⑥的溶液逐滴加入⑤的溶液中,恰好使溶液中的SO
 沉淀完全的离子方程式为
沉淀完全的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关的离子方程式为_______ 。
(4)原溶液可能大量共存的阴离子是_______(填字母)。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是_______(填字母)。
| A.Cl- | B.NO | C.CO | D.OH- |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按照下列要求填空:下列物质中①干冰②食盐水③熔融氢氧化钠④铁⑤硫酸铜 ⑥NaHCO3晶体⑦空气⑧稀硫酸。
(1)a.属于混合物的是___________ ;
b.属于氧化物的是___________ ;
c.属于电解质的是___________ ;
d.属于非电解质的是___________ 。
(2)a.写出稀硫酸的电离方程式:___________ 。
b.向⑧中加入少量⑥的离子方程式为___________ ;
c.在溶液中,④与⑤反应的离子方程式为___________ 。
(1)a.属于混合物的是
b.属于氧化物的是
c.属于电解质的是
d.属于非电解质的是
(2)a.写出稀硫酸的电离方程式:
b.向⑧中加入少量⑥的离子方程式为
c.在溶液中,④与⑤反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用一种试剂除去下列物质中的杂质(括号内物质为杂质,所用试剂均为适量),写出所加的试剂(写化学式)及有关反应的离子方程式。
(1)FeSO4溶液(CuSO4):所加试剂:_______ ,离子方程式: _______ 。
(2)Cu(Mg):所加试剂:_______ ,离子方程式: _______ 。
(3)CO(CO2):所加试剂:_______ ,离子方程式:_______ 。
(4)BaCl2(HCl):试剂_______ ,离子方程式为:_______ 。
(1)FeSO4溶液(CuSO4):所加试剂:
(2)Cu(Mg):所加试剂:
(3)CO(CO2):所加试剂:
(4)BaCl2(HCl):试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.现有中学化学中常见的八种物质:
①固体氢氧化钡②石墨棒③纯醋酸④液态氯化氢⑤硫酸氢钾固体⑥熔融氯化钠⑦蔗糖⑧干冰
请用序号填空:
(1)上述状态下可导电的是___________ ,属于非电解质的是___________ 。
Ⅱ.电解质溶液中自由移动离子的浓度越大,溶液导电能力就越大。现用如图装置向两份相同的滴有酚酞溶液的 溶液中,分别滴入导电能力相等的、
溶液中,分别滴入导电能力相等的、 溶液,测得混合溶液的导电能力随滴入溶液的体积变化曲线如下图所示。
溶液,测得混合溶液的导电能力随滴入溶液的体积变化曲线如下图所示。

(2)表示滴加 溶液的导电能力变化为曲线
溶液的导电能力变化为曲线___________ 。
(3)曲线①s→a反应的现象为___________ 。
(4)曲线②s→b反应的离子方程式为___________ 。
(5)溶液中 沉淀完全的有
沉淀完全的有___________ 点(填a、b、c、d)。
(6)若往两曲线的交点c溶液分别滴加 溶液,反应的离子方程式分别为:
溶液,反应的离子方程式分别为:
曲线①___________ 。
曲线②___________ 。
①固体氢氧化钡②石墨棒③纯醋酸④液态氯化氢⑤硫酸氢钾固体⑥熔融氯化钠⑦蔗糖⑧干冰
请用序号填空:
(1)上述状态下可导电的是
Ⅱ.电解质溶液中自由移动离子的浓度越大,溶液导电能力就越大。现用如图装置向两份相同的滴有酚酞溶液的
 溶液中,分别滴入导电能力相等的、
溶液中,分别滴入导电能力相等的、 溶液,测得混合溶液的导电能力随滴入溶液的体积变化曲线如下图所示。
溶液,测得混合溶液的导电能力随滴入溶液的体积变化曲线如下图所示。
(2)表示滴加
 溶液的导电能力变化为曲线
溶液的导电能力变化为曲线(3)曲线①s→a反应的现象为
(4)曲线②s→b反应的离子方程式为
(5)溶液中
 沉淀完全的有
沉淀完全的有(6)若往两曲线的交点c溶液分别滴加
 溶液,反应的离子方程式分别为:
溶液,反应的离子方程式分别为:曲线①
曲线②
您最近一年使用:0次
【推荐1】KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为:_____ KClO3+________ HCl(浓)→_________ KCl+_______ ClO2↑+______ Cl2↑+__________ H2O
(1)请配平该化学方程式(未知系数填入横线内)。
(2)浓盐酸在反应中显示出来的性质是________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)5 ℃ 下将产物氯气0.1 mol溶于水配成1 L溶液,请写出氯气溶于水的化学反应方程式____________________ 。
(4)若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:______________________________________________ 。
(1)请配平该化学方程式(未知系数填入横线内)。
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)5 ℃ 下将产物氯气0.1 mol溶于水配成1 L溶液,请写出氯气溶于水的化学反应方程式
(4)若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。

回答下列问题:
(1)X在水中的电离方程式为_______ 。
(2)Y可用于实验室制O2,其焰色试验为紫色,则Y的化学式为_______ ;Y在400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种是含氧酸盐,则生成这两种盐的物质的量之比是_______ 。
(3)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的_______ 倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示)。
(4)Cl2O熔点-116℃,沸点2℃,容易与水反应生成次氯酸,与空气混合容易爆炸。Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为________ ,适宜的收集方法是_______ 。

回答下列问题:
(1)X在水中的电离方程式为
(2)Y可用于实验室制O2,其焰色试验为紫色,则Y的化学式为
(3)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的
(4)Cl2O熔点-116℃,沸点2℃,容易与水反应生成次氯酸,与空气混合容易爆炸。Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学知识,按要求填空。

(1)上述第一级分类标准(分成A、B组)的依据为___ 。
(2)C组中某一物质常温能与冷水反应,其离子方程式为___ 。
(3)D组中与水反应时氧化剂和还原剂物质的量之比为1:1的物质有____ 。
(4)F组中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因:___ 。
(5)E组中某一物质的水溶液可使酸性KMnO4溶液褪色,用离子方程式表示褪色的原因:___ 。

(1)上述第一级分类标准(分成A、B组)的依据为
(2)C组中某一物质常温能与冷水反应,其离子方程式为
(3)D组中与水反应时氧化剂和还原剂物质的量之比为1:1的物质有
(4)F组中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因:
(5)E组中某一物质的水溶液可使酸性KMnO4溶液褪色,用离子方程式表示褪色的原因:
您最近一年使用:0次
【推荐1】呼吸面具中的Na2O2可吸收CO2放出O2,若用超氧化钾(KO2)代替Na2O2也可以得到类似的产物,起到同样的作用。
(1)标准状况下,若有30mL的CO2气体通过盛有足量的KO2的装置充分反应后,逸出气体的体积为_______ mL;
(2)标准状况下,若一定量的CO2(过量),通过盛有7.24gKO2和Na2O2的均匀混合物的装置充分反应后,逸出的气体中O2体积为1568mL,则混合物中KO2和Na2O2的物质的量分别为:KO2_______ mol、Na2O2_______ mol;
(3)比较Na2O2和KO2中氧氧键的键能大小,并说明理由:_______ 。
(1)标准状况下,若有30mL的CO2气体通过盛有足量的KO2的装置充分反应后,逸出气体的体积为
(2)标准状况下,若一定量的CO2(过量),通过盛有7.24gKO2和Na2O2的均匀混合物的装置充分反应后,逸出的气体中O2体积为1568mL,则混合物中KO2和Na2O2的物质的量分别为:KO2
(3)比较Na2O2和KO2中氧氧键的键能大小,并说明理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.按要求写出下列反应的方程式
(1)铝与足量氢氧化钠溶液反应的离子方程式______
(2)过氧化钠与水反应的化学方程式____
(3) 实验室制氢氧化铝的离子方程式________
Ⅱ. 请补充完整,配平方程式并用单线桥标出电子转移方向和数目
(1)KI+KIO3+H2SO4═I2+K2SO4+H2O:________________________
(2)MnO4-+NO2-+ ═Mn2++NO3-+H2O:_________________________
(1)铝与足量氢氧化钠溶液反应的离子方程式
(2)过氧化钠与水反应的化学方程式
(3) 实验室制氢氧化铝的离子方程式
Ⅱ. 请补充完整,配平方程式并用单线桥标出电子转移方向和数目
(1)KI+KIO3+H2SO4═I2+K2SO4+H2O:
(2)MnO4-+NO2-+ ═Mn2++NO3-+H2O:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】物质类别和元素价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价—类”二维图,请回答下列问题:
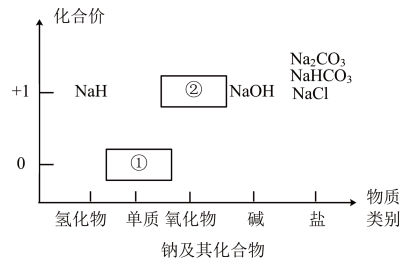
(1)①与水反应的离子方程式为______ ;通常将①的固体保存在______ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式为______ 。
(3)从元素价态的视角看, 中氢元素的化合价为
中氢元素的化合价为______ 价,从H的价态分析, 常用作
常用作______ (填“氧化剂”或“还原剂”), 与水反应生成一种强碱和可燃性气体,反应的化学方程式为
与水反应生成一种强碱和可燃性气体,反应的化学方程式为______ 。
(4)纯碱和小苏打都是重要的化工原料,根据不列三组实验,回答:
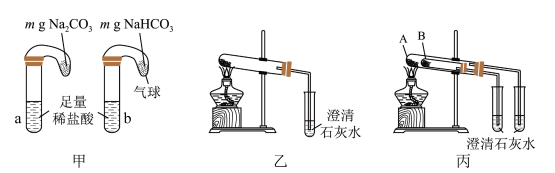
①甲组实验能鉴别纯碱和小苏打的实验现象是______ ;试管b中发生反应的离子方程式为______ 。
②乙、丙两组实验中,______ 组能更便捷的验证两者的热稳定性(填“乙”或“丙”),丙组实验中A处盛放的物质为______ (填化学式)。

(1)①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式为
(3)从元素价态的视角看,
 中氢元素的化合价为
中氢元素的化合价为 常用作
常用作 与水反应生成一种强碱和可燃性气体,反应的化学方程式为
与水反应生成一种强碱和可燃性气体,反应的化学方程式为(4)纯碱和小苏打都是重要的化工原料,根据不列三组实验,回答:

①甲组实验能鉴别纯碱和小苏打的实验现象是
②乙、丙两组实验中,
您最近一年使用:0次



