氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是_____ 。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2﹣N2+HCl
①该反应中被氧化的元素是_____ (填元素名称),氧化剂是_____ (填化学式)。
②配平该方程式:_____ NH3+_____ Cl2=_____ N2+_____ HCl
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为_____ 。
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为_____ 。
(1)下列表述中没有氧化还原反应发生的是
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2﹣N2+HCl
①该反应中被氧化的元素是
②配平该方程式:
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为
19-20高一上·湖南娄底·期中 查看更多[3]
(已下线)第11讲 氧化还原反应的应用和配平-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)辽宁省铁岭市开原市第二高级中学2021届高三第一次模拟考试化学试题湖南省娄底市娄星区2019-2020学年高一上学期期中考试化学试题
更新时间:2019-11-26 13:58:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填空。
(1)2molO3和3molO2的分子数之比为___________ ,原子数之比___________ 。
(2)某氯化物MCl219g,含有0.4molCl-,M的摩尔质量为___________ 。
(3)同温同压下,同体积的CH4气体和CO气体质量之比为___________ ,质子数之比为___________ 。
(4)从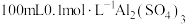 溶液中取出10mL,则10mL溶液中
溶液中取出10mL,则10mL溶液中 物质的量为
物质的量为___________ 。 的物质的量浓度是
的物质的量浓度是___________ 。
(1)2molO3和3molO2的分子数之比为
(2)某氯化物MCl219g,含有0.4molCl-,M的摩尔质量为
(3)同温同压下,同体积的CH4气体和CO气体质量之比为
(4)从
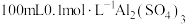 溶液中取出10mL,则10mL溶液中
溶液中取出10mL,则10mL溶液中 物质的量为
物质的量为 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)将9.5gMgCl2溶于水配成1L溶液,所得溶液的物质的量浓度为___ mol/L,500mL该溶液中所含Cl-的物质的量为___ mol。
(2)含有2NA个氢原子的CH4的质量为___ g。
(3)现有以下物质:①熔融NaCl ②液氨 ③醋酸水溶液 ④HCl气体 ⑤酒精(C2H5OH)。请用下列序号填空:能导电的是___ (填选项);属于电解质的是___ (填选项)。
A.①③ B.②④ C.①④ D.②③
(2)含有2NA个氢原子的CH4的质量为
(3)现有以下物质:①熔融NaCl ②液氨 ③醋酸水溶液 ④HCl气体 ⑤酒精(C2H5OH)。请用下列序号填空:能导电的是
A.①③ B.②④ C.①④ D.②③
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列10种物质:① 溶液;②石墨;③
溶液;②石墨;③ ;④
;④ ;⑤熔融
;⑤熔融 ;⑥
;⑥ 溶液;⑦蛋白质胶体;⑧
溶液;⑦蛋白质胶体;⑧ 溶液;⑨乙醇;⑩固体
溶液;⑨乙醇;⑩固体 。
。
(1)属于电解质且能导电的是__________ (填序号,下同),属于非电解质的是___________ .
(2)⑥和⑦的本质区别是________________ .
(3)将⑩加到①中,发生反应的离子方程式为_____________________________ .
(4)含有相同物质的量溶质的⑥和⑩的水溶液混合后,再加入 发生反应的离子方程式为
发生反应的离子方程式为_______________________________ .
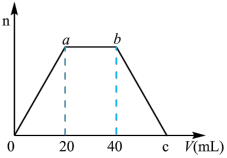
(5)向⑤和⑥制成得混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是____________ mL;写出ab段发生的离子方程式:_______________ .
 溶液;②石墨;③
溶液;②石墨;③ ;④
;④ ;⑤熔融
;⑤熔融 ;⑥
;⑥ 溶液;⑦蛋白质胶体;⑧
溶液;⑦蛋白质胶体;⑧ 溶液;⑨乙醇;⑩固体
溶液;⑨乙醇;⑩固体 。
。(1)属于电解质且能导电的是
(2)⑥和⑦的本质区别是
(3)将⑩加到①中,发生反应的离子方程式为
(4)含有相同物质的量溶质的⑥和⑩的水溶液混合后,再加入
 发生反应的离子方程式为
发生反应的离子方程式为(5)向⑤和⑥制成得混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是

您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中,氧化剂是___________ ,还原剂是_________ ,氧化产物是_______ ,还原产物是________ .请用双线桥法表示出该反应中电子转移的方向和数目______ .
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。如图是硫、氮两元素的价类二维图。
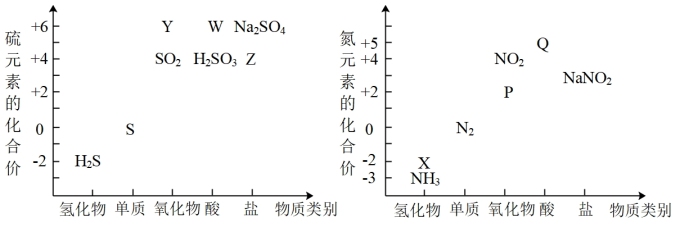
请回答下列问题:
(1)物质X可作为火箭发动机的燃料,其结构式为_______ 。
(2)宋代著名法医学家宋慈的 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为: (反应未配平),已知:
(反应未配平),已知: 为一种不溶于水的灰黑色固体。以下有关说法
为一种不溶于水的灰黑色固体。以下有关说法错误 的是_______(填字母)。
(3)已知物质Z是一种可溶性正盐能被酸性K2Cr2O7溶液氧化为Na2SO4,Cr2O 被还原Cr3+,请写出此反应的离子方程式为
被还原Cr3+,请写出此反应的离子方程式为_______ 。
(4)大苏打 在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是_______
在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是_______ 填字母
填字母 。
。
(5)氮的氧化物(NOx)是常见的大气污染物之一, 催化还原氮氧化物
催化还原氮氧化物 技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质
技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质 与NO2的物质的量之比为
与NO2的物质的量之比为 时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,请写出该反应的化学方程式为
时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,请写出该反应的化学方程式为_______ 。
(6)将 铜与
铜与 一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质
一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质 和二氧化氮混合气体共
和二氧化氮混合气体共 。则混合气体中物质
。则混合气体中物质 的体积为
的体积为_______ 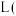 标准状况下
标准状况下 ,待反应结束后,向溶液中加入
,待反应结束后,向溶液中加入 的氢氧化钠溶液,恰好使溶液中的
的氢氧化钠溶液,恰好使溶液中的 全部转化为沉淀,则原物质Q的物质的量浓度为
全部转化为沉淀,则原物质Q的物质的量浓度为_______  。
。

请回答下列问题:
(1)物质X可作为火箭发动机的燃料,其结构式为
(2)宋代著名法医学家宋慈的
 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为: (反应未配平),已知:
(反应未配平),已知: 为一种不溶于水的灰黑色固体。以下有关说法
为一种不溶于水的灰黑色固体。以下有关说法| A.当银针变黑时,说明所检验的物质中可能有毒 |
B.银针验毒时, 被氧化 被氧化 |
| C.上述验毒反应中氧化剂和还原剂的物质的量之比为4:1 |
D. 在上述验毒反应中作还原剂 在上述验毒反应中作还原剂 |
 被还原Cr3+,请写出此反应的离子方程式为
被还原Cr3+,请写出此反应的离子方程式为(4)大苏打
 在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是_______
在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是_______ 填字母
填字母 。
。A. | B. |
C. | D. |
 催化还原氮氧化物
催化还原氮氧化物 技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质
技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质 与NO2的物质的量之比为
与NO2的物质的量之比为 时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,请写出该反应的化学方程式为
时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,请写出该反应的化学方程式为(6)将
 铜与
铜与 一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质
一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质 和二氧化氮混合气体共
和二氧化氮混合气体共 。则混合气体中物质
。则混合气体中物质 的体积为
的体积为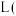 标准状况下
标准状况下 ,待反应结束后,向溶液中加入
,待反应结束后,向溶液中加入 的氢氧化钠溶液,恰好使溶液中的
的氢氧化钠溶液,恰好使溶液中的 全部转化为沉淀,则原物质Q的物质的量浓度为
全部转化为沉淀,则原物质Q的物质的量浓度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(12分)(1)已知离子反应: +6I-+6H+=R-+3I2+3H2O,n=
+6I-+6H+=R-+3I2+3H2O,n=____ ,R元素在 中的化合价是
中的化合价是_____ 。
(2)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:

① 在上述有编号的步骤中,需用氧化剂的是______ (填编号)。
②完成并配平下列反应的化学方程式,按要求标出电子转移的方向和数目,并回答问题:
__ Na2Cr2O7+__ KI+__ HCl——__ CrCl3+_NaCl+__ KCl+__ I2+ (用单线桥表示电子转移的方向、数目),当反应中有3mol电子转移时,氧化产物的质量是
(用单线桥表示电子转移的方向、数目),当反应中有3mol电子转移时,氧化产物的质量是_______ 。
 +6I-+6H+=R-+3I2+3H2O,n=
+6I-+6H+=R-+3I2+3H2O,n= 中的化合价是
中的化合价是(2)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:

① 在上述有编号的步骤中,需用氧化剂的是
②完成并配平下列反应的化学方程式,按要求标出电子转移的方向和数目,并回答问题:
 (用单线桥表示电子转移的方向、数目),当反应中有3mol电子转移时,氧化产物的质量是
(用单线桥表示电子转移的方向、数目),当反应中有3mol电子转移时,氧化产物的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)指出氧在下列各物质中的化合价,分别写出由氧气在一定条件下生成下列物质的化学方程式(必须注明反应条件)。
①Na2O:____________ ,_______________________________ 。
②Na2O2:___________ ,____________________________________ 。
(2)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式___________________________________________________ 。
(3)人体内O 对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
_____ O2-+_____ H2O=____ H2O2+O2+___ ______
①Na2O:
②Na2O2:
(2)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式
(3)人体内O
 对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
对健康有害,使人过早衰老,但在催化剂SOD存在下可以发生如下反应,请完成该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知铜在常温下能被稀HNO3溶解。反应方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO ↑+4H2O
(1)请将上述反应改成离子方程式____ 。
(2)用双线桥法表示电子得失的方向和数目:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O。___
(3若生成896mL的NO(标准状况下),则该过程中转移的电子数目是___ 。
(4)氧化剂与氧化产物的物质的量比为___ 。
Ⅱ.某反应体系有反应物和生成物共7种物质:C、H2SO4、K2CrO4、K2SO4、CO2、Cr2(SO4)3和H2O。已知该反应中发生如下过程:C→CO2。该反应的化学方程式:___ 。
(1)请将上述反应改成离子方程式
(2)用双线桥法表示电子得失的方向和数目:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O。
(3若生成896mL的NO(标准状况下),则该过程中转移的电子数目是
(4)氧化剂与氧化产物的物质的量比为
Ⅱ.某反应体系有反应物和生成物共7种物质:C、H2SO4、K2CrO4、K2SO4、CO2、Cr2(SO4)3和H2O。已知该反应中发生如下过程:C→CO2。该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】中国环境监测总站数据显示,颗粒物 等
等 为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对
为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对 、
、 、
、 等进行研究具有重要意义。请回答下列问题:
等进行研究具有重要意义。请回答下列问题:
(1)将 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据计算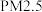 待测试样的pH =
待测试样的pH =___________ 。
(2)汽车发动机工作时会引发 和
和 反应,当尾气中空气不足时,
反应,当尾气中空气不足时, 在催化转化器中被还原成
在催化转化器中被还原成 排出。写出NO被CO还原的化学方程式
排出。写出NO被CO还原的化学方程式________ 。
(3)碘循环工艺不仅能吸收 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:
①用离子方程式表示反应器中发生的反应_______ 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出 的目的是
的目的是_______ 。
(4)下图是用 脱除烟气中NO的原理。
脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为________  填化学式
填化学式 和H2O。
和H2O。
②当消耗 和
和 时,除去的NO在标准状况下的体积为
时,除去的NO在标准状况下的体积为____ L。
 等
等 为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对
为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对 、
、 、
、 等进行研究具有重要意义。请回答下列问题:
等进行研究具有重要意义。请回答下列问题: (1)将
 样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表: | 离子 |  |  |  |  | 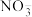 |  |
浓度 | 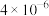 | 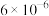 | 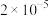 | 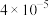 | 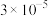 | 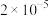 |
根据表中数据计算
 待测试样的pH =
待测试样的pH =(2)汽车发动机工作时会引发
 和
和 反应,当尾气中空气不足时,
反应,当尾气中空气不足时, 在催化转化器中被还原成
在催化转化器中被还原成 排出。写出NO被CO还原的化学方程式
排出。写出NO被CO还原的化学方程式(3)碘循环工艺不仅能吸收
 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下: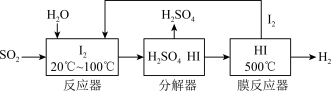
①用离子方程式表示反应器中发生的反应
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出
 的目的是
的目的是(4)下图是用
 脱除烟气中NO的原理。
脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为
 填化学式
填化学式 和H2O。
和H2O。②当消耗
 和
和 时,除去的NO在标准状况下的体积为
时,除去的NO在标准状况下的体积为
您最近一年使用:0次



