实验室可通过反应:3Cl2+6KOH 5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
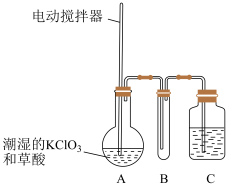
请回答下列问题:
(1)A 中反应的主要产物有:某种正盐、ClO2和CO2等,写出该反应的化学方程式:_____ 。
(2)请分析装置图,进行补充和完善。A部分缺________ 装置,B部分还应补充_______ 装置,还有一处设计明显不合理的是___________ (填“A”“B”或“C”)。
(3)C中的试剂为NaOH溶液时,反应生成NaClO3和NaClO2,写出该反应的离子方程式____ 。
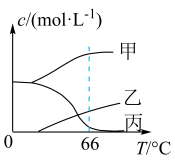
(4)在密闭容器中向9℃的KOH溶液中通入少量Cl2,此时Cl2的氧化产物主要是______ ;继续通入适量Cl2,将溶液加热,溶液中主要离子的浓度随温度的变化如图所示,图中甲、乙、丙依次表示的离子是__________ 、__________ 、__________ (不考虑Cl2的挥发)。
 5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
5KCl+KC1O3+3H2O 制取KC1O3,再用稍潮湿KC1O3和草酸(H2C2O4) 在60℃时反应制取ClO2气体,装置如图所示。ClO2是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。
请回答下列问题:
(1)A 中反应的主要产物有:某种正盐、ClO2和CO2等,写出该反应的化学方程式:
(2)请分析装置图,进行补充和完善。A部分缺
(3)C中的试剂为NaOH溶液时,反应生成NaClO3和NaClO2,写出该反应的离子方程式
(4)在密闭容器中向9℃的KOH溶液中通入少量Cl2,此时Cl2的氧化产物主要是

更新时间:2019-11-28 15:33:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室里用如图所示装置制取并验证氯气的部分化学性质同时制取纯净的无水FeCl3。

(1)写出装置A中生成氯气的化学方程式_______ 。
(2)装置B应盛放的试剂名称为_______ 。
(3)当有Cl2通过装置D时,干燥的有色布条能否褪色?_______ 。
(4)F装置所起的作用是_______ ,_______ 。
(5)此实验装置对制备目的的实现有何缺陷?_______ ,应如何改进?_______ 。

(1)写出装置A中生成氯气的化学方程式
(2)装置B应盛放的试剂名称为
(3)当有Cl2通过装置D时,干燥的有色布条能否褪色?
(4)F装置所起的作用是
(5)此实验装置对制备目的的实现有何缺陷?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学实验小组在实验室利用下图装鲁制取氯气并以氯气为原料制备其他物质。

回答下列问题:
(1)装置A圆底烧瓶中发生反应的离子方程式为___________ 。
(2)若用装置D制备少量氯化铁固体(氯化铁易吸水,在300 °C时升华),则:
①装置B内盛装饱和食盐水的作用是___________ 。
②装置C内盛装试剂为___________ 。
③装置D、E之间使用短粗导管的原因是___________ 。
(3)若在装置D的硬质玻璃管内盛装石英砂和炭粉,实验时发生如下反应:SiO2 +2C+2Cl2 SiCl4+ 2CO,已知SiCl4的熔点为一70°C,沸点为 57.7 °C,在潮湿空气中水解生成硅酸和氯化氢。
SiCl4+ 2CO,已知SiCl4的熔点为一70°C,沸点为 57.7 °C,在潮湿空气中水解生成硅酸和氯化氢。
①实验过程中,若装置E的广口瓶没有干燥,则装置E中出现的现象是_____ 。
②气球内收集到气体的主要成分是___________ 。

回答下列问题:
(1)装置A圆底烧瓶中发生反应的离子方程式为
(2)若用装置D制备少量氯化铁固体(氯化铁易吸水,在300 °C时升华),则:
①装置B内盛装饱和食盐水的作用是
②装置C内盛装试剂为
③装置D、E之间使用短粗导管的原因是
(3)若在装置D的硬质玻璃管内盛装石英砂和炭粉,实验时发生如下反应:SiO2 +2C+2Cl2
 SiCl4+ 2CO,已知SiCl4的熔点为一70°C,沸点为 57.7 °C,在潮湿空气中水解生成硅酸和氯化氢。
SiCl4+ 2CO,已知SiCl4的熔点为一70°C,沸点为 57.7 °C,在潮湿空气中水解生成硅酸和氯化氢。①实验过程中,若装置E的广口瓶没有干燥,则装置E中出现的现象是
②气球内收集到气体的主要成分是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某小组同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略).请按要求回答下列问题:

(1)装置A烧瓶中发生反应的化学方程式为________________________ 。
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→_____ 、_____ →_____ 、_____ →f→g→_____
(3)装置C中饱和食盐水的作用是__________________________ 。
(4)装置B中发生反应的离子方程式为_____________________________ 。
(5)加热装置D时,铜粉发生反应的化学方程式为___________________ 。

(1)装置A烧瓶中发生反应的化学方程式为
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→
(3)装置C中饱和食盐水的作用是
(4)装置B中发生反应的离子方程式为
(5)加热装置D时,铜粉发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成:BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。
Ⅰ.ZnSO4溶液的制备与提纯:
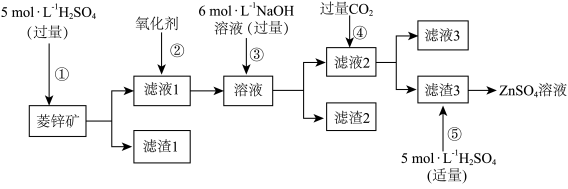
有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。
(1)若②中加入氧化剂为H2O2,写出离子反应方程式____ 。
(2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤___ (选填①、②、③、⑤)。
(3)滤渣2的主要成分为___ 。
(4)写出步骤④后产生滤渣3的离子反应方程式___ 。
Ⅱ.BaS溶液的制备:
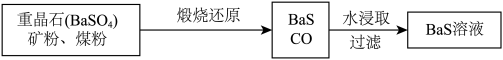
(5)写出煅烧还原的化学反应方程式____ 。
Ⅲ.制取锌钡白:
(6)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是___ 。
Ⅰ.ZnSO4溶液的制备与提纯:

有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。
(1)若②中加入氧化剂为H2O2,写出离子反应方程式
(2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤
(3)滤渣2的主要成分为
(4)写出步骤④后产生滤渣3的离子反应方程式
Ⅱ.BaS溶液的制备:

(5)写出煅烧还原的化学反应方程式
Ⅲ.制取锌钡白:
(6)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧化尿素(CO(NH2)2·H2O2)是过氧化氢水溶液与尿素的加和物,兼有尿素和过氧化氢的性质,是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。某化学小组同学用低浓度的双氧水和饱和尿素[CO(NH2)2]溶液在30℃条件下用右图装置合成过氧化尿素。请回答下列问题:

(1)仪器X的名称是______________ ;
(2)制备过氧化尿素的化学方程式为_______________________ ,反应时采取的受热方式为_____________ ;
(3)搅拌器不能选择铁质材料的原因是______________________
(4)过氧化尿素中活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品8.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL6mol·L-1H2SO4,然后用0.2000mol·L-1KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液与尿素不反应)。三次滴定平均消耗KMnO4溶液20.000mL:
①请完善滴定时反应的离子方程式:__ MnO +
+___ H2O2+______ ==_______________
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量_______ (填“偏高”、“偏低”或“不变”);
③根据滴定结果确定产品质量_______ (填“合格”或“不合格”),活性氧的质量分数为_________ 。

(1)仪器X的名称是
(2)制备过氧化尿素的化学方程式为
(3)搅拌器不能选择铁质材料的原因是
(4)过氧化尿素中活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品8.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL6mol·L-1H2SO4,然后用0.2000mol·L-1KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液与尿素不反应)。三次滴定平均消耗KMnO4溶液20.000mL:
①请完善滴定时反应的离子方程式:
 +
+②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
③根据滴定结果确定产品质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】富马酸亚铁为棕红色固体,较难溶于水,是一种治疗缺铁性贫血的安全有效的补铁制剂。某实验小组用富马酸 和
和 制备富马酸亚铁,并对其纯度进行测定,过程如下:
制备富马酸亚铁,并对其纯度进行测定,过程如下:
Ⅰ.制备富马酸亚铁
①将少量富马酸固体置于烧杯中,加入 热水搅拌使之溶解;
热水搅拌使之溶解;
②向烧杯中加入 一定浓度的
一定浓度的 溶液,控制
溶液,控制 为
为 ,并将其转移到仪器
,并将其转移到仪器 中;
中;
③通 并加热一段时间后,通过仪器
并加热一段时间后,通过仪器 缓慢加入
缓慢加入 新配置的
新配置的 溶液,继续加热约1小时后,出现大量棕红色沉淀。
溶液,继续加热约1小时后,出现大量棕红色沉淀。
④将反应混合液冷却后,减压过滤,洗涤,干燥,得粗产品。

(1)仪器 的名称是
的名称是___________ ,仪器 适宜的规格是
适宜的规格是___________ 。
A. B.
B. C.
C.
(2)通 的目的是
的目的是___________ 。
(3)合成富马酸亚铁反应的化学方程式为___________ 。
(4)采用减压过滤的优点是___________ 。
Ⅱ.产品纯度测定
取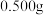 样品置于
样品置于 锥形瓶中,加入
锥形瓶中,加入 稀硫酸,加热使之溶解,冷却后再加入
稀硫酸,加热使之溶解,冷却后再加入 新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇
新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用 硫酸铈铵
硫酸铈铵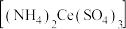 标准液滴定(还原产物为
标准液滴定(还原产物为 ),滴定至终点。平行测定三次,消耗标准液体积如下:
),滴定至终点。平行测定三次,消耗标准液体积如下:
(5)滴定终点的现象为___________ ,产品的纯度是___________  (保留4位有效数字)。
(保留4位有效数字)。
 和
和 制备富马酸亚铁,并对其纯度进行测定,过程如下:
制备富马酸亚铁,并对其纯度进行测定,过程如下:Ⅰ.制备富马酸亚铁
①将少量富马酸固体置于烧杯中,加入
 热水搅拌使之溶解;
热水搅拌使之溶解;②向烧杯中加入
 一定浓度的
一定浓度的 溶液,控制
溶液,控制 为
为 ,并将其转移到仪器
,并将其转移到仪器 中;
中;③通
 并加热一段时间后,通过仪器
并加热一段时间后,通过仪器 缓慢加入
缓慢加入 新配置的
新配置的 溶液,继续加热约1小时后,出现大量棕红色沉淀。
溶液,继续加热约1小时后,出现大量棕红色沉淀。④将反应混合液冷却后,减压过滤,洗涤,干燥,得粗产品。

(1)仪器
 的名称是
的名称是 适宜的规格是
适宜的规格是A.
 B.
B. C.
C.
(2)通
 的目的是
的目的是(3)合成富马酸亚铁反应的化学方程式为
(4)采用减压过滤的优点是
Ⅱ.产品纯度测定
取
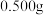 样品置于
样品置于 锥形瓶中,加入
锥形瓶中,加入 稀硫酸,加热使之溶解,冷却后再加入
稀硫酸,加热使之溶解,冷却后再加入 新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇
新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用 硫酸铈铵
硫酸铈铵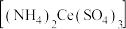 标准液滴定(还原产物为
标准液滴定(还原产物为 ),滴定至终点。平行测定三次,消耗标准液体积如下:
),滴定至终点。平行测定三次,消耗标准液体积如下:| 第一次 | 第二次 | 第三次 |
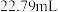 | 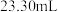 | 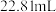 |
(5)滴定终点的现象为
 (保留4位有效数字)。
(保留4位有效数字)。
您最近一年使用:0次



