如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)。
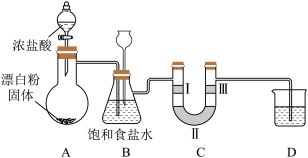
已知:装置A是氯气的发生装置,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O。据此回答下列问题:
(1)装置B中饱和食盐水的作用是________ ;长颈漏斗的作用是__________ 。
(2)装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是: 湿润的有色布条、 无水氯化钙、干燥的有色布条,请你推测Ⅰ、Ⅲ处的现象依次为:______ ,_____ 。
(3)装置D的作用是___________ ,则烧杯中的溶液是______ ,写出所发生反应的化学方程式: ________ 。

已知:装置A是氯气的发生装置,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O。据此回答下列问题:
(1)装置B中饱和食盐水的作用是
(2)装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是: 湿润的有色布条、 无水氯化钙、干燥的有色布条,请你推测Ⅰ、Ⅲ处的现象依次为:
(3)装置D的作用是
更新时间:2019-12-01 10:15:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中____ 是氧化剂,该反应中氧化产物与还原产物的物质的量之比为____ 。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是:______________________ 。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液____ mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式______________ 。
(5)现需490 mL 2.0 mol·L-1 NaOH溶液:
①所需称量的氢氧化钠固体的质量是____ 。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、______ 。
③在配制溶液的过程中,下列操作可能造成结果偏高的是____ 。
A.定容时俯视
B.容量瓶不干燥,含有少量蒸馏水
C.溶解所用烧杯未洗涤
D.NaOH溶解后,未冷却即进行实验
(1)上述反应中
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是:
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式
(5)现需490 mL 2.0 mol·L-1 NaOH溶液:
①所需称量的氢氧化钠固体的质量是
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、
③在配制溶液的过程中,下列操作可能造成结果偏高的是
A.定容时俯视
B.容量瓶不干燥,含有少量蒸馏水
C.溶解所用烧杯未洗涤
D.NaOH溶解后,未冷却即进行实验
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】固体粉末 中含有
中含有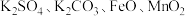 等物质,现取
等物质,现取 进行连续实验,实验过程及产物如图:
进行连续实验,实验过程及产物如图:
(1)①气体C的主要成分是___________ (填“ ”或“
”或“ ”)。
”)。
②溶液B中一定存在的金属阳离子是 、
、___________ (填“ ”或“
”或“ ”)。
”)。
③实验室收集 时用排
时用排___________ (填“饱和食盐水”或“饱和碳酸氢钠溶液”)法。
(2)回收利用 是环境科学的研究热点。工业上常在高温、高压、催化剂条件下利用天然气与二氧化碳反应制备合成气
是环境科学的研究热点。工业上常在高温、高压、催化剂条件下利用天然气与二氧化碳反应制备合成气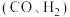 ,其原理是
,其原理是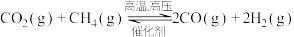 。
。
①恒温条件下,分别向甲、乙两个恒容容器中各加入 与
与 的混合气体,开始时容器压强:甲
的混合气体,开始时容器压强:甲 乙。则反应速率关系是容器甲
乙。则反应速率关系是容器甲___________ (填“ ”或“
”或“ ”)容器乙。
”)容器乙。
②上述反应达到最大限度时,则___________ (填字母)。
A.正、逆反应速率相等 B. 的转化率为
的转化率为 C.反应停止
C.反应停止
 中含有
中含有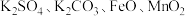 等物质,现取
等物质,现取 进行连续实验,实验过程及产物如图:
进行连续实验,实验过程及产物如图: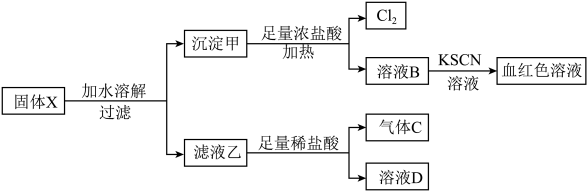
(1)①气体C的主要成分是
 ”或“
”或“ ”)。
”)。②溶液B中一定存在的金属阳离子是
 、
、 ”或“
”或“ ”)。
”)。③实验室收集
 时用排
时用排(2)回收利用
 是环境科学的研究热点。工业上常在高温、高压、催化剂条件下利用天然气与二氧化碳反应制备合成气
是环境科学的研究热点。工业上常在高温、高压、催化剂条件下利用天然气与二氧化碳反应制备合成气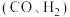 ,其原理是
,其原理是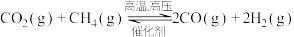 。
。①恒温条件下,分别向甲、乙两个恒容容器中各加入
 与
与 的混合气体,开始时容器压强:甲
的混合气体,开始时容器压强:甲 乙。则反应速率关系是容器甲
乙。则反应速率关系是容器甲 ”或“
”或“ ”)容器乙。
”)容器乙。②上述反应达到最大限度时,则
A.正、逆反应速率相等 B.
 的转化率为
的转化率为 C.反应停止
C.反应停止
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】含氯物质在生产、生活中有重要作用。舍勒在研究软锰矿(主要成分是MnO2,其摩尔质量为87 g/mol)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。
(1)写出浓盐酸与MnO2反应生成黄绿色气体的化学方程式为_________ ,用8.7 gMnO2与足量浓盐酸充分反应,生成Cl2的体积(标准状况下)为_________ L。
(2)实验室制取并收集干燥、纯净的该气体时,所需装置的接口连接顺序为:e接_________ (按气流方向,用小写字母表示)。所用仪器如下图所示:

(3)实验室中也可以用高锰酸钾与浓盐酸在常温下反应制取氯气。从下列仪器中选择制取氯气的装置是_________ (填字母),仪器P的名称为_________ 。
A.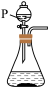 B.
B.  C.
C.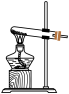
(4)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
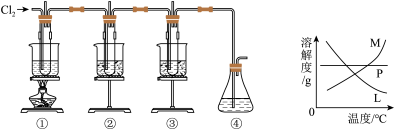
图中:①的试管里盛有15 mL 30%KOH溶液,置于热水浴中;
②的试管里盛有15 mL 8%NaOH溶液,置于冰水浴中;
③的试管里加有紫色石蕊试液;
④为尾气吸收装置。
写出②中制取次氯酸钠的离子方程式_________ 。为什么②装置要放在冰水浴中制取次氯酸钠_________ 。反应完毕经冷却后,①的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是_________ (填写编号字母)。试管③紫色石蕊试液的颜色怎样变化?_________ 。
(1)写出浓盐酸与MnO2反应生成黄绿色气体的化学方程式为
(2)实验室制取并收集干燥、纯净的该气体时,所需装置的接口连接顺序为:e接

(3)实验室中也可以用高锰酸钾与浓盐酸在常温下反应制取氯气。从下列仪器中选择制取氯气的装置是
A.
 B.
B.  C.
C.
(4)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①的试管里盛有15 mL 30%KOH溶液,置于热水浴中;
②的试管里盛有15 mL 8%NaOH溶液,置于冰水浴中;
③的试管里加有紫色石蕊试液;
④为尾气吸收装置。
写出②中制取次氯酸钠的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.高锰酸钾生产过程中会产生较多的废锰渣,工业上将废锰渣(含MnO2及少量KOH、MgO、Fe2O3)再利用,以它为原料来制备MnSO4·H2O。请回答下列问题:
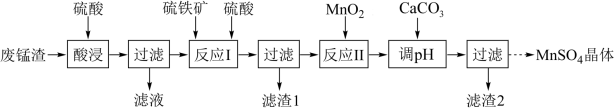
已知:反应Ⅰ的离子方程式为:MnO2 + FeS2 + 4H+ = 2S + Mn2+ + Fe2+ + 2H2O
(1)为提高酸浸过程中浸出率,实验中可采取的措施有___________ 、___________ (任写两种)。
(2)已知:室温下Ksp[Fe(OH)2]=4.9×10-17,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2×10-13,反应Ⅱ后溶液中c(Mn2+)=0.2mol·L-1。
①反应Ⅱ中MnO2的作用是___________ 。
②欲使溶液中c(Fe3+)<10-5mol·L-1,“调pH”过程需控制溶液pH的范围是___________ 。
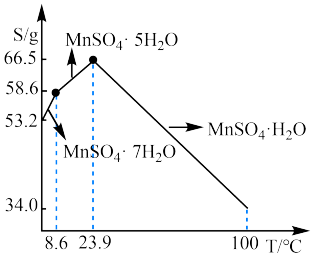
(3)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。从滤液制取较多MnSO4·H2O的操作是:控制温度在80~90℃之间,然后___________ 、___________ ,使固体MnSO4·H2O与溶液分离;获得的MnSO4·H2O晶体常用酒精洗涤,优点是___________ 。
(4)测定产品纯度。
①取制得的MnSO4晶体0.3020g,溶于适量水中,加硫酸酸化;
②用过量NaBiO3(难溶于水)将Mn2+完全氧化为MnO ,过滤、洗涤;
,过滤、洗涤;
③将几次洗涤的滤液与过滤所得的滤液合并,向其中加入Na2C2O4固体1.072g,充分反应;
④再用0.0320mol·L-1 KMnO4溶液滴定步骤③反应后的溶液,用去40.00mL。
已知:C2O + MnO
+ MnO →CO2 + Mn2+(未配平)。
→CO2 + Mn2+(未配平)。
a.用KMnO4溶液滴定时,滴定终点的现象为___________ 。
b.计算产品中MnSO4的质量分数___________ 。
Ⅱ.某实验小组为检验MnSO4受热分解是否生成SO2或SO3,设计探究实验装置如图所示:
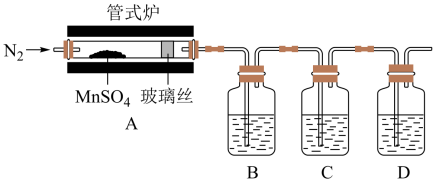
(5)装置B、C、D中的溶液依次为___________ (填字母)。
a.Ba(NO3)2 b.BaCl2 c.品红 d.浓硫酸 e.Ca(OH)2 f.NaOH
(6)实验结束时,为防止倒吸,正确的操作方法是___________ 。

已知:反应Ⅰ的离子方程式为:MnO2 + FeS2 + 4H+ = 2S + Mn2+ + Fe2+ + 2H2O
(1)为提高酸浸过程中浸出率,实验中可采取的措施有
(2)已知:室温下Ksp[Fe(OH)2]=4.9×10-17,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2×10-13,反应Ⅱ后溶液中c(Mn2+)=0.2mol·L-1。
①反应Ⅱ中MnO2的作用是
②欲使溶液中c(Fe3+)<10-5mol·L-1,“调pH”过程需控制溶液pH的范围是
(3)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。从滤液制取较多MnSO4·H2O的操作是:控制温度在80~90℃之间,然后

(4)测定产品纯度。
①取制得的MnSO4晶体0.3020g,溶于适量水中,加硫酸酸化;
②用过量NaBiO3(难溶于水)将Mn2+完全氧化为MnO
 ,过滤、洗涤;
,过滤、洗涤;③将几次洗涤的滤液与过滤所得的滤液合并,向其中加入Na2C2O4固体1.072g,充分反应;
④再用0.0320mol·L-1 KMnO4溶液滴定步骤③反应后的溶液,用去40.00mL。
已知:C2O
 + MnO
+ MnO →CO2 + Mn2+(未配平)。
→CO2 + Mn2+(未配平)。a.用KMnO4溶液滴定时,滴定终点的现象为
b.计算产品中MnSO4的质量分数
Ⅱ.某实验小组为检验MnSO4受热分解是否生成SO2或SO3,设计探究实验装置如图所示:

(5)装置B、C、D中的溶液依次为
a.Ba(NO3)2 b.BaCl2 c.品红 d.浓硫酸 e.Ca(OH)2 f.NaOH
(6)实验结束时,为防止倒吸,正确的操作方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】磷化铝(AlP)通常可作为一种广谱性熏蒸杀虫剂,吸水后会立即产生高毒性PH3气体(沸点-89.7℃,还原性强)。某化学兴趣小组的同学用下述方法测定粮食中残留磷化物的含量。
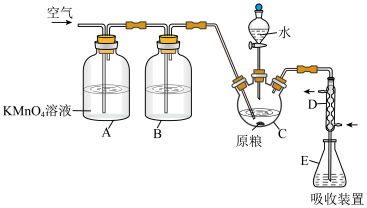
在C中加入100g原粮,E中加入20.00mL 1.50×l0-3mol/L KMnO4溶液(H2SO4酸化),往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中过量的KMnO4溶液。回答下列问题:
(1)仪器D的名称是____ 。
(2)AlP与水反应的化学方程式为_____________ 。
(3)装置A中盛装KMnO4溶液的作用是除去空气中的还原性气体,装置B中盛有焦性没食子酸(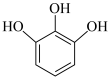 )的碱性溶液,其作用是
)的碱性溶液,其作用是______ 。
(4)通入空气的作用是___________ 。
(5)装置E中PH3被氧化成磷酸,则装置E中发生反应的氧化剂和还原剂物质的量之比为____ 。
(6)收集装置E中的吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,用4.0×10-4mol/L的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液15.00mL,Na2SO3与KMnO4溶液反应的离子方程式为______ ,则该原粮中磷化物(以PH3计)的含量为_____ mg·kg-1。

在C中加入100g原粮,E中加入20.00mL 1.50×l0-3mol/L KMnO4溶液(H2SO4酸化),往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中过量的KMnO4溶液。回答下列问题:
(1)仪器D的名称是
(2)AlP与水反应的化学方程式为
(3)装置A中盛装KMnO4溶液的作用是除去空气中的还原性气体,装置B中盛有焦性没食子酸(
 )的碱性溶液,其作用是
)的碱性溶液,其作用是(4)通入空气的作用是
(5)装置E中PH3被氧化成磷酸,则装置E中发生反应的氧化剂和还原剂物质的量之比为
(6)收集装置E中的吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,用4.0×10-4mol/L的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液15.00mL,Na2SO3与KMnO4溶液反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(1)下列有关NH3的说法中,不正确的是__________ (双选)。
A.工业合成NH3需要在高温高压下进行 B. NH3可用来生产碳铵和尿素等化肥
C. NH3可用浓硫酸或无水氯化钙干燥 D. NH3受热易分解,须置于冷暗处保存
(2)NH3易于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为________________ mol.L-1。
(3)氨气在氧化炉中所发生反应的化学方程式为_____________________________________________ 。
(4)“吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为:Na2CO3+2NO2=NaNO3+________ +CO2 (请填写完成化学方程式)。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为__________ 。

(1)下列有关NH3的说法中,不正确的是
A.工业合成NH3需要在高温高压下进行 B. NH3可用来生产碳铵和尿素等化肥
C. NH3可用浓硫酸或无水氯化钙干燥 D. NH3受热易分解,须置于冷暗处保存
(2)NH3易于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
(3)氨气在氧化炉中所发生反应的化学方程式为
(4)“吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为:Na2CO3+2NO2=NaNO3+
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近一年使用:0次



