某小组拟制备三氯乙醛,装置如图所示(夹持装置略去)。

已知:制备反应原理为CH3CH2OH+4Cl2→CCl3CHO+5HCl,可能发生的副反应为CH3CH2OH+HCl→CH3CH2Cl+H2O 。常温下,高锰酸钾和浓盐酸可以制备氯气。
(1)写出A中发生反应的离子方程式:______________ 。
(2)实验发现,通入D中的氯气速率过快,合理的解决方案是______________ 。
(3)实验完毕后。从D中分离产品的操作是______________ 。
(4)进入D装置中的氯气要干燥、纯净。B中试剂可能是________ (填序号);如果拆去B装置,后果是_____ 。
a、NaOH溶液 b、饱和食盐水 c、稀盐酸 d、稀硫酸

已知:制备反应原理为CH3CH2OH+4Cl2→CCl3CHO+5HCl,可能发生的副反应为CH3CH2OH+HCl→CH3CH2Cl+H2O 。常温下,高锰酸钾和浓盐酸可以制备氯气。
(1)写出A中发生反应的离子方程式:
(2)实验发现,通入D中的氯气速率过快,合理的解决方案是
(3)实验完毕后。从D中分离产品的操作是
(4)进入D装置中的氯气要干燥、纯净。B中试剂可能是
a、NaOH溶液 b、饱和食盐水 c、稀盐酸 d、稀硫酸
更新时间:2019-12-06 18:40:39
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯气是一种重要的化工原料,在生活和生产中的应用十分广泛。请回答:
(1)请写出工业制备氯气的离子方程式_______ 。
(2)实验室常用MnO2与浓盐酸反应制备Cl2,装置如图所示:

仪器a的名称为_______ 。制备实验开始时,先检查装置气密性,接下来的操作依次是:_______ (填序号)。
①往烧瓶中加入MnO2粉末 ②加热 ③往烧瓶中加入浓盐酸
(3)为证明Cl2与H2O反应为可逆反应,将生成的气体通入图所示装置:

①装置A中应加入的试剂是_______ 。
②证明可逆反应,需验证在B中反应物和生成物同时存在,证明氯水中有Cl2存在的现象是_______ ,仅使用一种试剂证明氯水中HCl和HClO均存在,合适的试剂是_______ 。
a.AgNO3溶液 b.石蕊试液 c.NaOH溶液 d.品红溶液
③装置C中NaOH溶液的作用是_______ 。
(1)请写出工业制备氯气的离子方程式
(2)实验室常用MnO2与浓盐酸反应制备Cl2,装置如图所示:

仪器a的名称为
①往烧瓶中加入MnO2粉末 ②加热 ③往烧瓶中加入浓盐酸
(3)为证明Cl2与H2O反应为可逆反应,将生成的气体通入图所示装置:

①装置A中应加入的试剂是
②证明可逆反应,需验证在B中反应物和生成物同时存在,证明氯水中有Cl2存在的现象是
a.AgNO3溶液 b.石蕊试液 c.NaOH溶液 d.品红溶液
③装置C中NaOH溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】人类对氯的认识经历了漫长的过程。回答下列问题:
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是___________ 。
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。___________ ,装置接口的连接顺序是a→______→______→______→______→f。___________
②装置乙中的试剂Y是___________ 。
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”);打开开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”),证明氯气没有漂白性,但氯气与水反应的产物___________ 具有漂白性。
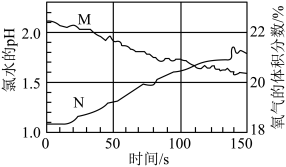
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是___________ (填“M”或“N”),据此分析,此时广口瓶中发生反应的化学方程式是___________ 。___________ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。

②装置乙中的试剂Y是
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D (放置有铁粉 )。请回答:
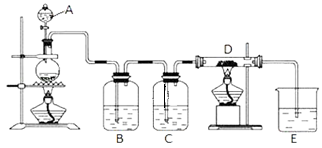
(1)烧瓶中反应的化学方程式是_____ ;
(2)装置B中盛放液体是_____ ,气体通过装置B的目的是_____ ;装置C中盛放的液体是_____ ,气体通过装置C的目的是_____ ;
(3)烧杯E中盛放的液体是_____ ;
(4)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O (g )剧烈反应;为收集D中产物,在D与E之间,除增加收集装置外,还需要增加_____ 装置;
(5)当电子转移的数目为6.02×1023个时生成的氯气的物质的量为_____ mol,生成的氯气需用0.5mol/L的NaOH溶液_____ L完全吸收。

(1)烧瓶中反应的化学方程式是
(2)装置B中盛放液体是
(3)烧杯E中盛放的液体是
(4)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O (g )剧烈反应;为收集D中产物,在D与E之间,除增加收集装置外,还需要增加
(5)当电子转移的数目为6.02×1023个时生成的氯气的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】工业水合肼法制备叠氮化钠的工艺流程如图所示:

一、合成水合肼
已知: (水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。
(水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。 (水合肼)熔点-40℃,沸点118.5℃。
(水合肼)熔点-40℃,沸点118.5℃。
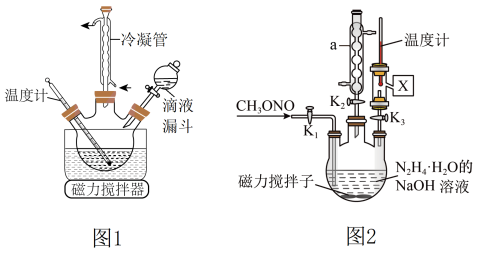
合成 的装置如图1所示。
的装置如图1所示。 碱性溶液与尿素
碱性溶液与尿素 水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
(1)写出 的结构式
的结构式____________ , 的电子式
的电子式____________
(2)①写出制取 的离子方程式
的离子方程式___________________________
②实验中通过滴液漏斗滴加的溶液是_________ 理由是_______________ 图1使用冷凝管的目的是____________________________________
③从反应后的混合溶分离出 ,应该采用的分离方法最合理的是
,应该采用的分离方法最合理的是________ 。
二、合成叠氮化钠(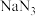 )晶体
)晶体
已知:相关物质的物理性质如下表
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是________________ 。(写出1点即可)
②图中 处连接的最合适装置应为下图中的
处连接的最合适装置应为下图中的__________ 。
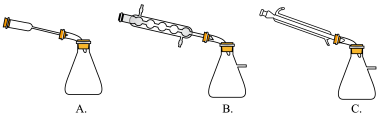
③步骤Ⅱ中制备叠氮化钠的操作是________ (填序号)步骤Ⅲ中溶液 进行蒸馏的合理操作顺序是
进行蒸馏的合理操作顺序是_______ 。(填序号)
①打开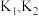 ,关闭
,关闭 ②打开
②打开 ③加热④关闭
③加热④关闭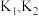
(4)步骤Ⅳ对溶液 加热蒸发至溶液体积的
加热蒸发至溶液体积的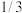 ,
,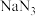 结晶析出。步骤Ⅴ可以用
结晶析出。步骤Ⅴ可以用________ 洗涤晶体。
A.水B.乙醚C.乙醇水溶液D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:
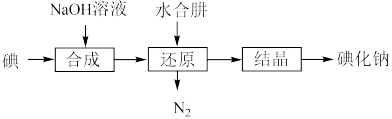
还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是______________________________________ 。


一、合成水合肼
已知:
 (水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。
(水合肼)与水互溶,有毒且不稳定,100℃以上易分解失水,具有强还原性和强碱性。 (水合肼)熔点-40℃,沸点118.5℃。
(水合肼)熔点-40℃,沸点118.5℃。合成
 的装置如图1所示。
的装置如图1所示。 碱性溶液与尿素
碱性溶液与尿素 水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。(1)写出
 的结构式
的结构式 的电子式
的电子式(2)①写出制取
 的离子方程式
的离子方程式②实验中通过滴液漏斗滴加的溶液是
③从反应后的混合溶分离出
 ,应该采用的分离方法最合理的是
,应该采用的分离方法最合理的是二、合成叠氮化钠(
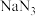 )晶体
)晶体已知:相关物质的物理性质如下表
| 熔点℃ | 沸点℃ | 溶解性 | |
 | -97 | 67.1 | 与水互溶 |
水合肼( ) ) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
亚硝酸甲酯(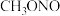 ) ) | -17 | -12 | 溶于乙醇、乙醚 |
| NaN3 | 与水互溶,不溶于乙醚、微溶于乙醇 |
(3)实验室模拟工艺流程步骤Ⅱ的实验装置如图2
①根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是
②图中
 处连接的最合适装置应为下图中的
处连接的最合适装置应为下图中的
③步骤Ⅱ中制备叠氮化钠的操作是
 进行蒸馏的合理操作顺序是
进行蒸馏的合理操作顺序是①打开
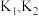 ,关闭
,关闭 ②打开
②打开 ③加热④关闭
③加热④关闭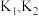
(4)步骤Ⅳ对溶液
 加热蒸发至溶液体积的
加热蒸发至溶液体积的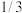 ,
,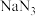 结晶析出。步骤Ⅴ可以用
结晶析出。步骤Ⅴ可以用A.水B.乙醚C.乙醇水溶液D.乙醇
(5)工业上还可以用水合肼还原法制取碘化钠,工艺流程如图:

还原过程中可用硫化钠或铁屑等物质替代水合肼,但水合肼还原法制得的产品纯度更高,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯气化学性质活泼,在加热条件下能与大多数金属和非金属反应,某同学设计实验利用氯气和硼反应制取 (熔点
(熔点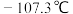 ,沸点
,沸点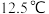 ,遇水剧烈反应,其中一种产物为
,遇水剧烈反应,其中一种产物为 )。请回答下列问题:
)。请回答下列问题:
(1)该同学利用如下装置(可重复使用)进行实验装置连接的合理顺序为A→_______ 
_______ 
_______ 
_______ →D→F。
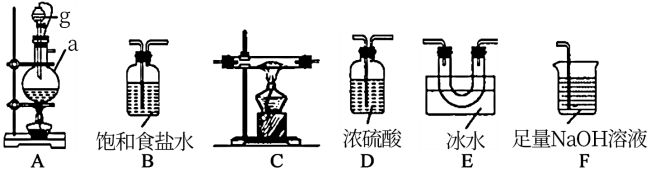
(2)A中发生反应的离子方程式为_______ 。仪器a的名称为_______ 。
(3)图中g管的作用是_______ 。
(4)在装置F前连接装置D的作用是_______ 。
(5)写出BCl3与水发生反应的化学方程式_______ 。
(6)装置E中冰水的作用是_______ 。
(7)实验结束后,经测定装置F中生成的 与
与 的物质的量之比为
的物质的量之比为 ,则该反应氧化产物与还原产物的物质的量之比为
,则该反应氧化产物与还原产物的物质的量之比为_______ 。
 (熔点
(熔点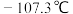 ,沸点
,沸点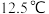 ,遇水剧烈反应,其中一种产物为
,遇水剧烈反应,其中一种产物为 )。请回答下列问题:
)。请回答下列问题:(1)该同学利用如下装置(可重复使用)进行实验装置连接的合理顺序为A→




(2)A中发生反应的离子方程式为
(3)图中g管的作用是
(4)在装置F前连接装置D的作用是
(5)写出BCl3与水发生反应的化学方程式
(6)装置E中冰水的作用是
(7)实验结束后,经测定装置F中生成的
 与
与 的物质的量之比为
的物质的量之比为 ,则该反应氧化产物与还原产物的物质的量之比为
,则该反应氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】工业生产硫酸的黄铁矿烧渣(主要成分为Fe2O3及少量的FeS、SiO2、Cu、Au、Ag等)是工业三废之一,其综合利用是一条变废为宝的重要途径。
I.以黄铁矿烧渣为原料制备颜料铁红(Fe2O3)和回收(NH4)2SO4的生产工艺流程如下图:

请回答下列问题:
(1)能提高“废渣溶解”速率的措施有______ (写出一条即可),“氧化”的目的是______________ 。 (2)(NH4)2Fe6(SO4)4(OH)12中Fe的化合价是__________________ 。
(3)该工艺流程图中,第二次加入氨水后,反应的离子方程式为________________________ 。
II.下图是以黄铁矿烧渣为原料制备颜料铁红的另外一种生产工艺流程:

(4)在滤液I中加入廉价的熟石灰,反应的化学方程式是___________________ 。
(5)“氧化”反应较多,其中FeS 可以看做被水溶液中Cl2氧化,氧化后的溶液中滴加BaCl2有不溶解于盐酸的白色沉淀生成,则水溶液中FeS 与Cl2反应的离子方程式为________________ 。
(6)试剂X 为过量铁粉,其作用是________________________________ 。
I.以黄铁矿烧渣为原料制备颜料铁红(Fe2O3)和回收(NH4)2SO4的生产工艺流程如下图:

请回答下列问题:
(1)能提高“废渣溶解”速率的措施有
(3)该工艺流程图中,第二次加入氨水后,反应的离子方程式为
II.下图是以黄铁矿烧渣为原料制备颜料铁红的另外一种生产工艺流程:

(4)在滤液I中加入廉价的熟石灰,反应的化学方程式是
(5)“氧化”反应较多,其中FeS 可以看做被水溶液中Cl2氧化,氧化后的溶液中滴加BaCl2有不溶解于盐酸的白色沉淀生成,则水溶液中FeS 与Cl2反应的离子方程式为
(6)试剂X 为过量铁粉,其作用是
您最近一年使用:0次



