随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
方法二 CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
在25 ℃、101 kPa下,1g液态甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式:_________________ 。
(2)金属钛冶炼过程中其中一步反应是将原料金红石转化:
TiO2(金红石)+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
已知:C(s)+O2(g)=CO2(g) ΔH=﹣393.5kJ/mol
2CO(g)+O2(g)=2CO2(g) ΔH=﹣566 kJ/mol
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_______________________ 。
(3)臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应如6Ag(s)+O3(g)=3Ag2O(s) ΔH=﹣235.8 kJ/mol,
已知:2Ag2O(s)=4Ag(s)+O2(g) ΔH= +62.2 kJ/mol,则O3转化为O2的热化学方程式为________________ 。
(1)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)方法二 CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)在25 ℃、101 kPa下,1g液态甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式:
(2)金属钛冶炼过程中其中一步反应是将原料金红石转化:
TiO2(金红石)+2C+2Cl2
 TiCl4+2CO
TiCl4+2CO已知:C(s)+O2(g)=CO2(g) ΔH=﹣393.5kJ/mol
2CO(g)+O2(g)=2CO2(g) ΔH=﹣566 kJ/mol
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
(3)臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应如6Ag(s)+O3(g)=3Ag2O(s) ΔH=﹣235.8 kJ/mol,
已知:2Ag2O(s)=4Ag(s)+O2(g) ΔH= +62.2 kJ/mol,则O3转化为O2的热化学方程式为
18-19高一下·河南鹤壁·阶段练习 查看更多[4]
贵州省贵阳市清镇养正学校2019-2020学年高二上学期期中考试化学试题2020年春季人教版高中化学选修4第一章《化学反应与能量》测试卷(已下线)2019年12月18日 《每日一题》化学人教版(选修4)——盖斯定律河南省鹤壁市高级中学2018-2019学年高一下学期第一次段考化学试题
更新时间:2019-12-09 19:41:12
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。
反应Ⅰ:CO(g)+2H2(g) CH3OH(g),△H1
CH3OH(g),△H1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+ H2O(g),△H2
下表所列数据是反应I在不同温度下的化学平衡常数(K):
(1)在一定条件下将2 molCO和6molH2充入2L的密闭容器中发生反应I,5min后测得c(CO)=0.4 mol/L,计算此段时间的反应速 率(用H2表示)
率(用H2表示)___________ mol/(L·min)。
(2)由表中数据判断△H1_____ 0(填“>”、“<”或“=”)反应,CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3=____ (用△H1和△H2表示)。
(3)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是_________ (选字母)。
a.充入CO,使体系总压强增大
b.将CH3OH(g)从体系中分离
e.充入He,使体系总压强增大
d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:K=_________ ;保持恒温恒容的条件下将反应Ⅱ的平衡体系各物质浓度均增加一倍,则化学平衡_________ (填“正向”、“逆向”或“不”)移动,平衡常数K____ (填“变大”、“变小”或“不变”)。
反应Ⅰ:CO(g)+2H2(g)
 CH3OH(g),△H1
CH3OH(g),△H1反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+ H2O(g),△H2
下表所列数据是反应I在不同温度下的化学平衡常数(K):
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.0 | 0.27 | 0.012 |
 率(用H2表示)
率(用H2表示)(2)由表中数据判断△H1
(3)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是
a.充入CO,使体系总压强增大
b.将CH3OH(g)从体系中分离
e.充入He,使体系总压强增大
d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:K=
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题。
(1)25℃、1.01><105Pa时,实验测得108g液态水完全分解成H2和O2,需要吸收1716kJ 的热量,则表示H2的燃烧热的热化学方程式为_____ 。
(2)从化学键的角度分析,化学反应的过程就是反应物化学键破坏和生成物化学键形成的过程,已知几种化学键的键能如下:
已知:N2(g)+3H2(g)=2NH3(g) △H=-93 kJ mol-1。试根据表中所列键能数据计算a 的数值_____ 。
(3)已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ mol-1①
2H2(g)+ O2(g)=2H2O(l)△H2=-571.6kJ mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ mol-1③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g) △H=_____ 。
(1)25℃、1.01><105Pa时,实验测得108g液态水完全分解成H2和O2,需要吸收1716kJ 的热量,则表示H2的燃烧热的热化学方程式为
(2)从化学键的角度分析,化学反应的过程就是反应物化学键破坏和生成物化学键形成的过程,已知几种化学键的键能如下:
| 化学键 | H—H | N—H | N≡N |
| 键能kJ/mol | 436 | 391 | a |
已知:N2(g)+3H2(g)=2NH3(g) △H=-93 kJ mol-1。试根据表中所列键能数据计算a 的数值
(3)已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ mol-1①
2H2(g)+ O2(g)=2H2O(l)△H2=-571.6kJ mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ mol-1③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g) △H=
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)已知:①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+ O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
由上述方程式可知:CH3OH的燃烧热________ (填“大于”“等于”或“小于”)192.9 kJ/mol。
已知水的气化热为44 kJ/mol。则表示氢气燃烧热的热化学方程式为__________ 。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)===H2O(g) ΔH=+44.0 kJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式是_____________________________ 。
(3)已知:①Fe(s)+ O2(g)===FeO(s) ΔH1=-272.0 kJ/mol
O2(g)===FeO(s) ΔH1=-272.0 kJ/mol
②2Al(s)+ O2(g)===Al2O3(s) ΔH2=-1675.7 kJ/mol
O2(g)===Al2O3(s) ΔH2=-1675.7 kJ/mol
Al和FeO发生铝热反应的热化学方程式是_____________________________________ 。该反应的自发性趋势很大,原因是________________________________________ 。
②CH3OH(g)+
 O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol由上述方程式可知:CH3OH的燃烧热
已知水的气化热为44 kJ/mol。则表示氢气燃烧热的热化学方程式为
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)===H2O(g) ΔH=+44.0 kJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式是
(3)已知:①Fe(s)+
 O2(g)===FeO(s) ΔH1=-272.0 kJ/mol
O2(g)===FeO(s) ΔH1=-272.0 kJ/mol②2Al(s)+
 O2(g)===Al2O3(s) ΔH2=-1675.7 kJ/mol
O2(g)===Al2O3(s) ΔH2=-1675.7 kJ/molAl和FeO发生铝热反应的热化学方程式是
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知下列反应的反应热:
(1)CH3COOH(l)+2O2(g) =2CO2(g) + 2H2O(l)△H = - 870.3 kJ/mol
(2)C(s)+O2(g)=CO2(g)△H = - 393.5 kJ/mol
(3)2 H2(g)+O2(g)=2H2O(l)△H = - 571.6 kJ/mol,
试计算反应2C(s) + 2 H2(g) + O2(g) = CH3COOH(l)的反应热△H =___ ,2克H2完全燃烧生成液态水时放出的热量为___ kJ,H2的燃烧热为△H = _____ 。
(1)CH3COOH(l)+2O2(g) =2CO2(g) + 2H2O(l)△H = - 870.3 kJ/mol
(2)C(s)+O2(g)=CO2(g)△H = - 393.5 kJ/mol
(3)2 H2(g)+O2(g)=2H2O(l)△H = - 571.6 kJ/mol,
试计算反应2C(s) + 2 H2(g) + O2(g) = CH3COOH(l)的反应热△H =
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】已知:①2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
③CH4(g)+2O2(g)=2H2O(l)+CO2(g) ΔH=-890kJ·mol-1
(1)已知H—H键的键能为436kJ·mol-1,O=O键的键能为496kJ·mol-1,H—O键的键能为463kJ·mol-1,根据上述数据通过键能可直接计算出反应___ (填反应序号)的焓变,由反应①②可得出反应比H2O(l)=H2O(g)的焓变ΔH=___ 。
(2)根据题干可计算出CO2(g)+4H2(g)=CH4(g)+2H2O(g)的焓变ΔH=___ 。
(3)在①②③三个热化学方程式中,可表示燃烧热的热化学方程式的是___ (填序号)。标准状况下,取甲烷和氢气的混合气体11.2L,完全燃烧后恢复到常温,放出的热量为263.8kJ,则混合气体中甲烷和氢气的体积比为___ 。
②2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
③CH4(g)+2O2(g)=2H2O(l)+CO2(g) ΔH=-890kJ·mol-1
(1)已知H—H键的键能为436kJ·mol-1,O=O键的键能为496kJ·mol-1,H—O键的键能为463kJ·mol-1,根据上述数据通过键能可直接计算出反应
(2)根据题干可计算出CO2(g)+4H2(g)=CH4(g)+2H2O(g)的焓变ΔH=
(3)在①②③三个热化学方程式中,可表示燃烧热的热化学方程式的是
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】(12分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下

(1)合成塔中反应的化学方程式为_____________ ;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了________________ 。
(2)从合成塔分离出甲醇的原理与下列______ 操作的原理比较相符(填字母)
工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施。“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括__________ .
(3)在体积为2L的合成塔中,充人2 mol CO2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
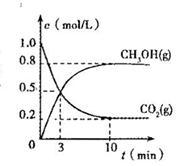
从反应开始到平衡,V(H2) =______________ ;能使平衡体系中nCH3OH)/n(CO2)增大的措施有____________ 。
A、加入催化剂
B、充入He(g),使体系压强增大
C、将H2O(g)从体系中分离
D、降低温度
(4) 如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
已知CH4(g) + 2O2(g)=CO2(g)+ 2H2O(l) ΔH1=― 890.3 kJ/mol
H2(g) + 1/2O2(g)=H2O(l) ΔH2=-285.8 kJ/mol
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式________________ 。

(1)合成塔中反应的化学方程式为
(2)从合成塔分离出甲醇的原理与下列
| A.过滤 | B.分液 | C.蒸馏 | D.结晶 |
(3)在体积为2L的合成塔中,充人2 mol CO2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

从反应开始到平衡,V(H2) =
A、加入催化剂
B、充入He(g),使体系压强增大
C、将H2O(g)从体系中分离
D、降低温度
(4) 如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
已知CH4(g) + 2O2(g)=CO2(g)+ 2H2O(l) ΔH1=― 890.3 kJ/mol
H2(g) + 1/2O2(g)=H2O(l) ΔH2=-285.8 kJ/mol
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式
您最近半年使用:0次



