下列热化学方程式(△H的绝对值均正确)书写正确的是
A.2CO(g)+O2(g)===2CO2(g);  H=-566 kJ·mol-1(燃烧热) H=-566 kJ·mol-1(燃烧热) |
B.NaOH(aq)+HCl(aq) ===NaCl(aq)+H2O(l);  H=+57.3 kJ·mol-1 (中和热) H=+57.3 kJ·mol-1 (中和热) |
C.C2H5OH(l)+3O2(g) ===2CO2(g)+3H2O(l); H=-1366.8 kJ·mol-1 (燃烧热) H=-1366.8 kJ·mol-1 (燃烧热) |
D.Ba(OH)2(aq)+2HCl(aq)===BaCl2(aq)+2H2O(l); H=-114.6 kJ·mol-1 (中和热) H=-114.6 kJ·mol-1 (中和热) |
更新时间:2019-12-12 17:34:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下图是反应CO(g)+2H2(g)  CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是
CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是

 CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是
CH3OH(g)进行过程中的能量变化曲线。曲线a 表示不使用催化剂时反应的能量变化,曲线 b 表示使用催化剂后的能量变化。下列相关说法正确的是
| A.升高温度,能提高 CO 的转化率 |
| B.使用催化剂后反应热减小,能耗降低 |
| C.生成物的总键能小于反应物的总键能 |
D.热化学方程式为CO(g)+2H2(g)  CH3OH(g) △H =—91 kJ/mol CH3OH(g) △H =—91 kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的值。已知反应;
①

②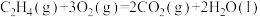

其他数据如下表:
下列说法正确的是
①


②
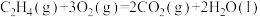

其他数据如下表:
| 化学键 | C=O | O=O | C-H | O-H | C=C |
键能/( ) ) | 798 | x | 413 | 463 | 610 |
A.a<b,且 的燃烧热为 的燃烧热为 |
B.上表中 |
C.  |
| D.当有4NA个C-H键断裂时,该反应放出热量一定为a kJ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】在生产、生活、科技中,氢能已获得越来越多的关注,是非常重要的能源。已知:
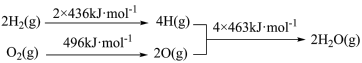
下列推断正确的是
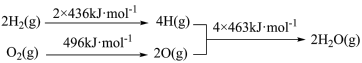
下列推断正确的是
| A.H2O(l)吸收能量后,分子中氢氧键断裂而生成H2O(g) |
B.2H2(g)+O2(g)=2H2O(g)  =-484 kJ =-484 kJ |
| C.若2H2(g)+O2(g)=2H2O(g)+Q1;2H2(g)+O2(l)=2H2O(g)+Q2;则Q1>Q2 |
| D.将2 mol H2O(g)分解成H2(g)和O2(g),吸收4×463 kJ的热量 |
您最近半年使用:0次
【推荐1】下列说法正确的是
| A.C与CO2的反应、盐酸与NaHCO3的反应、Ba(OH)2与NH4Cl的反应都是吸热反应 |
B.C的燃烧热的热化学方程式可表示为C(s)+ O2(g)= CO(g) △H=-110.5kJ·mol-1 O2(g)= CO(g) △H=-110.5kJ·mol-1 |
C.已知:Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) △H = -akJ·mol-1,则中和热为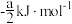 |
| D.利用盖斯定律可以求出所有反应的反应热 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
A.手性分子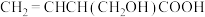 与足量的 与足量的 反应后分子有两个手性碳原子 反应后分子有两个手性碳原子 |
B.500℃、30MPa下,将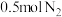 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式为: ,放热19.3kJ,其热化学方程式为:  |
C.在25℃和101kPa时:① 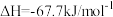 ② 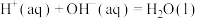 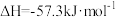 ,则氢氟酸的电离方程式及热效应可表示为: ,则氢氟酸的电离方程式及热效应可表示为: 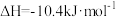 |
D.已知氢气在氯气中燃烧的热化学方程式:  ,拆开1molH-H键和1molCl-Cl键所需能量大于拆开2molH-Cl键所需能量 ,拆开1molH-H键和1molCl-Cl键所需能量大于拆开2molH-Cl键所需能量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的 不同 不同 |
| B.CH3OH(l)的燃烧热为1452 kJ·mol-1 |
C. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)= Ba(OH)2(aq)= BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| D.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列涉及的方程式表示正确的是
A.亚硫酸氢钠溶液呈酸性的主要原因: |
B.铅酸电池的正极在充电时的电极反应式: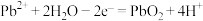 |
C. 的燃烧热为 的燃烧热为 ,则 ,则 燃烧的热化学方程式为: 燃烧的热化学方程式为: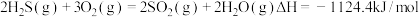 |
D. 溶液与足量的 溶液与足量的 溶液反应: 溶液反应: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2008年9月我国“神七”发射升空,中国航天员实现首次太空行走。运载火箭的原料用肼( )作为发动机的燃料,
)作为发动机的燃料, 为氧化剂,反应生成氮气和水蒸气。已知:
为氧化剂,反应生成氮气和水蒸气。已知:
 kJ/mol,
kJ/mol,
 kJ/mol,下列判断正确的是
kJ/mol,下列判断正确的是
 )作为发动机的燃料,
)作为发动机的燃料, 为氧化剂,反应生成氮气和水蒸气。已知:
为氧化剂,反应生成氮气和水蒸气。已知:
 kJ/mol,
kJ/mol,
 kJ/mol,下列判断正确的是
kJ/mol,下列判断正确的是| A.所有物质与氧气发生的化学反应都是放热反应 |
B. 的燃烧热为534 kJ/mol 的燃烧热为534 kJ/mol |
C.肼与 反应的热化学方程 反应的热化学方程  kJ/mol kJ/mol |
| D.3.2 g肼完全反应转移的电子数为0.6 mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列依据热化学方程式得出的结论正确的是( )
A.已知 2SO2 + O2 2SO3 为放热反应,则 SO2 的能量一定高于 SO3 的能量 2SO3 为放热反应,则 SO2 的能量一定高于 SO3 的能量 |
B.由 C(s) + O2 (g) ═ CO(g)△H=-110.5 kJ•mol﹣1 可知碳的燃烧热为 110.5 kJ•mol﹣1 O2 (g) ═ CO(g)△H=-110.5 kJ•mol﹣1 可知碳的燃烧热为 110.5 kJ•mol﹣1 |
| C.若 C(石墨,s) = C(金刚石,s)△H>0,则石墨比金刚石稳定 |
| D.已知 2C(s) +2O2 (g)═2CO2 (g) △H1,2C(s) + O2 (g) ═ 2CO(g)△H2,则△H1>△H2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知葡萄糖(相对分子质量180)燃烧的热化学方程式为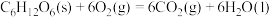 ∆H=-2803kJ∙mol-1。下列说法错误的是
∆H=-2803kJ∙mol-1。下列说法错误的是
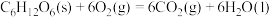 ∆H=-2803kJ∙mol-1。下列说法错误的是
∆H=-2803kJ∙mol-1。下列说法错误的是A.葡萄糖的热值约为 |
| B.若生成物中水为气态,则∆H变大 |
C.该条件下, 的焓变为 的焓变为 |
D.该条件下,完全燃烧30g葡萄糖时消耗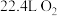 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知反应:①2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol;②稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ/mol。下列结论正确的是
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀硫酸与稀Ba(OH)2溶液反应的中和热为57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】关于热化学方程式,下列说法正确的是
A.2molSO2和1molO2充分反应后放出热量196.6kJ,则2SO2(g) + O2(g) 2SO3(g) △H=-196.6 kJ/mol 2SO3(g) △H=-196.6 kJ/mol |
| B.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,若将含1molCH3COOH的醋酸溶液与含1molNaOH的溶液混合,放出的热量小于57.3kJ |
| C.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D.甲烷的燃烧热为-890.3KJ/mol,则甲烷燃烧的热化学方程式表示为CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H=-890.3kJ/mol |
您最近半年使用:0次



