Ⅰ 从海水得到的粗食盐水中常含
从海水得到的粗食盐水中常含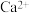 、
、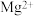 、
、 ,需要分离提纯
,需要分离提纯 现有含少量
现有含少量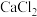 、
、 的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂
的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂 盐酸、
盐酸、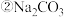 、
、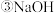 、
、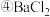 来除去食盐水中
来除去食盐水中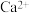 、
、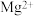 、
、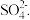 提纯时的操作步骤和加入试剂的情况如图1。
提纯时的操作步骤和加入试剂的情况如图1。
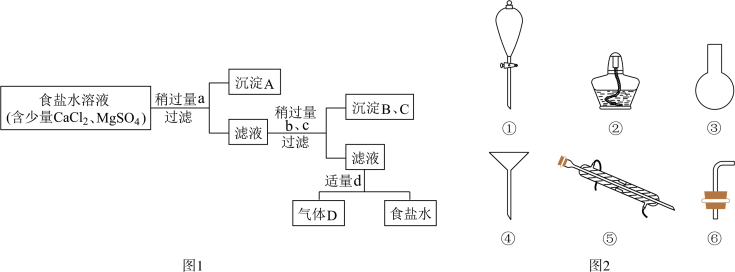
图1中a、b、c、d分别表示上述4种试剂中的一种,试回答:
 沉淀A的名称是
沉淀A的名称是______ .
 试剂d是
试剂d是______ ;判断试剂d适量的方法是______ .
 加入b、c后溶液中发生的化学反应的化学方程式为
加入b、c后溶液中发生的化学反应的化学方程式为______ .
Ⅱ 海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要图2仪器中的
海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要图2仪器中的______  填序号
填序号 ,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做
,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做______ .
 从海水得到的粗食盐水中常含
从海水得到的粗食盐水中常含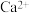 、
、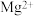 、
、 ,需要分离提纯
,需要分离提纯 现有含少量
现有含少量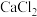 、
、 的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂
的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂 盐酸、
盐酸、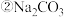 、
、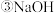 、
、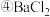 来除去食盐水中
来除去食盐水中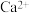 、
、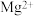 、
、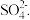 提纯时的操作步骤和加入试剂的情况如图1。
提纯时的操作步骤和加入试剂的情况如图1。
图1中a、b、c、d分别表示上述4种试剂中的一种,试回答:
 沉淀A的名称是
沉淀A的名称是 试剂d是
试剂d是 加入b、c后溶液中发生的化学反应的化学方程式为
加入b、c后溶液中发生的化学反应的化学方程式为Ⅱ
 海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要图2仪器中的
海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要图2仪器中的 填序号
填序号 ,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做
,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做
更新时间:2019-12-16 13:57:29
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】镍(Ni)是一种硬而有延展性并具有铁磁性的金属,其常见硫酸盐(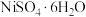 )是一种蓝色晶体,主要用于电镀行业镀镍、制镍催化剂、印染的媒染剂等,工业上用富含(NiS)的废渣(主要有
)是一种蓝色晶体,主要用于电镀行业镀镍、制镍催化剂、印染的媒染剂等,工业上用富含(NiS)的废渣(主要有 、FeO等杂质)制备
、FeO等杂质)制备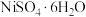 ,其流程如下:
,其流程如下: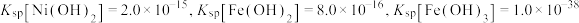 。
。
(1)Ni元素在元素周期表的位置为___________ ,其基态原子的价电子排布式为___________ 。
(2)“预处理”操作可以选择用___________(填标号)来除去含镍废料表面的矿物油污。
(3)“酸浸”过程中,加稀硫酸的同时还应加入少量的稀硝酸,其目的是将NiS氧化为 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(4)“氧化”过程保持滤液温度在45℃左右,原因是___________ ,请写出该过程反应的离子方程式___________ 。
(5)常温下加NaOH溶液调节pH,若溶液中 ,则溶液的pH范围应调节为
,则溶液的pH范围应调节为___________ (通常认为溶液中的离子浓度小于 为沉淀完全)。操作a应为
为沉淀完全)。操作a应为___________ ,过滤。
(6)煅烧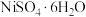 晶体,剩余固体质量与温度变化关系如图所示,该曲线中B段所表示氧化物为
晶体,剩余固体质量与温度变化关系如图所示,该曲线中B段所表示氧化物为___________ 。(填化学式)
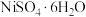 )是一种蓝色晶体,主要用于电镀行业镀镍、制镍催化剂、印染的媒染剂等,工业上用富含(NiS)的废渣(主要有
)是一种蓝色晶体,主要用于电镀行业镀镍、制镍催化剂、印染的媒染剂等,工业上用富含(NiS)的废渣(主要有 、FeO等杂质)制备
、FeO等杂质)制备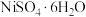 ,其流程如下:
,其流程如下: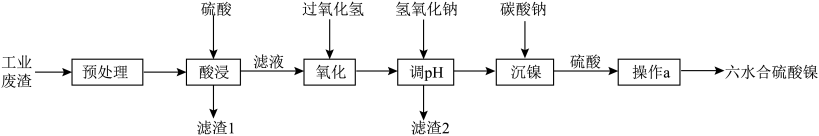
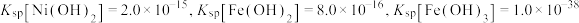 。
。(1)Ni元素在元素周期表的位置为
(2)“预处理”操作可以选择用___________(填标号)来除去含镍废料表面的矿物油污。
| A.纯碱溶液 | B.NaOH溶液 | C.酒精 | D.硫酸溶液 |
(3)“酸浸”过程中,加稀硫酸的同时还应加入少量的稀硝酸,其目的是将NiS氧化为
 ,写出该反应的化学方程式
,写出该反应的化学方程式(4)“氧化”过程保持滤液温度在45℃左右,原因是
(5)常温下加NaOH溶液调节pH,若溶液中
 ,则溶液的pH范围应调节为
,则溶液的pH范围应调节为 为沉淀完全)。操作a应为
为沉淀完全)。操作a应为(6)煅烧
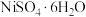 晶体,剩余固体质量与温度变化关系如图所示,该曲线中B段所表示氧化物为
晶体,剩余固体质量与温度变化关系如图所示,该曲线中B段所表示氧化物为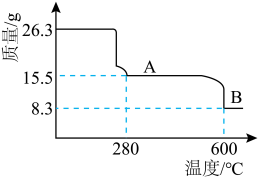
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案:
(1)为了加快粗盐的溶解,可采取的措施有_______ (填一种即可)。
(2)写出步骤ⅳ中发生反应的化学方程式:_______ 。
(3)沉淀B的主要成分为_______ (填化学式);往沉淀B中加入足量稀盐酸,观察到的现象为_______ 。
(4)在步骤ⅵ中,___ (填“能”或“不能”)用稀硝酸代替稀盐酸进行该实验,理由为____ 。
(5)步骤ⅶ中操作b指的是_______ 。
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为_______ 。
 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案: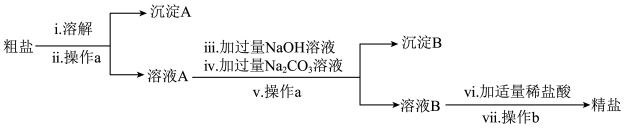
(1)为了加快粗盐的溶解,可采取的措施有
(2)写出步骤ⅳ中发生反应的化学方程式:
(3)沉淀B的主要成分为
(4)在步骤ⅵ中,
(5)步骤ⅶ中操作b指的是
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为
您最近一年使用:0次
【推荐3】海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体系的简图:
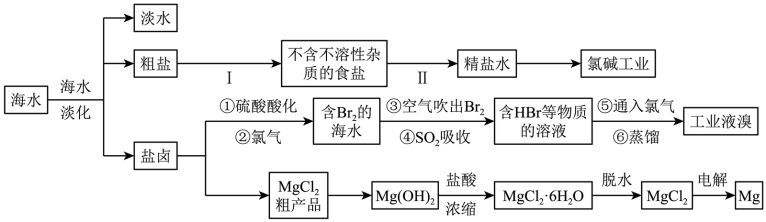
回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有__ 、__ 等。
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是___ 。
(3)粗盐中可溶性的杂质离子主要有SO 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是___ 。
Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为___ ;从理论上考虑下列也能吸收Br2的是___ 。
A.NaCl B.FeCl2 C.Na2SO3 D.H2O E.K2S
(5)经过步骤①②已获得Br2,不直接用含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、通入氯气”后再蒸馏,其目的是___ 。
Ⅳ.海水提镁
(6)该工业生产过程中,为了使MgCl2转化为Mg(OH)2,应加入的试剂为___ 。

回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是
(3)粗盐中可溶性的杂质离子主要有SO
 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为
A.NaCl B.FeCl2 C.Na2SO3 D.H2O E.K2S
(5)经过步骤①②已获得Br2,不直接用含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、通入氯气”后再蒸馏,其目的是
Ⅳ.海水提镁
(6)该工业生产过程中,为了使MgCl2转化为Mg(OH)2,应加入的试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】胶体金免疫层析法可用于快速检测新冠病毒抗体,胶体金是该技术的重要材料。目前最经典的制备胶体金的方法是柠檬酸钠还原法,具体步骤如下:
①量取50mL 0.1g/L的黄色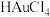 溶液,加热至沸腾;
溶液,加热至沸腾;
②搅拌的同时。迅速加入2mL 10g/L的柠檬酸钠溶液;
③保持加热和搅拌,一段时间后停止反应;
④使用孔径大小为0.22μm(微米)滤膜过滤溶液,获得产品。
已知:不同粒径胶体金的制备及特性:
回答下列问题:
(1)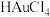 溶液可通过金溶解在王水中制得。王水的溶质为
溶液可通过金溶解在王水中制得。王水的溶质为___________ (填化学式)。
(2)经滤膜过滤后,留取___________ (填“滤液”或“滤渣”)为所制产品。
(3)本实验反应装置如图1所示,为避免水分挥发出现“干点”,安装在a口最合适的仪器是___________ (填仪器名称)。
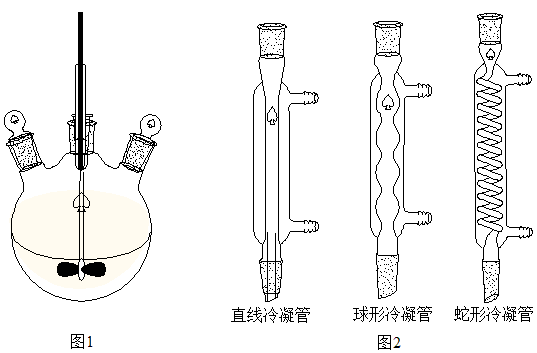
(4)步骤③中,当观察到液体___________ 时停止反应,关闭仪器的正确顺序为___________ (填选项编号)。
A.停止加热 B.关闭冷却水 C.停止搅拌
(5)结合生产实际从经济效益考虑,依据以上试剂量进行反应,获得胶体中金的理论最大质量为___________ mg(保留2位有效数字)。
(6)胶体金的制备还可选择葡萄糖还原,在碱性环境下加热葡萄糖与 混合溶液,葡萄糖变为葡萄糖酸钠(
混合溶液,葡萄糖变为葡萄糖酸钠(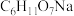 ),写出该反应化学方程式
),写出该反应化学方程式___________ ;某同学使用该方法制得的胶体金为灰黑色,请写出实验中可能存在的问题___________ 。
①量取50mL 0.1g/L的黄色
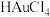 溶液,加热至沸腾;
溶液,加热至沸腾;②搅拌的同时。迅速加入2mL 10g/L的柠檬酸钠溶液;
③保持加热和搅拌,一段时间后停止反应;
④使用孔径大小为0.22μm(微米)滤膜过滤溶液,获得产品。
已知:不同粒径胶体金的制备及特性:
| 胶体金粒径(nm) | 柠檬酸钠加入量(mL) | 胶体金特性呈色 |
| 16 | 2.00 | 橙色 |
| 24.5 | 1.50 | 橙红 |
| 41 | 1.00 | 红色 |
| 71.5 | 0.70 | 紫色 |
(1)
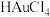 溶液可通过金溶解在王水中制得。王水的溶质为
溶液可通过金溶解在王水中制得。王水的溶质为(2)经滤膜过滤后,留取
(3)本实验反应装置如图1所示,为避免水分挥发出现“干点”,安装在a口最合适的仪器是

(4)步骤③中,当观察到液体
A.停止加热 B.关闭冷却水 C.停止搅拌
(5)结合生产实际从经济效益考虑,依据以上试剂量进行反应,获得胶体中金的理论最大质量为
(6)胶体金的制备还可选择葡萄糖还原,在碱性环境下加热葡萄糖与
 混合溶液,葡萄糖变为葡萄糖酸钠(
混合溶液,葡萄糖变为葡萄糖酸钠(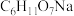 ),写出该反应化学方程式
),写出该反应化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上用铝土矿(主要成分为Al2O3、Fe2O3、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下:

(1)第一步在铝土矿中加入盐酸后的实验基本操作是______ ,若在固体B中加入氢氧化钠溶液________ (填”会”或”不会”)发生反应,若会,则写出反应的离子方程式____________ ;
(2)验证滤液A中是否含Fe3+,可取少量滤液A并加入___________ (填试剂名称),现象是______________________ 。
(3)在整个操作过程中_________ (填“是”或“否”)有氧化还原反应;写出碳酸氢钠的一种用途__________ 。

(1)第一步在铝土矿中加入盐酸后的实验基本操作是
(2)验证滤液A中是否含Fe3+,可取少量滤液A并加入
(3)在整个操作过程中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
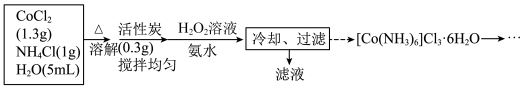
【推荐3】三氯化六氨合钴(III)([Co(NH3)6]Cl3)是一种重要的含钴配合物,由CoCl2制备它的流程如下:
回答下列问题:
(1)制备装置如图所示,装混合液的仪器名称是___________ ;___________ 。
(3)实验开始,向混合液加入H2O2溶液与氨水时,应最先打开活塞___________ (填字母代号);原料中加入NH4Cl有利于后续钴离子的络合反应,其原因是___________ 。加入所有试剂后,水浴的温度控制在55℃左右,反应约30分钟,温度控制在55℃左右的原因是___________ ;
(4)CoCl2制备[Co(NH3)6]Cl3的总反应化学方程式为___________ 。
(5)由滤渣获取[Co(NH3)6]Cl3•6H2O的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥,得到产品2.14g。
①下列选项合理的是___________ (填标号)。
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
②该反应的产率为___________
回答下列问题:
(1)制备装置如图所示,装混合液的仪器名称是

(3)实验开始,向混合液加入H2O2溶液与氨水时,应最先打开活塞
(4)CoCl2制备[Co(NH3)6]Cl3的总反应化学方程式为
(5)由滤渣获取[Co(NH3)6]Cl3•6H2O的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥,得到产品2.14g。
①下列选项合理的是
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为水 C.甲为浓盐酸,乙为乙醇
②该反应的产率为
您最近一年使用:0次



