已知:①C(s)+O2(g)=CO2(g)△H1= akJ•mol﹣1
②S(s)+2K(s)=K2S(s)△H2= bkJ•mol﹣1
③2K(s)+N2(g)+3O2(g)=2KNO3(s)△H3= ckJ•mol﹣1
则S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g)的热效应△H为( )
②S(s)+2K(s)=K2S(s)△H2= bkJ•mol﹣1
③2K(s)+N2(g)+3O2(g)=2KNO3(s)△H3= ckJ•mol﹣1
则S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g)的热效应△H为( )
| A.(a+b﹣c)kJ•mol﹣1 | B.(3a+b﹣c)kJ•mol﹣1 |
| C.(c﹣a﹣b)kJ•mol﹣1 | D.(c﹣3a﹣b)kJ•mol﹣1 |
18-19高三·河北石家庄·阶段练习 查看更多[3]
湖南省临湘市第五中学2021-2022学年高二上学期第一次月考化学试题(已下线)1.2.1 盖斯定律(练习)——2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河北省辛集中学2020届高三第三次阶段考试化学试题
更新时间:2019-12-19 16:15:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】我国大力推广氢能汽车,水煤气法是获得氢能的有效途径之一、
已知:①
②
③
④
已知:25℃、101kPa时,1mol纯物质完全燃烧生成稳定氧化物所放出的热量,叫该物质的燃烧热。下列说法正确的是
已知:①

②

③

④

已知:25℃、101kPa时,1mol纯物质完全燃烧生成稳定氧化物所放出的热量,叫该物质的燃烧热。下列说法正确的是
A.C(s)的燃烧热 |
B. |
C. |
| D.若将反应②设计成原电池,能将化学能全部转化成电能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 与
与 生成
生成 的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示。下列说法不正确的是
的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示。下列说法不正确的是

 与
与 生成
生成 的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示。下列说法不正确的是
的反应可以一步完成,也可以分两步完成,各步反应之间的关系如图所示。下列说法不正确的是
A. 燃烧是放热反应 燃烧是放热反应 |
B. 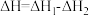 |
C.1mol 和1mol 和1mol 分别在足量 分别在足量 中燃烧生成 中燃烧生成 ,前者放热多 ,前者放热多 |
D.化学反应的 只与反应体系的始态和终态有关,与反应途径无关 只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】运载火箭以液氢为燃烧剂,液氧为氧化剂。已知:
①H2(g)=H2(l) ΔH=-0. 92 kJ·mol-1 ②O2(g)=O2(l) ΔH=-6. 84 kJ·mol-1
下列说法正确的是
①H2(g)=H2(l) ΔH=-0. 92 kJ·mol-1 ②O2(g)=O2(l) ΔH=-6. 84 kJ·mol-1
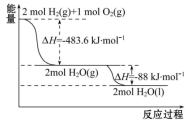
下列说法正确的是
| A.2 mol H2(g)与1 mol O2(g)所具有的总能量比2 mol H2O(g)所具有的总能量低 |
| B.氢气的燃烧热为ΔH=-241. 8 kJ·mol-1 |
C.火箭中液氢燃烧的热化学方程式为2H2(l)+O2(l) 2H2O(g) ΔH=-474. 92 kJ·mol-1 2H2O(g) ΔH=-474. 92 kJ·mol-1 |
| D.H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】研究表明 和
和 在催化剂存在下可发生反应生成
在催化剂存在下可发生反应生成 。已知部分反应的热化学方程式如下:
。已知部分反应的热化学方程式如下:

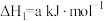
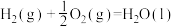
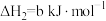
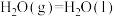
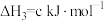
则 的
的 等于
等于
 和
和 在催化剂存在下可发生反应生成
在催化剂存在下可发生反应生成 。已知部分反应的热化学方程式如下:
。已知部分反应的热化学方程式如下:
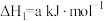
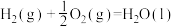
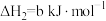
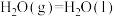
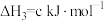
则
 的
的 等于
等于A.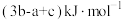 | B.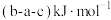 |
C.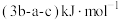 | D.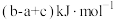 |
您最近一年使用:0次
【推荐2】已知下列两个热化学方程式:
①

②
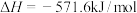 。
。
下列结论正确的是
①


②

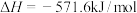 。
。下列结论正确的是
| A.①的反应热为221 kJ/mol |
| B.碳的燃烧热大于110.5 kJ/mol |
C.由②可知氢气的燃烧热为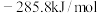 |
D.已知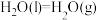 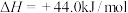 ,则 ,则  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】选择性催化还原烟气脱硝技术是一种成熟的NOx控制处理方法,主要反应如下:
4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH1=akJ·mol-1
4N2(g)+6H2O(g) ΔH1=akJ·mol-1
4NH3(g)+2NO2(g)+O2(g) 3N2(g)+6H2O(g) ΔH2=bkJ·mol-1
3N2(g)+6H2O(g) ΔH2=bkJ·mol-1
副反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH3=ckJ·mol-1
4NO(g)+6H2O(g) ΔH3=ckJ·mol-1
根据以上反应,可以计算出反应2NO(g)+O2(g) 2NO2(g)的ΔH为
2NO2(g)的ΔH为
4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH1=akJ·mol-1
4N2(g)+6H2O(g) ΔH1=akJ·mol-14NH3(g)+2NO2(g)+O2(g)
 3N2(g)+6H2O(g) ΔH2=bkJ·mol-1
3N2(g)+6H2O(g) ΔH2=bkJ·mol-1副反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) ΔH3=ckJ·mol-1
4NO(g)+6H2O(g) ΔH3=ckJ·mol-1根据以上反应,可以计算出反应2NO(g)+O2(g)
 2NO2(g)的ΔH为
2NO2(g)的ΔH为A. kJ·mol-1 kJ·mol-1 | B. kJ·mol-1 kJ·mol-1 |
C. kJ·mol-1 kJ·mol-1 | D. kJ·mol-1 kJ·mol-1 |
您最近一年使用:0次



