已知:SO32-+I2+H2O→SO42-+2I-+2H+。溴水和碘水均为有色液体。某溶液中可能含有Na+、NH4+、Fe2+、K+、I−、SO32- 、SO42−,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
| A.肯定不含I− | B.肯定含有SO32− |
| C.SO42−是否含有,不能确定 | D.肯定含有NH4+ |
更新时间:2019-12-18 15:43:58
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】取某固体样品,进行如下实验:
①取一定量的样品,加足量水充分溶解,得澄清透明溶液
②取10 mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
③分液后,将②中上层溶液加入足量BaCl2和HCl 溶液,产生白色沉淀2.33g;
④另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。该固体样品可能是
①取一定量的样品,加足量水充分溶解,得澄清透明溶液
②取10 mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
③分液后,将②中上层溶液加入足量BaCl2和HCl 溶液,产生白色沉淀2.33g;
④另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。该固体样品可能是
| A.NH4Cl、NaBr、(NH4)2SO4 | B.NaCl、NaBr、(NH4)2SO3 |
| C.NaBr、Na2CO3、(NH4)2SO4 | D.CuBr2、NaCl、(NH4)2SO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在MgCl2 、KCl、K2SO4三中盐的混合溶液中,若K+ 、Cl—、Mg2+的物质的量分别为1.5mol、1.5mol、0.5mol,则SO42—的物质的量为
| A.0.1mol | B.0.15mol | C.0.5mol | D.0.75mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】某无色溶滚中可能含有Na+、NH4+、Ba2+、Cu2+、SO42﹣、SO32﹣、Cl﹣、Br﹣、CO32﹣中的若干种.为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.下列关于原溶液的说法正确的是
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.下列关于原溶液的说法正确的是
| A.肯定存在NH4+、Cl﹣、Br﹣ |
| B.SO42﹣、SO32﹣至少含有一种 |
| C.是否存在Na+需要通过焰色反应来确定 |
| D.肯定不存在Ba2+、Cu2+、SO32﹣、CO32﹣ |
您最近一年使用:0次
【推荐1】工业上以铬铁矿(主要成分为 )、碳酸钠、氧气、硫酸为原料生产重铬酸钠
)、碳酸钠、氧气、硫酸为原料生产重铬酸钠 ,其主要反应为:(1)高温下发生反应:
,其主要反应为:(1)高温下发生反应: (未配平)
(未配平)
(2) ;下列说法正确的是
;下列说法正确的是
 )、碳酸钠、氧气、硫酸为原料生产重铬酸钠
)、碳酸钠、氧气、硫酸为原料生产重铬酸钠 ,其主要反应为:(1)高温下发生反应:
,其主要反应为:(1)高温下发生反应: (未配平)
(未配平)(2)
 ;下列说法正确的是
;下列说法正确的是| A.反应(1)和(2)均为氧化还原反应 |
B.反应(1)中每生成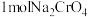 时电子转移 时电子转移 |
C.高温下, 的氧化性强于 的氧化性强于 ,弱于 ,弱于 |
D.反应(1)中参加反应的 与生成的 与生成的 物质的量之比 物质的量之比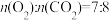 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】黄铁矿的主要成分是FeS2 (Fe为 价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO
价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO +16H+。下列说法中正确的是
+16H+。下列说法中正确的是
 价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO
价),利用Fe2(SO4)3溶液可以浸取黄铁矿中的Fe元素,浸取反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO +16H+。下列说法中正确的是
+16H+。下列说法中正确的是| A.反应中氧化产物和还原产物的物质的量之比为2∶15 |
| B.FeS2是反应中的氧化剂,发生还原反应 |
C.由反应可知氧化性:SO >Fe3+ >Fe3+ |
D.每生成1mol SO ,反应中转移的电子是7mol ,反应中转移的电子是7mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】将 、
、 、
、 、
、 、
、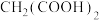 及可溶性淀粉(指示剂)混合进行碘钟实验,通过光线传感器绘制出碘钟振荡反应曲线如下图。下列说法正确的是
及可溶性淀粉(指示剂)混合进行碘钟实验,通过光线传感器绘制出碘钟振荡反应曲线如下图。下列说法正确的是

已知:碘钟周期性振荡的反应如下,除 与
与 外,其他物质在此溶液中为无色或浅色。
外,其他物质在此溶液中为无色或浅色。
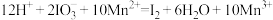 (琥珀色)
(琥珀色)
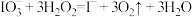
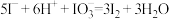

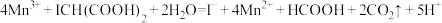
 、
、 、
、 、
、 、
、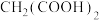 及可溶性淀粉(指示剂)混合进行碘钟实验,通过光线传感器绘制出碘钟振荡反应曲线如下图。下列说法正确的是
及可溶性淀粉(指示剂)混合进行碘钟实验,通过光线传感器绘制出碘钟振荡反应曲线如下图。下列说法正确的是
已知:碘钟周期性振荡的反应如下,除
 与
与 外,其他物质在此溶液中为无色或浅色。
外,其他物质在此溶液中为无色或浅色。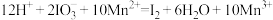 (琥珀色)
(琥珀色)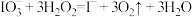
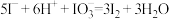

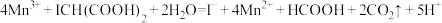
A.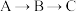 过程中,颜色变化为:蓝色→琥珀色→无色 过程中,颜色变化为:蓝色→琥珀色→无色 |
B. 过程放出的气体为 过程放出的气体为 |
C. 持续时间变长,是因为 持续时间变长,是因为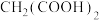 逐渐被消耗 逐渐被消耗 |
D.H点透光率减弱是因为 浓度下降 浓度下降 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】关于下列氧化还原反应说法正确的是
| A.对于11PH3+24CuSO4+12H2O=3H3PO4+24H2SO4+8Cu3P↓反应中每24molCuSO4氧化11molPH3 |
B.在淀粉和 的混合溶液中滴加 的混合溶液中滴加 溶液。[已知: 溶液。[已知: 、 、 分别与卤素单质、卤素离子性质相似],溶液仍为蓝色,证明氧化性: 分别与卤素单质、卤素离子性质相似],溶液仍为蓝色,证明氧化性: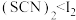 |
| C.K2H3IO6+9HI=2KI+4I2+6H2O,还原剂与氧化剂的物质的量之比为7:1 |
D. ,产生22.4L(标准状况) ,产生22.4L(标准状况) 时,反应中转移 时,反应中转移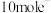 |
您最近一年使用:0次



