现有34gNH3,请通过计算填空:
(1)该气体物质的量为___ mol,所含H原子数目为___ 。
(2)该气体在标准状况下的体积为___ L。
(3)若将该气体溶于水配成VL溶液,所得溶液溶质的物质的量浓度为___ mol/L。
(4)若将该气体溶100mL水中,所得溶液溶质的质量分数约为___ %(小数点后保留一位小数)。
(1)该气体物质的量为
(2)该气体在标准状况下的体积为
(3)若将该气体溶于水配成VL溶液,所得溶液溶质的物质的量浓度为
(4)若将该气体溶100mL水中,所得溶液溶质的质量分数约为
更新时间:2019-12-25 17:27:59
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】胶体金即金溶胶,其具有光吸收性、呈色性和胶体性等特点。免疫胶体金技术作为胶体金标记物,可实现对抗原抗体的测定。用白磷还原法可制得一种金(①)的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。其操作步骤如下:
a.取20%白磷(②)的乙醚溶液(③)0.5mL,加蒸馏水(④)60mL。
b.先滴加1%氯化金(AuCl)水溶液0.75 mL,再加入K2CO3粉末(⑤)0. 69 g,振荡变成棕红色。
c.加热煮沸至溶液变成透明红色即可。
d.分离提纯,除去无机溶质。
所得分散系中,金颗粒直径在5~12 nm之间。
请回答下列问题:
(1)上述物质①②③④⑤中属于混合物的是___________ (填序号, 下同),属于电解质的___________ ,属于单质的是___________ 。
(2)写出氯化金在水溶液中的电离方程式___________ 。
(3)判断该分散系属于胶体的有力证据是___________ 。
(4)0.69gK2CO3中含有的原子数目为___________ 。
a.取20%白磷(②)的乙醚溶液(③)0.5mL,加蒸馏水(④)60mL。
b.先滴加1%氯化金(AuCl)水溶液0.75 mL,再加入K2CO3粉末(⑤)0. 69 g,振荡变成棕红色。
c.加热煮沸至溶液变成透明红色即可。
d.分离提纯,除去无机溶质。
所得分散系中,金颗粒直径在5~12 nm之间。
请回答下列问题:
(1)上述物质①②③④⑤中属于混合物的是
(2)写出氯化金在水溶液中的电离方程式
(3)判断该分散系属于胶体的有力证据是
(4)0.69gK2CO3中含有的原子数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)0.2 mol 某气体的质量为8.8g,该气体的摩尔质量为____ ,在标准状况下,该气体的体积是___________ ;
(2)物质的量相同的O2和O3,其分子数之比为___ ,质量比为_____ ,氧原子个数比为_____ ,同温同压下气体的体积比为_____ ;
(3)将11.7g NaCl固体溶于水配成500mL溶液,此溶液中NaCl的物质的量浓度为____ ,从配好的溶液中取出100mL,加水稀释至1000mL,则稀释后NaCl溶液的物质的量浓度为___ 。
(1)0.2 mol 某气体的质量为8.8g,该气体的摩尔质量为
(2)物质的量相同的O2和O3,其分子数之比为
(3)将11.7g NaCl固体溶于水配成500mL溶液,此溶液中NaCl的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)标准状况下,2molNH3与______ gCO2的体积相等。
(2)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为_______ 。
(3)在同温同压下,等质量的CO和CO2,其体积之比为______ ,密度之比为_____ ,质子数之比________ 。
(1)标准状况下,2molNH3与
(2)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(3)在同温同压下,等质量的CO和CO2,其体积之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)0.5 mol H2O的质量为 ____ ,其中含有_____ 个水分子,共有____ 个原子。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是______ ,在相同温度和相同压强条件下,体积最大的是______ ,体积最小的是________ 。
(3)在_______ mL 0.2 mol/L NaOH溶液中含1 g溶质;配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O _________ g。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
(3)在
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】假定把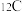 的相对原子质量定为24,把24 g
的相对原子质量定为24,把24 g 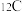 含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。此时142 g
含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。此时142 g  配成1 L溶液,其物质的量浓度为
配成1 L溶液,其物质的量浓度为_______ 。
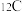 的相对原子质量定为24,把24 g
的相对原子质量定为24,把24 g 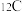 含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。此时142 g
含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。此时142 g  配成1 L溶液,其物质的量浓度为
配成1 L溶液,其物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:
(1)混合液中,硝酸铵的物质的量为___________ ,硝酸钾的质量为___________ 。
(2)该混合溶液中硝酸镁的物质的量浓度为___________ ,将该混合溶液加水稀释至体积为 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(3)向该稀释后的溶液中通入标准状况下的
___________ L可使 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式___________ 。
 ,部分离子的浓度如下表所示:
,部分离子的浓度如下表所示:| 离子种类 |  |  |  |
离子的物质的量浓度( ) ) | 0.2 | 0.1 | 0.6 |
(1)混合液中,硝酸铵的物质的量为
(2)该混合溶液中硝酸镁的物质的量浓度为
 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为(3)向该稀释后的溶液中通入标准状况下的

 沉淀完全,写出
沉淀完全,写出 沉淀过程中的离子方程式
沉淀过程中的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求完成下列题目:
(1)在标准状况下,0.2NA二氧化碳所占体积是_____________ ;
(2)将含有4mol氢原子的硫酸,配成1L的溶液,则溶质的物质的量浓度是__________ 。
(1)在标准状况下,0.2NA二氧化碳所占体积是
(2)将含有4mol氢原子的硫酸,配成1L的溶液,则溶质的物质的量浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)在AlCl3溶液中滴加过量的氨水,反应的化学方程式为__________________ 。
(2)碳酸氢钠与稀硫酸反应的离子方程式__________________ ;铜与浓硫酸共热反应的化学方程式__________________ 。
(3)现有0.284kg质量分数为10%的Na2SO4溶液,则溶液中Na2SO4的物质的量为______ ;配制250mL2.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液的体积_________ mL。
(4)同一主族元素性质具有一定的相似性和递变性;同一主族,从上到下:原子的电子层数逐渐____________ ,原子半径逐渐____________ ;失电子能力逐渐____________ ,金属性逐渐____________ ;得电子能力逐渐 ___________ ,非金属性逐渐____________ 。
(5)A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1。回答下列问题:
写出E元素的元素符号:________ 画出B、C的原子结构示意图:B.________ C________ 画出D的离子结构示意图:________ 。
(2)碳酸氢钠与稀硫酸反应的离子方程式
(3)现有0.284kg质量分数为10%的Na2SO4溶液,则溶液中Na2SO4的物质的量为
(4)同一主族元素性质具有一定的相似性和递变性;同一主族,从上到下:原子的电子层数逐渐
(5)A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1。回答下列问题:
写出E元素的元素符号:
您最近一年使用:0次



