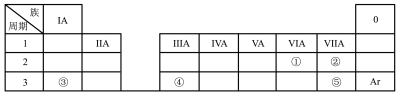
从宏观和微观两个角度认识氯、硫、铁、铝等元素的单质及其化合物是学好中学化学的重要基础。完成下列填空:
(1)Cl在元素周期表中的位置为______________ ,由此可知,其最高价氧化物对应的水化物的化学式 为:______________ ,次氯酸分子的结构式为:_____________ 。
(2)Cl、S、Na三种元素形成简单离子其半径由大到小的顺序是_______________________ (用离子符号 表示)。铝最高价氧化物对应的水化物表现出了独特的性质,其在水溶液中的电离方程式 为____________________________________________________________________________ 。
(3)硫和氯的非金属性强弱关系是_________________ ,试从原子结构的角度解释其原因。______________
(4)现有试剂:溴水、硫化钠溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水。 要证明Na2SO3具有还原 性,应选用的试剂有______________ ,看到的现象是 ____________________ 。要证明Na2SO3具有氧化性,应选用的试剂有___________________ ,反应的离子方程式是 ________________________________ 。
(1)Cl在元素周期表中的位置为
(2)Cl、S、Na三种元素形成简单离子其半径由大到小的顺序是
(3)硫和氯的非金属性强弱关系是
(4)现有试剂:溴水、硫化钠溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水。 要证明Na2SO3具有还原 性,应选用的试剂有
更新时间:2019-12-29 10:47:19
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】化学在药物的开发、合成和使用中起着至关重要的作用。
(1)下面是一种常见药品说明书的部分内容,请将其补充完整。
【药品名称】碳酸氢钠。
【其他名称】重碳酸钠、酸性碳酸钠、____ 。
【功效主治】适用于胃酸过多、消化不良及碱化尿液等;静脉给药用于酸中毒;外用滴耳软化耵聍。
【不良反应】对胃溃疡的病人,中和胃酸时产生的气体会刺激溃疡面,甚至有胃穿孔的危险。其中的化学原理(用离子方程式表示)是____ 。
(2)胃舒平(复方氢氧化铝)也可以治疗胃酸过多,所依据的反应原理(用离子方程式表示)是____ 。
(3)氢氧化铝跟氢氧化钠溶液反应的离子方程式是____ 。
(4)根据金属钠的性质填空
金属钠切开后,光亮的金属断面____ ,说明常温下钠能够跟____ 反应,生成____ ;钠投入水中,钠____ 水面上,并四处游动,发出响声,这说明____ ,熔成一个闪亮的小球,说明____ ,最后向烧杯中滴加酚酞,溶液变____ ,反应的化学方程式为:____ 。
(5)用金属钠制取过氧化钠的化学方程式____ ,现象是____ 。
(1)下面是一种常见药品说明书的部分内容,请将其补充完整。
【药品名称】碳酸氢钠。
【其他名称】重碳酸钠、酸性碳酸钠、
【功效主治】适用于胃酸过多、消化不良及碱化尿液等;静脉给药用于酸中毒;外用滴耳软化耵聍。
【不良反应】对胃溃疡的病人,中和胃酸时产生的气体会刺激溃疡面,甚至有胃穿孔的危险。其中的化学原理(用离子方程式表示)是
(2)胃舒平(复方氢氧化铝)也可以治疗胃酸过多,所依据的反应原理(用离子方程式表示)是
(3)氢氧化铝跟氢氧化钠溶液反应的离子方程式是
(4)根据金属钠的性质填空
金属钠切开后,光亮的金属断面
(5)用金属钠制取过氧化钠的化学方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】近年来,铝在汽车、航天、机械制造、军事等产业中应用迅猛发展。
(1)铝元素的离子结构示意图为_______ ;工业上,用冰晶石作助熔剂、石墨作电极电解熔融氧化铝制铝,请写出电解反应方程式__________ ;在电解过程中____ 极(填“阴”或“阳”)需要定期补充。
(2)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性
①请写出Be(OH)2溶于NaOH溶液的化学方程式为:________ ;
②往10.0mL1.00 mol/L的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加入量的变化图:_____________

(1)铝元素的离子结构示意图为
(2)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性
①请写出Be(OH)2溶于NaOH溶液的化学方程式为:
②往10.0mL1.00 mol/L的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加入量的变化图:

您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)研究表明26Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是_______ (填字母,下同)。
a.比较这两种元素的单质的硬度和熔点
b.Mg(OH)2属于中强碱,Al(OH)3属于两性氢氧化物
c.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液
d.将空气中放置已久的这两种元素的单质分别和热水作用
(2)某同学认为铝有一定的非金属性,下列化学反应中,你认为能支持该同学观点的是_______ 。
a.铝片与盐酸反应放出氢气
b.氢氧化铝溶于强碱溶液
c.氢氧化铝溶于强酸溶液
(1)研究表明26Al可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是
a.比较这两种元素的单质的硬度和熔点
b.Mg(OH)2属于中强碱,Al(OH)3属于两性氢氧化物
c.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液
d.将空气中放置已久的这两种元素的单质分别和热水作用
(2)某同学认为铝有一定的非金属性,下列化学反应中,你认为能支持该同学观点的是
a.铝片与盐酸反应放出氢气
b.氢氧化铝溶于强碱溶液
c.氢氧化铝溶于强酸溶液
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)元素最高正化合价为+6,其负化合价为____ ,某元素R与氢形成的气态氢化物的化学式为RH3,其最高价氧化物的化学式为___________ 。
(2)下列各题中有关物质的比较,请用“>”、“<”、“=”填空
酸性: H3PO4____ HNO3 ,H2SO4______ HClO4
热稳定性:CH4_____ NH3 ,HCl____ HI
(3)1~18号元素中,最外层电子数是次外层电子数二倍的元素是______ ,原子结构示意图_______________ ,能与氧形成的氧化物的化学式________ 、_______ 。
(2)下列各题中有关物质的比较,请用“>”、“<”、“=”填空
酸性: H3PO4
热稳定性:CH4
(3)1~18号元素中,最外层电子数是次外层电子数二倍的元素是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】用“>”或“<”回答下列问题:
(1)酸性:H2CO3___ H2SiO3,H2SiO3___ H3PO4。
(2)碱性:Ca(OH)2___ Mg(OH)2,Mg(OH)2___ Al(OH)3。
(3)气态氢化物的稳定性:H2O___ H2S,H2S___ HCl。
(4)还原性:H2O__ H2S,H2S___ HCl。
从以上答案中可以归纳出:
①元素的非金属性越强,其最高价氧化物对应水化物的酸性越___ 。
②元素的金属性越强,其最高价氧化物对应水化物的碱性越___ 。
③元素___ 性越强,其对应气态氢化物的稳定性越强。
④元素非金属性越强,其对应气态氢化物的还原性越__ 。
(1)酸性:H2CO3
(2)碱性:Ca(OH)2
(3)气态氢化物的稳定性:H2O
(4)还原性:H2O
从以上答案中可以归纳出:
①元素的非金属性越强,其最高价氧化物对应水化物的酸性越
②元素的金属性越强,其最高价氧化物对应水化物的碱性越
③元素
④元素非金属性越强,其对应气态氢化物的还原性越
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】1808年科学家戴维通过电解生石灰和汞的混合物制得了银白色的金属钙。请回答:
(1)钙的原子结构示意图为_______ ,它在元素周期表中的位置是_______
(2)原子半径:Ca_______ (填“>”或“<”,下同)Mg;氧化性:Ca2+_______ Mg2+
(3)科学家经分析后提出了有关推断,其中正确的是_______ (填选项序号)。
①自然界可能存在钙的单质②钙的金属性强于铝③钙与氧气不能反应
(4)钙的金属性_______ (填“强于”或“弱于”)镁,可以通过_______ (填实验方法)加以验证。
(1)钙的原子结构示意图为
(2)原子半径:Ca
(3)科学家经分析后提出了有关推断,其中正确的是
①自然界可能存在钙的单质②钙的金属性强于铝③钙与氧气不能反应
(4)钙的金属性
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,根据表中给出10种元素(其中X、Y分别代表某种化学元素),按要求作答。
(1)X、Y两种元素符号分别是___________ 和___________ ;
(2)最外层电子数为4的原子,其元素符号是___________ ;
(3)某阴离子结构示意图为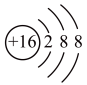 ,该离子符号是
,该离子符号是___________ ;
(4)C与N原子半径较小的是___________ ;
(5)保存在煤油中的金属是___________ ;
(6)化学性质最不活泼的单质是___________ ;
(7)HF与HCl热稳定性较强的是___________ ;
(8) 与
与 酸性较强的是
酸性较强的是___________ ;NaOH与 碱性较弱的是
碱性较弱的是___________ ;
(9)写出Y元素组成的单质与氧气反应的化学方程式:___________ 。
周期 族 | IA | IIA | ⅢA | IVA | VA | ⅥA | ⅦA | O |
| 2 | C | N | X | F | Ne | |||
| 3 | Na | Mg | Y | S | Cl |
(1)X、Y两种元素符号分别是
(2)最外层电子数为4的原子,其元素符号是
(3)某阴离子结构示意图为
 ,该离子符号是
,该离子符号是(4)C与N原子半径较小的是
(5)保存在煤油中的金属是
(6)化学性质最不活泼的单质是
(7)HF与HCl热稳定性较强的是
(8)
 与
与 酸性较强的是
酸性较强的是 碱性较弱的是
碱性较弱的是(9)写出Y元素组成的单质与氧气反应的化学方程式:
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】亚硫酸钠中+4价的硫既有氧化性又有还原性。现有试剂:氯水、硫化钠溶液、亚硫酸钠溶液、稀硫酸、氢氧化钠溶液。
(1)要证明亚硫酸溶液具有还原性,应选用什么试剂____ ?会观察到什么现象____ ?写出反应的离子方程式____ 。
(2)要证明亚硫酸钠溶液具有氧化性,应选用什么试剂____ ?会观察到什么现象____ ?写出反应的离子方程式____ 。
(3)如何通过实验证明亚硫酸钠已被氧化____ ?
(1)要证明亚硫酸溶液具有还原性,应选用什么试剂
(2)要证明亚硫酸钠溶液具有氧化性,应选用什么试剂
(3)如何通过实验证明亚硫酸钠已被氧化
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(Ⅰ)近年来我国对碳纳米管的研究也有了较大突破,即用电弧合成法来制碳纳米管,但往往有大量的碳纳米颗粒,需用氧化法来提纯这些颗粒,化学方程式为:

试回答下列问题:
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂为_______ ,被氧化的元素为________ 。
(3)H2SO4在上述反应中表现出来的性质是___ (填字母)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若生成11 g CO2,则转移电子的数目为__________ 。
(Ⅱ)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1型流感(或称H1N1型猪流感)疫情,随后也不断蔓延我国各地.防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感.
(5)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
_______________________________________________________
(6)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只被还原的是____ 。
A. MnO2 B.KMnO4溶液
C.稀盐酸 D.Na2SO3溶液
(7)漂白剂亚氯酸钠(NaClO2)在常温于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是____ 。

试回答下列问题:
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂为
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若生成11 g CO2,则转移电子的数目为
(Ⅱ)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1型流感(或称H1N1型猪流感)疫情,随后也不断蔓延我国各地.防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感.
(5)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
(6)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只被还原的是
A. MnO2 B.KMnO4溶液
C.稀盐酸 D.Na2SO3溶液
(7)漂白剂亚氯酸钠(NaClO2)在常温于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是
您最近半年使用:0次