制备漂白粉的化学方程式为___________ 。Ca(ClO)2中三种元素的离子半径从大到小的顺序为___________ 。
更新时间:2023-03-30 16:01:58
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)写出下列反应的方程式
①实验室制备氯气的离子方程式___________ 。
②工业上制备漂白粉的化学方程式___________ 。
(2)下列物质能导电的是___________ ,属于电解质的是___________ (填序号)。
①NaCl溶液②熔化的KNO3③液态氯化氢④铁⑤硫酸钡固体⑥蔗糖(C12H22O11)⑦氨气⑧硫酸氢钠固体
写出⑧在水溶液中的电离方程式___________ 。
①实验室制备氯气的离子方程式
②工业上制备漂白粉的化学方程式
(2)下列物质能导电的是
①NaCl溶液②熔化的KNO3③液态氯化氢④铁⑤硫酸钡固体⑥蔗糖(C12H22O11)⑦氨气⑧硫酸氢钠固体
写出⑧在水溶液中的电离方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病的有效方法之一、漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]中制取漂白粉,化学方程式为__________________ 。
(2)漂白粉溶于水后,与空气中的CO2作用,产生有漂白、杀菌作用的次氯酸,化学方程式为______________________ 。
(1)工业上将氯气通入石灰乳[Ca(OH)2]中制取漂白粉,化学方程式为
(2)漂白粉溶于水后,与空气中的CO2作用,产生有漂白、杀菌作用的次氯酸,化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】化学与人类生产、生活密切相关,按要求回答下列问题。
(1)铁及其化合物中,常用作红色油漆与涂料的是_______ (填化学式);具有磁性的黑色晶体是_______ (填化学式)。
(2)①“84消毒液”②高铁酸钠 ③碘酒④
③碘酒④ 酒精⑤
酒精⑤ 是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是
是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是_______ (填序号),写出②的电离方程式为_______ ,双氧水也是常用消毒剂,其电子式为_______ 。
(3)钠的化合物中,可用作潜水艇中供氧剂的是_______ (填名称),其与 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(4)印刷电路板用途广泛,电子工业中常用覆铜板为基材,利用 溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为
溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为_______ ;其氧化剂为_______ 。
(1)铁及其化合物中,常用作红色油漆与涂料的是
(2)①“84消毒液”②高铁酸钠
 ③碘酒④
③碘酒④ 酒精⑤
酒精⑤ 是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是
是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是(3)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(4)印刷电路板用途广泛,电子工业中常用覆铜板为基材,利用
 溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为
溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求写出下列反应的方程式。
(1)Na2CO3溶液与足量稀盐酸的化学方程式:___________ ;
(2)BaCl2溶液与Na2SO4溶液的离子方程式:___________ ;
(3)制备漂白液的化学方程式为:___________ 。
(1)Na2CO3溶液与足量稀盐酸的化学方程式:
(2)BaCl2溶液与Na2SO4溶液的离子方程式:
(3)制备漂白液的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】实验装置
装置特点:固+液 气。
气。

(1)仪器a的名称_______ ,仪器b的名称_______ 。
(2)Cl2的收集方法是_______ 。
(3)烧杯中NaOH溶液的作用是_______ 。
(4)A装置中导出的气体有Cl2、HCl、H2O(g)等。
装置特点:固+液
 气。
气。
(1)仪器a的名称
(2)Cl2的收集方法是
(3)烧杯中NaOH溶液的作用是
(4)A装置中导出的气体有Cl2、HCl、H2O(g)等。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】研究氯水的性质
(1) 和水反应的离子方程式为
和水反应的离子方程式为___________ ; 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为___________
(2)将制得的 溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象不能得出相应结论的是
溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象不能得出相应结论的是___________ (填字母)。
(3)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。

结合化学反应反应方程式解释上两图中曲线变化的原因___________ 。
(1)
 和水反应的离子方程式为
和水反应的离子方程式为 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为(2)将制得的
 溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象不能得出相应结论的是
溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象不能得出相应结论的是| 操作 | 现象 | 结论 | |
| a | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含 |
| b | 向饱和 溶液中加入足量氯水 溶液中加入足量氯水 | 有无色气体产生 | 氯水中含 |
| c | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
| d | 向淀粉碘化钾试纸上滴加少量氯水 | 试纸变蓝 | 氯水具有氧化性 |
(3)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。

结合化学反应反应方程式解释上两图中曲线变化的原因
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如图是元素周期表的框架,请在表中①~⑩元素中回答问题

请用化学语言回答下列问题:
(1)在表中④、⑤、⑥三种元素的简单离子半径由大到小的顺序为______。
(2)其中⑤与⑦两元素的最高价氧化物的水化物反应的离子方程式为______。
(3)⑧与⑩两种元素非金属较强的是______,请用一个离子方程式证明该结论______。
(4)①与③的两种单质可以在金属铂做电极时构成一种对环境友好的燃料电池,电解质为⑨的最高价氧化物的水化物,请书写出正极反应式______,电池工作时阴离子定向移动到______极(填正或负)。
(5)元素①与⑧的两种单质在一定条件下可反应生成一种化合物甲,已知下表中的数据是破坏1mol物质中的化学键所吸收的能量(kJ),则生成1mol甲时释放的能量为______kJ。

请用化学语言回答下列问题:
(1)在表中④、⑤、⑥三种元素的简单离子半径由大到小的顺序为______。
(2)其中⑤与⑦两元素的最高价氧化物的水化物反应的离子方程式为______。
(3)⑧与⑩两种元素非金属较强的是______,请用一个离子方程式证明该结论______。
(4)①与③的两种单质可以在金属铂做电极时构成一种对环境友好的燃料电池,电解质为⑨的最高价氧化物的水化物,请书写出正极反应式______,电池工作时阴离子定向移动到______极(填正或负)。
(5)元素①与⑧的两种单质在一定条件下可反应生成一种化合物甲,已知下表中的数据是破坏1mol物质中的化学键所吸收的能量(kJ),则生成1mol甲时释放的能量为______kJ。
| 化学键 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表列出了A~R9种元素在周期表中的位置:
(1)在这9种元素中化学性质最不活泼的是_____
A.E B.D C.R D.H
(2)A、B、C三种元素按原子半径由大到小的顺序排列为_____
A.r(A)>r(B)>r(C) B.r(B)>r(A)>r(C)
C.r(A)>r(C)>r(B) D.r(B)>r(C)>r(A)
(3)F元素氢化物在常温下跟A发生反应所得溶液的pH______ 7
A.< B.> C.= D.无法确定
(4)在此周期表中,9种元素所形成的最高价氧化物对应的水化物,其中酸性最强和碱性最强的化学式是_____
A.H2SO4,NaOH B.H2SO4,KOH
C.HClO4,NaOH D.HClO4,KOH
(5)G元素和H元素两者核电荷数之差是_____
A.8 B.10 C.18 D.26
(6)H元素和A元素形成化合物的化学式以及高温灼烧该化合物时,火焰颜色____
A.NaBr 黄 B.NaCl 黄 C.KBr 紫 D.KCl 紫
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
A.E B.D C.R D.H
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
A.r(A)>r(B)>r(C) B.r(B)>r(A)>r(C)
C.r(A)>r(C)>r(B) D.r(B)>r(C)>r(A)
(3)F元素氢化物在常温下跟A发生反应所得溶液的pH
A.< B.> C.= D.无法确定
(4)在此周期表中,9种元素所形成的最高价氧化物对应的水化物,其中酸性最强和碱性最强的化学式是
A.H2SO4,NaOH B.H2SO4,KOH
C.HClO4,NaOH D.HClO4,KOH
(5)G元素和H元素两者核电荷数之差是
A.8 B.10 C.18 D.26
(6)H元素和A元素形成化合物的化学式以及高温灼烧该化合物时,火焰颜色
A.NaBr 黄 B.NaCl 黄 C.KBr 紫 D.KCl 紫
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素,回答下列问题:
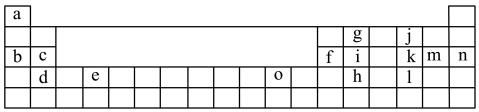
(1)表中所列元素中:属于短周期主族元素的有___________ 种,化学性质最稳定的元素是___________ (填元素符号),h元素在周期表中的位置是___________ 。
(2)下列___________元素的单质可能都是电的良导体。
(3)1元素的最高正化合价为___________ ,b与f两元素的最高价氧化物对应水化物间相互反应的离子方程式为___________ 。
(4)b、c、k三种元素原子半径由大到小的顺序是___________ (用元素符号作答)。
(5)比较c和d两元素原子的失电子能力的强弱,并从原子结构角度进行论证___________ 。
(6)比较元素i、k、m的最高价氧化物对应水化物,按酸性从强到弱的顺序排列为___________ 。

(1)表中所列元素中:属于短周期主族元素的有
(2)下列___________元素的单质可能都是电的良导体。
| A.b、c、i | B.a、g、k | C.c、g、o | D.d、e、f |
(3)1元素的最高正化合价为
(4)b、c、k三种元素原子半径由大到小的顺序是
(5)比较c和d两元素原子的失电子能力的强弱,并从原子结构角度进行论证
(6)比较元素i、k、m的最高价氧化物对应水化物,按酸性从强到弱的顺序排列为
您最近一年使用:0次



