近年科学家提出“绿色自由”构想。把含有大量 的空气吹入
的空气吹入 溶液中,再把
溶液中,再把 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与 反应生成可再生能源甲醇。其工艺流程如图所示:
反应生成可再生能源甲醇。其工艺流程如图所示:
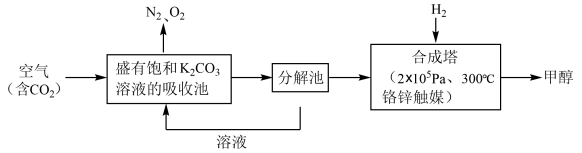
(1)分解池中主要物质是______ ;
(2)在合成塔中,若有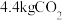 与足量
与足量 恰好完全反应,生成气态的水和甲醇,可放出5370kJ的热量,写出该反应的热化学方程式
恰好完全反应,生成气态的水和甲醇,可放出5370kJ的热量,写出该反应的热化学方程式______ ;
(3)该工艺在那些方面体现了“绿色自由”构想中的“绿色”______ 。(答二条)
(4)一定条件下,向2L恒容密闭容器中充入1mol 和3mol
和3mol  ,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内
,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
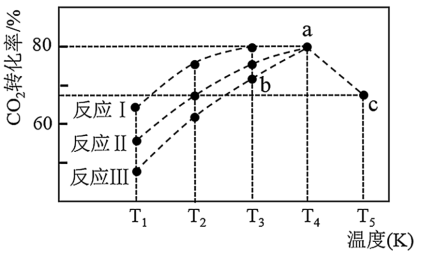
 图中c点的转化率为
图中c点的转化率为 ,即转化了
,即转化了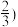
①催化剂效果最佳的反应是______ (填“反应I”,“反应II”,“反应III”)。
②b点v (正)______ v (逆)(填“>”,“<”,“=”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是______ 。
④c点时该反应的平衡常数K=______ 。
⑤一定条件下,向2L恒容密闭的上述容器中再充入1mol 和3mol
和3mol  ,达到新的化学平衡后,
,达到新的化学平衡后, 的浓度较原平衡浓度
的浓度较原平衡浓度______  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
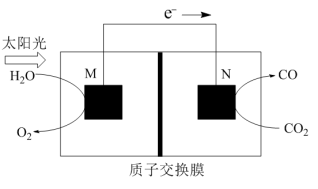
(5)科学家还研究了其它转化温室气体的方法,利用图所示装置可以将 转化为气体燃料
转化为气体燃料 该装置工作时,N电极的电极反应式为
该装置工作时,N电极的电极反应式为______ 。
 的空气吹入
的空气吹入 溶液中,再把
溶液中,再把 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与 反应生成可再生能源甲醇。其工艺流程如图所示:
反应生成可再生能源甲醇。其工艺流程如图所示:
(1)分解池中主要物质是
(2)在合成塔中,若有
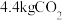 与足量
与足量 恰好完全反应,生成气态的水和甲醇,可放出5370kJ的热量,写出该反应的热化学方程式
恰好完全反应,生成气态的水和甲醇,可放出5370kJ的热量,写出该反应的热化学方程式(3)该工艺在那些方面体现了“绿色自由”构想中的“绿色”
(4)一定条件下,向2L恒容密闭容器中充入1mol
 和3mol
和3mol  ,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内
,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:
 图中c点的转化率为
图中c点的转化率为 ,即转化了
,即转化了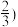
①催化剂效果最佳的反应是
②b点v (正)
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是
④c点时该反应的平衡常数K=
⑤一定条件下,向2L恒容密闭的上述容器中再充入1mol
 和3mol
和3mol  ,达到新的化学平衡后,
,达到新的化学平衡后, 的浓度较原平衡浓度
的浓度较原平衡浓度 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。(5)科学家还研究了其它转化温室气体的方法,利用图所示装置可以将
 转化为气体燃料
转化为气体燃料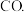 该装置工作时,N电极的电极反应式为
该装置工作时,N电极的电极反应式为
更新时间:2020-01-07 18:17:59
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图所示。
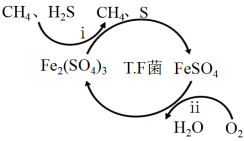
(1)过程i中H2S发生了___ (填“氧化”或“还原”)反应。
(2)过程ii的离子方程式是___ 。
(3)已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
请结合以上信息,判断工业脱硫应选择的最佳pH范围,并说明原因:___ 。
II.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。
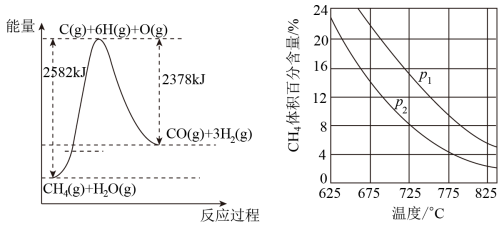
(4)①该过程的热化学方程式是___ 。
②比较压强p1和p2的大小关系:p1___ p2(选填“>”“<”或“=”)。
III.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
IV.H2提纯:将CO2和H2分离得到H2的过程示意图如图。
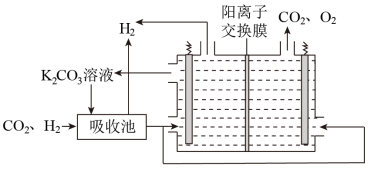
(5)①吸收池中发生反应的离子方程式是___ 。
②结合电极反应式,简述K2CO3溶液的再生原理:___ 。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图所示。

(1)过程i中H2S发生了
(2)过程ii的离子方程式是
(3)已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
| Fe2+氧化速率/(g·L-1·h-1) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
II.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(4)①该过程的热化学方程式是
②比较压强p1和p2的大小关系:p1
III.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
IV.H2提纯:将CO2和H2分离得到H2的过程示意图如图。

(5)①吸收池中发生反应的离子方程式是
②结合电极反应式,简述K2CO3溶液的再生原理:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E、F、G是元素周期表中1~36号的七种常见元素,其原子序数依次增大。其中B、D、G三种元素的原子核外未成对电子数均等于其周期序数;F的单质常用于工业上制漂白粉;D与A、E均可形成原子个数比为1:1和1:2的化合物,请回答下列问题:
(1)F在元素周期表中的位置_____________ ,B、C、D、E元素第一电离能由大到小的顺序是____________ (用元素符号表示)。
(2)F、G两元素的单质间反应所得产物为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醇,丙酮等有机溶剂,据此判断该产物晶体为______ 晶体,该产物中G元素相应价态离子的核外电子排布式为__________________ 。
(3)B、C、D均可与A形成10电子和18电子的分子。
①在B、C、D分别与A形成的10电子分子中,极性最强的共价键是______ (用化学键表示),A、B、C三元素形成的最简单分子中σ键与π键个数比为______ 。
②C、D分别与A形成的18电子分子X、Y可用作火箭推进剂,已知16g液态X与足量液态Y充分反应生成一种液态化合物和一种气态单质,并放出838kJ的热量,试写出X与Y反应的热化学方程式___________________ 。
(1)F在元素周期表中的位置
(2)F、G两元素的单质间反应所得产物为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醇,丙酮等有机溶剂,据此判断该产物晶体为
(3)B、C、D均可与A形成10电子和18电子的分子。
①在B、C、D分别与A形成的10电子分子中,极性最强的共价键是
②C、D分别与A形成的18电子分子X、Y可用作火箭推进剂,已知16g液态X与足量液态Y充分反应生成一种液态化合物和一种气态单质,并放出838kJ的热量,试写出X与Y反应的热化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。
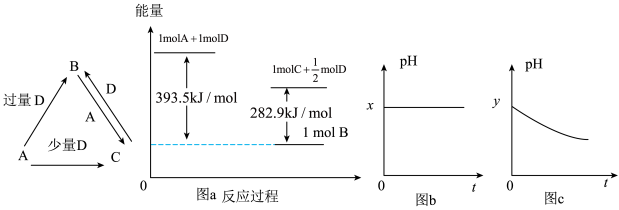
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为____________________ 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则①C的化学式为_________________ ;②反应B+A→C的离子方程式为______________________ ;
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为____________ (填化学式),此时图b中x___________ 7(填“﹥”“﹤”“﹦”)②若图c符合事实,则其pH变化的原因是________________ (用离子方程式表示)。
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式:________________________________ 。

(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则①C的化学式为
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】按要求回答下列有关问题。
(1)据报道,科学家新研发出一种常温下催化合成NH3的方法:2N2(g)+6H2O(l)=4NH3(g)+3O2(g)
已知如下信息:
①化合物的生成热可以表示其相对能量。化学上,规定标准状况下稳定单质的生成热为0。几种物质的生成热:NH3(g)为mkJ·mol-1,H2O(l)为nkJ·mol-1。
反应的△H=产物的生成热之和---反应物的生成热之和
②几种化学键的键能数据如下:

上述反应中,△H=_______ kJ·mol-1,H-N键的键能为_______ kJ·mol-1。
(2)二氧化硫在一定条件下可以发生如下反应:
SO2(g)+NO2(g) SO3(g)+NO(g),△H= -42kJ·mol-1,在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
SO3(g)+NO(g),△H= -42kJ·mol-1,在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)=_____________________ ;
②实验丙中,达到平衡时,NO2的转化率为____________ ;
③由表中数据可推知,Tl______ T2(填“>”“<’’或“=”);
(3)对反应N2O4(g) 2NO2(g) △H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
2NO2(g) △H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是__________ 。
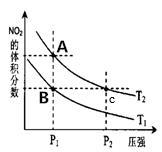
a.A、C两点的反应速率:A>C
b.A、C两点气体的颜色:A深,C浅
c.由状态A到状态B,可以用加热的方法
d.A、C两点的化学平衡常数:A="C"
(4)工业上,采用石墨、铁棒作为电极,电解除去废水中的CN-(N为-3价,下同),装置如图所示,通电过程中,阳极区两种离子的放电产物会进一步发生反应,其方程式为:C12+CNO-+OH-→□+Cl-+CO32-+H2O(未配平)。最终阴、阳两极均有无色无味气体产生。
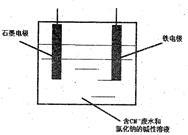
①铁电极应连接直流电源的____________ (填写电极名称)。
②上述反应方程式配平后“□”内应填写________ ;
③阳极上发生的电极反应为2Cl--2e-=Cl2↑和_______________ ;
(1)据报道,科学家新研发出一种常温下催化合成NH3的方法:2N2(g)+6H2O(l)=4NH3(g)+3O2(g)
已知如下信息:
①化合物的生成热可以表示其相对能量。化学上,规定标准状况下稳定单质的生成热为0。几种物质的生成热:NH3(g)为mkJ·mol-1,H2O(l)为nkJ·mol-1。
反应的△H=产物的生成热之和---反应物的生成热之和
②几种化学键的键能数据如下:

上述反应中,△H=
(2)二氧化硫在一定条件下可以发生如下反应:
SO2(g)+NO2(g)
 SO3(g)+NO(g),△H= -42kJ·mol-1,在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
SO3(g)+NO(g),△H= -42kJ·mol-1,在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| N(SO2) | N(NO2) | N(NO) | ||
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)=
②实验丙中,达到平衡时,NO2的转化率为
③由表中数据可推知,Tl
(3)对反应N2O4(g)
 2NO2(g) △H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
2NO2(g) △H>0 在温度为Tl、T2时平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
a.A、C两点的反应速率:A>C
b.A、C两点气体的颜色:A深,C浅
c.由状态A到状态B,可以用加热的方法
d.A、C两点的化学平衡常数:A="C"
(4)工业上,采用石墨、铁棒作为电极,电解除去废水中的CN-(N为-3价,下同),装置如图所示,通电过程中,阳极区两种离子的放电产物会进一步发生反应,其方程式为:C12+CNO-+OH-→□+Cl-+CO32-+H2O(未配平)。最终阴、阳两极均有无色无味气体产生。

①铁电极应连接直流电源的
②上述反应方程式配平后“□”内应填写
③阳极上发生的电极反应为2Cl--2e-=Cl2↑和
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】我国正式公布实现碳达峰、碳中和的时间和目标后,使含碳化合物的综合利用更受关注和重视。回答下列问题:
(1)一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变 废为宝,其反应机理如图所示,该反应的化学方程式为_______ ,反应过程中碳元素的化合价为-2价的中间体是_______ 。

(2)二氧化碳与氢气重整体系中涉及的主要反应如下:
Ⅰ.CO2 (g)+4H2 (g) CH4 (g)+2H2O(g) ΔH=-165kJ·mol-1
CH4 (g)+2H2O(g) ΔH=-165kJ·mol-1
Ⅱ.CO2 (g)+H2 (g) CO(g)+H2O(g) ΔH=+41kJ·mol-1
CO(g)+H2O(g) ΔH=+41kJ·mol-1
①二氧化碳与甲烷反应生成一氧化碳和氢气的热化学方程式为_______ ;恒温恒容密闭容器中进行该反应,下列事实能说明反应达到平衡状态的是_______ (填选 项字母)。
A.CO2与CH4的有效碰撞几率不变 B.相同时间内形成C-H键和 H-H 键的数目相等
C.混合气体的密度不再改变 D.氢原子数不再改变
②一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO 的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)=_______ mol·L-1·min-1;反应Ⅱ的平衡常数Kp=_______ (Kp是用分压表示的平衡常数)。
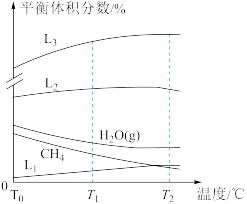
③向恒容密闭容器中以物质的量之比为1∶4充入CO2和H2,发生反应Ⅰ和反应Ⅱ,实验测得平衡体系中各组分的体积分数与温度的关系如图所示。其中表示H2的体积分数与温度关系的曲线为_______ (填“L1”“L2”或“L3”);T1℃之后,H2O(g)平衡体积分数随温度的变化程度小于CH4平衡体积分数随温度的变化程度,原因为_______ ; T1℃时CO 的平衡分压_______ (填“>”“<”或“=”) T2℃时 CO的平衡分压,理由为_______ 。
(1)一定条件下,Pd-Mg/SiO2催化剂可使CO2甲烷化从而变 废为宝,其反应机理如图所示,该反应的化学方程式为

(2)二氧化碳与氢气重整体系中涉及的主要反应如下:
Ⅰ.CO2 (g)+4H2 (g)
 CH4 (g)+2H2O(g) ΔH=-165kJ·mol-1
CH4 (g)+2H2O(g) ΔH=-165kJ·mol-1Ⅱ.CO2 (g)+H2 (g)
 CO(g)+H2O(g) ΔH=+41kJ·mol-1
CO(g)+H2O(g) ΔH=+41kJ·mol-1①二氧化碳与甲烷反应生成一氧化碳和氢气的热化学方程式为
A.CO2与CH4的有效碰撞几率不变 B.相同时间内形成C-H键和 H-H 键的数目相等
C.混合气体的密度不再改变 D.氢原子数不再改变
②一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO 的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)=
③向恒容密闭容器中以物质的量之比为1∶4充入CO2和H2,发生反应Ⅰ和反应Ⅱ,实验测得平衡体系中各组分的体积分数与温度的关系如图所示。其中表示H2的体积分数与温度关系的曲线为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.利用测压法在刚性反应器中研究 T℃ 时:
3NO2(g) 3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:
3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:
(1)该反应达到平衡后的熵值较平衡前______________ (填“增大”“减小”“不变”)。
(2)若降低反应温度,则平衡后体系压强 p____ 24.00 MPa(填“大于”“等于”“小于”),原因是_____________________________________________________________________ 。15min 时,反应物的转化率 α=__________ %
Ⅱ.一定条件下,在体积为 2 L 的密闭容器中发生反应:2NO2(g) 2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。
2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。

(1)要提高 NO2转化率,可采取的措施是________________ 、__________________ 。
(2)前2min内,以NO2表示该反应的化学反应速率为___________________ 。
(3)计算 A 点处v正/ v逆=_________________ (保留一位小数)。
3NO2(g)
 3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:
3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
(2)若降低反应温度,则平衡后体系压强 p
Ⅱ.一定条件下,在体积为 2 L 的密闭容器中发生反应:2NO2(g)
 2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。
2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。
(1)要提高 NO2转化率,可采取的措施是
(2)前2min内,以NO2表示该反应的化学反应速率为
(3)计算 A 点处v正/ v逆=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】为了提高资源利用率,减少环境污染,化工集团将钛厂、氯碱厂和甲醇厂组成产业链,如图所示。
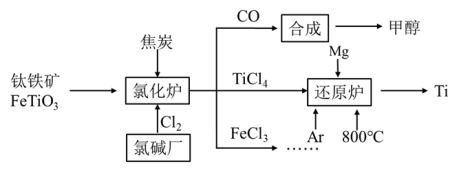
请填写下列空白:
(1)钛铁矿进入氯化炉前通常采取洗涤、粉碎、烘干、预热等物理方法处理,请从原理上解释粉碎的作用:_______________________________________ ;
(2)已知氯化炉中反应氯气和焦炭的理论用料物质的量比为7∶ 6,则氯化炉中的化学方程为_________________________________________________ 。
(3)TiCl4在常温下为无色液体,在军事上可作为人造烟雾剂,因为它在湿空气中会大冒白烟,水解生成二氧化钛的水凝胶TiO2·xH2O(也常写成H2TiO₃),工业上可也用此反应制备TiO2。请写出该水解方程式__________________________________________ (用TiO2·xH2O或H2TiO₃表示均可),工业上用TiCl4制备TiO2·xH2O时要加入大量的水,同时加热,目的是:______________________________
(4)Ar气通入还原炉中并不参与反应,通入Ar气的作用是__________________________
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为2CH3OH+3O2+4OH-= 2CO32-+6H2O,工作一段时间后,测得溶液的pH_____ (填“减小”、“增大”或“不变”)。
(6)FeCl3溶液可作为印刷电路铜板的腐蚀液,写出该反应的离子方程式_____________________________

请填写下列空白:
(1)钛铁矿进入氯化炉前通常采取洗涤、粉碎、烘干、预热等物理方法处理,请从原理上解释粉碎的作用:
(2)已知氯化炉中反应氯气和焦炭的理论用料物质的量比为7∶ 6,则氯化炉中的化学方程为
(3)TiCl4在常温下为无色液体,在军事上可作为人造烟雾剂,因为它在湿空气中会大冒白烟,水解生成二氧化钛的水凝胶TiO2·xH2O(也常写成H2TiO₃),工业上可也用此反应制备TiO2。请写出该水解方程式
(4)Ar气通入还原炉中并不参与反应,通入Ar气的作用是
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为2CH3OH+3O2+4OH-= 2CO32-+6H2O,工作一段时间后,测得溶液的pH
(6)FeCl3溶液可作为印刷电路铜板的腐蚀液,写出该反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ 甲醇水蒸气重整制氢
甲醇水蒸气重整制氢 系统简单,产物中
系统简单,产物中 含量高、CO含量低
含量高、CO含量低 会损坏燃料电池的交换膜
会损坏燃料电池的交换膜 ,是电动汽车氢氧燃料电池理想的氢源。反应如下:
,是电动汽车氢氧燃料电池理想的氢源。反应如下:
反应 主
主
反应 副
副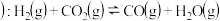
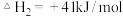
温度高于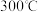 则会同时发生反应
则会同时发生反应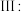
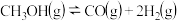

(1)计算反应III的
______________ 。
Ⅱ 太阳能电池可用作电解的电源
太阳能电池可用作电解的电源 如图
如图 。
。
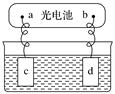
(2)若c、d均为惰性电极,电解质溶液为硫酸铜溶液,电解过程中,c极先无气体产生,后又生成气体,则c极为________ 极,在电解过程中,溶液的pH________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ,停止电解后,为使溶液恢复至原溶液应加入适量的
,停止电解后,为使溶液恢复至原溶液应加入适量的____________________ 。
(3)若c、d均为铜电极,电解质溶液为氯化钠溶液,则电解时,溶液中氯离子的物质的量将________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
(4)若用石墨、铁作电极材料,可组装成一个简易污水处理装置。其原理是加入试剂调节污水的pH在 。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的有色物质具有吸附性,吸附污物而沉积,起到凝聚净化作用。该装置中,阴极的电极反应为
。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的有色物质具有吸附性,吸附污物而沉积,起到凝聚净化作用。该装置中,阴极的电极反应为________ ;阳极区生成的有色物质是________ 。
Ⅲ 现有以下三种乙醇燃料电池
现有以下三种乙醇燃料电池 。
。
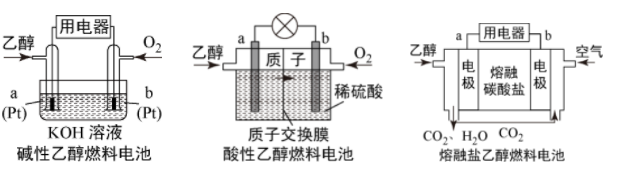
(5) 碱性乙醇燃料电池中,电极a上发生的电极反应式为
碱性乙醇燃料电池中,电极a上发生的电极反应式为___________________________ 。
 酸性乙醇燃料电池中,电极b上发生的电极反应式为
酸性乙醇燃料电池中,电极b上发生的电极反应式为___________________________ 。
 熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为
熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为__________ 。以此电源电解足量的硝酸银溶液,若阴极产物的质量为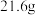 ,电解后溶液体积为2L,溶液的pH约为
,电解后溶液体积为2L,溶液的pH约为_____
 甲醇水蒸气重整制氢
甲醇水蒸气重整制氢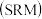 系统简单,产物中
系统简单,产物中 含量高、CO含量低
含量高、CO含量低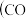 会损坏燃料电池的交换膜
会损坏燃料电池的交换膜 ,是电动汽车氢氧燃料电池理想的氢源。反应如下:
,是电动汽车氢氧燃料电池理想的氢源。反应如下: 反应
 主
主
反应
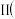 副
副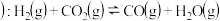
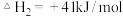
温度高于
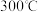 则会同时发生反应
则会同时发生反应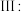
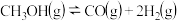

(1)计算反应III的

Ⅱ
 太阳能电池可用作电解的电源
太阳能电池可用作电解的电源 如图
如图 。
。
(2)若c、d均为惰性电极,电解质溶液为硫酸铜溶液,电解过程中,c极先无气体产生,后又生成气体,则c极为
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ,停止电解后,为使溶液恢复至原溶液应加入适量的
,停止电解后,为使溶液恢复至原溶液应加入适量的(3)若c、d均为铜电极,电解质溶液为氯化钠溶液,则电解时,溶液中氯离子的物质的量将
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。(4)若用石墨、铁作电极材料,可组装成一个简易污水处理装置。其原理是加入试剂调节污水的pH在
 。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的有色物质具有吸附性,吸附污物而沉积,起到凝聚净化作用。该装置中,阴极的电极反应为
。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的有色物质具有吸附性,吸附污物而沉积,起到凝聚净化作用。该装置中,阴极的电极反应为Ⅲ
 现有以下三种乙醇燃料电池
现有以下三种乙醇燃料电池 。
。
(5)
 碱性乙醇燃料电池中,电极a上发生的电极反应式为
碱性乙醇燃料电池中,电极a上发生的电极反应式为 酸性乙醇燃料电池中,电极b上发生的电极反应式为
酸性乙醇燃料电池中,电极b上发生的电极反应式为 熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为
熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电极b上发生的电极反应式为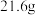 ,电解后溶液体积为2L,溶液的pH约为
,电解后溶液体积为2L,溶液的pH约为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】甲醇的燃点低,很容易着火,是发展前景很好的一种液体燃料。
(1)已知甲醇的燃烧热为726.5kJ/mol,则甲醇燃烧的热化学方程式为_________ .
(2)利用合成气主要成分为CO和H2)在催化剂的作用下合成甲醇,已知反应中有关物质的化学键键能数据如下表所示:
则: CO(g)+2H2(g)⇌CH3OH(g)△H=_________ kJ•mol-1,每消耗标准状况下8.96LCO时转移电子的物质的量是________ .
(3)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。如图是月前研究较多的一类固体氧化物燃料电池工作原理示意图。B极为电池____ 极,B极的电极反应式为____
(1)已知甲醇的燃烧热为726.5kJ/mol,则甲醇燃烧的热化学方程式为
(2)利用合成气主要成分为CO和H2)在催化剂的作用下合成甲醇,已知反应中有关物质的化学键键能数据如下表所示:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
则: CO(g)+2H2(g)⇌CH3OH(g)△H=
(3)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。如图是月前研究较多的一类固体氧化物燃料电池工作原理示意图。B极为电池

您最近一年使用:0次



