已知:①向MnO2固体中加入浓盐酸,加热后充分反应,产生黄绿色气体,②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③向KMnO4晶体滴加浓盐酸,产生黄绿色气体。下列判断正确的为( )
| A.实验②证明Fe2+既有氧化性又有还原性 |
| B.实验③生成的气体不能使湿润的淀粉KI试纸变蓝 |
| C.上述实验中,有三个氧化还原反应 |
| D.上述实验证明氧化性:MnO2>MnO4﹣>Cl2>Fe3+ |
更新时间:2020-01-08 16:30:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。在回收过程当中涉及到如下化学反应:
①SeO2+4KI+4HNO3→Se+2I2+4KNO3+2H2O;
②Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O。下列有关叙述不正确 的是
①SeO2+4KI+4HNO3→Se+2I2+4KNO3+2H2O;
②Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O。下列有关叙述
| A.反应①中每有0.6mol I2生成,转移电子数目为1.2NA |
| B.①中Se是还原产物,I2是氧化产物 |
| C.反应①中KI是氧化剂,SeO2是还原剂 |
| D.SeO2、H2SO4(浓)、I2的还原性由强到弱的顺序是H2SO4(浓)>SeO2>I2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在下列反应中,HNO3既表现出氧化性,又表现出还原性的是
| A.H2S+2HNO3=S↓+2NO2↑+2H2O |
| B.2HNO3+CuO=Cu(NO3)2+H2O |
| C.8HNO3+3Cu=2NO↑+2Cu(NO3)2+4H2O |
D.4HNO3 4NO2↑+O2↑+2H2O 4NO2↑+O2↑+2H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象和结论都正确且有相关性的是
| 选项 | 操作 | 现象 | 结论 |
| A | 在酸性H2O2溶液中滴加FeI2溶液 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| B | 在溴水中滴加适量植物油(无色) | 橙色溶液变无色,液体分层 | 植物油含有不饱和碳碳键 |
| C | 向紫色石蕊溶液中持续通入SO2 | 溶液由紫色变红色,最终变无色 | 酸性氧化物SO2有漂白性 |
| D | 在硫酸酸化的KMnO4溶液中加入Na2S溶液,再滴加BaCl2溶液 | 产生白色沉淀 |  将 将 氧化成 氧化成 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知 Cl-、Br-、I-、Fe2+、SO2均有还原性,在酸性溶液中还原能力的强弱顺序为: Cl-<Br-<Fe2+<I-<SO2,则下列反应不能发生的是
A.2Fe3++SO2 +2H2O═2Fe2++SO +4H+ +4H+ | B.6FeI2 +3Cl2═2FeCl3 +4FeI3 |
| C.I2+SO2+2H2O═H2SO4+2HI | D.2Fe2++Br2═2Fe3++2Br- |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物。其漂白原理可用下面的反应方程式表示:

下列说法正确的是

下列说法正确的是
| A.品红分子结构中,19个碳原子都可能在同一平面上 |
| B.SO2和Cl2分别使品红溶液褪色的原因可以用同一原理解释 |
| C.“无色化合物”分子中,19个碳原子都可能在同一平面上 |
| D.品红溶液中同时通入Cl2、SO2,漂白效果会更好 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验方法能达到实验目的的是
| A.用浓硫酸干燥氨气 |
| B.用乙醇萃取溴水中的溴单质 |
| C.通入氯气可除去FeCl3溶液中含有的FeCl2 |
| D.向蛋白质溶液中加入CuSO4溶液,出现沉淀,加水使蛋白质溶解 |
您最近半年使用:0次

 )因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下
)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下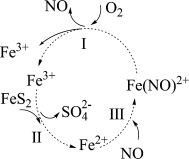
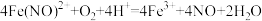
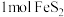 ,转移电子的物质的量为
,转移电子的物质的量为
 和
和 均作催化剂
均作催化剂 氧化
氧化 溶液制备
溶液制备 ,反应原理为:
,反应原理为: 。下列说法不正确的是
。下列说法不正确的是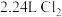 ,转移0.2mol电子
,转移0.2mol电子

