(1)FeS2(二硫化亚铁)不溶于水,可溶于适量的稀硝酸中,离子反应式如下,请配平此氧化还原反应方程式:_____ FeS2+_____H++_____N =______Fe2++______S+_____NO↑+______H2O。在上述氧化还原反应方程式中还原剂为
=______Fe2++______S+_____NO↑+______H2O。在上述氧化还原反应方程式中还原剂为_____________ 。
(2)为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,实验方案设计错误的是____________ (填字母)

A.④和⑤ B.只有③ C.③和④ D.①②③
(3)已知:氧化性Cl2>Br2>Fe3+,还原性Fe2+>Br->Cl-,则向1 L 0.2 mol·L-1的FeBr2溶液中通入标准状况下氯气2.24 L,被氧化的粒子是________ ,此反应的离子方程式:________ 。
 =______Fe2++______S+_____NO↑+______H2O。在上述氧化还原反应方程式中还原剂为
=______Fe2++______S+_____NO↑+______H2O。在上述氧化还原反应方程式中还原剂为(2)为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,实验方案设计错误的是

A.④和⑤ B.只有③ C.③和④ D.①②③
(3)已知:氧化性Cl2>Br2>Fe3+,还原性Fe2+>Br->Cl-,则向1 L 0.2 mol·L-1的FeBr2溶液中通入标准状况下氯气2.24 L,被氧化的粒子是
更新时间:2020-01-13 17:27:41
|
相似题推荐
【推荐1】填空题
(1)配平下面的方程式:_______ 。
_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2_______Cl2↑+_______H2O
指出上述反应中:_______ 是氧化剂,_______ 元素被氧化。此反应中,HCl表现的性质有_______ 性和_______ 性。
(2)根据反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是_______ 。
II.用双线桥表示该反应电子转移的方向和数目_______ 。
(1)配平下面的方程式:
_______KMnO4+_______HCl(浓)=_______KCl+_______MnCl2_______Cl2↑+_______H2O
指出上述反应中:
(2)根据反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是
II.用双线桥表示该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】ClO2气体是一种常用的消毒剂,我国从2000年起逐步用 ClO2代替氯气对饮用水进行消毒.
(1)消毒水时, ClO2还可将水中的 Fe2+、Mn2+ 等转化成Fe(OH)3 和 MnO2等难溶物除去,在这个过程中, Fe2+、Mn2+的化合价升高,说明 ClO2具有______ 性.
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:2KClO3+SO2==2ClO2+_____ 。
(3)使Cl2 和H2O(g) 通过灼热的炭层,生成HCl和CO2 ,写出化学方程式:_____________
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg/L之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2== S4O62-+2I-)
Ⅲ加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:
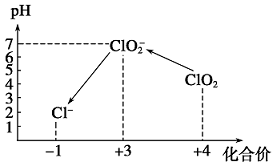
请回答:
①操作Ⅰ中反应的离子方程式是_____ 。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是_____ 。
③若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mol/L的Na2S2O3溶液10ml,则水样中ClO2的浓度是_____ mg/L。
(1)消毒水时, ClO2还可将水中的 Fe2+、Mn2+ 等转化成Fe(OH)3 和 MnO2等难溶物除去,在这个过程中, Fe2+、Mn2+的化合价升高,说明 ClO2具有
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:2KClO3+SO2==2ClO2+
(3)使Cl2 和H2O(g) 通过灼热的炭层,生成HCl和CO2 ,写出化学方程式:
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg/L之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2== S4O62-+2I-)
Ⅲ加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:

请回答:
①操作Ⅰ中反应的离子方程式是
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是
③若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mol/L的Na2S2O3溶液10ml,则水样中ClO2的浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)加入双氧水能提高软锰矿(主要成分是MnO2)的浸出率,锰转化成Mn2+。写出酸性条件下双氧水提高软锰矿浸出率的离子方程式:_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:___ 。
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:_____________ 。
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是_______ 。
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。
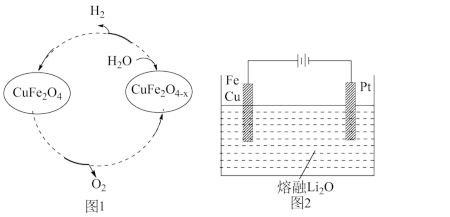
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_________ 。
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为_________ 。
(2)碘与氢氧化钠反应的生成物中含有IO3-,写出反应过程的离子方程式:
(3) 电镀污泥中的Cr2O3与加入的Na2CO3在空气中焙烧,Cr2O3被氧化为Na2CrO4,还有CO2逸出,写出该反应的化学方程式:
(4)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是
(5) 用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O也可制H2,其物质转化如图1所示。

①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为
②CuFe2O4可用电化学方法得到,其原理如图2所示,则阳极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据要求填空:
(1)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的化学方程式如下:
,反应的化学方程式如下:
 .
.
①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)______________________________________________________ 。
②该反应中,______ 是氧化剂,______ 是氧化产物.
③转移3mol电子,则所产生的氮气在标准状况下的体积为______ .
(2)铁是人类较早使用的金属之一.
①鉴别 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是______ .
②某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有
溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有 ,下列叙述正确的是
,下列叙述正确的是______ (填序号).
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有
(1)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的化学方程式如下:
,反应的化学方程式如下: .
.①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)
②该反应中,
③转移3mol电子,则所产生的氮气在标准状况下的体积为
(2)铁是人类较早使用的金属之一.
①鉴别
 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是②某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有
溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有 ,下列叙述正确的是
,下列叙述正确的是A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有

C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】金属和非金属被广泛应用于人类生产生活中。
(1)向一铝制易拉罐中充满 CO2后,再往罐中注入足量的质量分数为20%的NaOH溶液,立即严封罐口,不一会儿就发现易拉罐变瘪,再过一会易拉罐又鼓胀起来,解释上述实验现象,易拉罐又鼓胀起来的原因是_______ (用离子方程式表示)
(2)配制FeSO4溶液时需加入_______ 防止Fe2+被氧化,Fe(OH)2沉淀露置在空气中被氧化的化学反应方程式_______
(3)工业上将氯气通入石灰乳制取漂白粉,漂白粉的有效成分是_______ (填化学式),漂白粉露置于空气中后失效的化学方程式_______ 。
(4)向足量的铜粉与稀硝酸反应完的烧杯中滴加稀硫酸会继续产生气体,产生该气体的离子反应方程式为_______ 。
(5)实验室制备SO2的化学反应方程式_______ 。
(1)向一铝制易拉罐中充满 CO2后,再往罐中注入足量的质量分数为20%的NaOH溶液,立即严封罐口,不一会儿就发现易拉罐变瘪,再过一会易拉罐又鼓胀起来,解释上述实验现象,易拉罐又鼓胀起来的原因是
(2)配制FeSO4溶液时需加入
(3)工业上将氯气通入石灰乳制取漂白粉,漂白粉的有效成分是
(4)向足量的铜粉与稀硝酸反应完的烧杯中滴加稀硫酸会继续产生气体,产生该气体的离子反应方程式为
(5)实验室制备SO2的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】金属和非金属被广泛应用于人类生产生活中。
(1)Na的一种化合物常用于潜艇中处理CO2和供氧,它处理CO2的化学方程式为__________ 。
(2)检验FeSO4是否变质,可取少量溶液,加入几滴________________ 。
(3)工业上将氯气通入石灰乳制取漂白粉,漂白粉的有效成分是_______ (填化学式)。
(4)人们常常选用雕花玻璃装饰房间。在玻璃上雕花时发生的化学方程式是____________ 。
(5)许多人喜欢佩戴玉石饰品。玉石的主要成分基本都属于硅酸盐,例如和田玉(Ca2Mg5H2Si8O24)可表示为复杂氧化物形式2CaO·5MgO·8SiO2·H2O,则南阳玉(CaAl2Si2O8)表示为复杂氧化物形式是________ 。
(1)Na的一种化合物常用于潜艇中处理CO2和供氧,它处理CO2的化学方程式为
(2)检验FeSO4是否变质,可取少量溶液,加入几滴
(3)工业上将氯气通入石灰乳制取漂白粉,漂白粉的有效成分是
(4)人们常常选用雕花玻璃装饰房间。在玻璃上雕花时发生的化学方程式是
(5)许多人喜欢佩戴玉石饰品。玉石的主要成分基本都属于硅酸盐,例如和田玉(Ca2Mg5H2Si8O24)可表示为复杂氧化物形式2CaO·5MgO·8SiO2·H2O,则南阳玉(CaAl2Si2O8)表示为复杂氧化物形式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠( )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
①湿法制备:___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)
②干法制备: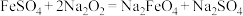
(1) 中Fe元素的化合价为
中Fe元素的化合价为___________ ,其在水溶液中的电离方程式为___________ 。
(2) 的电子式为
的电子式为___________ ,其与 反应的化学方程式为
反应的化学方程式为___________ 。
(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目___________ 。该反应每生成1 mol  ,转移的电子数为
,转移的电子数为___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:
___________  (选填“<”或“>”)。
(选填“<”或“>”)。
(5) 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂___________ 检验。 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是___________ 。
 )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:①湿法制备:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)②干法制备:
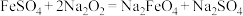
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)
 的电子式为
的电子式为 反应的化学方程式为
反应的化学方程式为(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目
 ,转移的电子数为
,转移的电子数为___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:

 (选填“<”或“>”)。
(选填“<”或“>”)。(5)
 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】近年来,我国的电子工业迅速发展,造成了大量的电路板蚀刻废液的产生和排放。蚀刻液主要有酸性的(HCl-H2O2)、传统的FeCl3型(HCl-FeCl3)等方法.蚀刻废液中含有大量的Cu2+,废液的回收利用可减少铜资源的流失.几种蚀刻废液的常用处理方法如下:
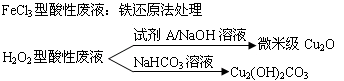
(1)FeCl3型酸性废液用还原法处理是利用Fe和Cl2分别作为还原剂和氧化剂,可回收铜并使蚀刻液再生。发生的主要化学反应有:Fe+Cu2+=Fe2++Cu、Fe+2H+=Fe2++H2↑,还有_______________ 、__________________ .(用离子方程式表示)。
(2)HCl-H2O2型蚀刻液蚀刻过程中发生的化学反应用化学方程式可表示为:__________ 。
(3)处理H2O2型酸性废液回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是____________________________________ 。

(1)FeCl3型酸性废液用还原法处理是利用Fe和Cl2分别作为还原剂和氧化剂,可回收铜并使蚀刻液再生。发生的主要化学反应有:Fe+Cu2+=Fe2++Cu、Fe+2H+=Fe2++H2↑,还有
(2)HCl-H2O2型蚀刻液蚀刻过程中发生的化学反应用化学方程式可表示为:
(3)处理H2O2型酸性废液回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列填空:
I.(1)呼吸面具中,Na2O2起反应的化学方程式为_____________ 。
(2)印刷电路板由高分子材料和铜箔复合而成,用FeCl3溶液刻制印刷电路时,发生的反应离子方程式为__________________ 。
(3)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度之比为3:2,则已反应的Fe3+和未反应的Fe3+的物质的量之比为_____________ 。
II.某一反应体系中有反应物和生成物共6种: HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe(SO4)3,反应前在溶液中滴加KSCN 溶液显红色,反应后红色消失。
(1)该反应中的还原剂是_____________ 。
(2)写出该反应的化学方程式_____________ 。
I.(1)呼吸面具中,Na2O2起反应的化学方程式为
(2)印刷电路板由高分子材料和铜箔复合而成,用FeCl3溶液刻制印刷电路时,发生的反应离子方程式为
(3)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度之比为3:2,则已反应的Fe3+和未反应的Fe3+的物质的量之比为
II.某一反应体系中有反应物和生成物共6种: HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe(SO4)3,反应前在溶液中滴加KSCN 溶液显红色,反应后红色消失。
(1)该反应中的还原剂是
(2)写出该反应的化学方程式
您最近一年使用:0次



