对于氨气的催化氧化反应:4NH3 +5O2 =4NO + 6H2O
(1)该反应中的还原剂是________ ,被还原的元素是_________ ;
(2)用单线桥标出该反应中电子转移的方向和数目;4NH3 +5O2 =4NO + 6H2O_________
(3)若反应转移了2mol电子,则产生的气体在标准状态下体积约为_______ 。
(1)该反应中的还原剂是
(2)用单线桥标出该反应中电子转移的方向和数目;4NH3 +5O2 =4NO + 6H2O
(3)若反应转移了2mol电子,则产生的气体在标准状态下体积约为
更新时间:2020-01-17 19:40:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】H2O2既可以作氧化剂,又可以作还原剂。现在H2O2溶液中加入用硫酸酸化的KMnO4溶液,紫红色的KMnO4溶液变成了无色溶液。该反应体系中共七种物质:O2、KMnO4、MnSO4、H2SO4、K2SO4、H2O、H2O2。
(1)请将以上反应物与生成物分别填入以下空格内___ 。

(2)该反应中的还原剂是__ (填化学式)被还原的元素是____ (填元素符号)。
(3)如反应中电子转移了0.5mol,则产生的气体在标准状况下的体积为__ L。
(4)+6价铬的化合物毒性较大,酸性溶液中常用NaHSO3将废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为___ 。
(1)请将以上反应物与生成物分别填入以下空格内

(2)该反应中的还原剂是
(3)如反应中电子转移了0.5mol,则产生的气体在标准状况下的体积为
(4)+6价铬的化合物毒性较大,酸性溶液中常用NaHSO3将废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)铝热反应在工业生产中的重要用途之一是_________________ ;用化学方程式表示出其中的原理________________________________________ (举一例)。铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸碱破坏,若将氧化铝与氢氧化钠溶液作用,反应的化学方程式为____________________________________ 。
(2)氯气用于漂白、消毒时,能起漂白、消毒作用的物质是____________ (写化学式)。缺铁性贫血患者应补充Fe元素,通常以硫酸亚铁的形式给药,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是_______________ 。
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是_________ 。(用化学方程式表示)。
(4)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C=2AlN+3CO。
①在化学方程式上标出该反应中电子转移的方向和数目。_________
②在该反应中,氧化剂是________________ ,氧化产物是_______________ 。
(1)铝热反应在工业生产中的重要用途之一是
(2)氯气用于漂白、消毒时,能起漂白、消毒作用的物质是
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是
(4)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C=2AlN+3CO。
①在化学方程式上标出该反应中电子转移的方向和数目。
②在该反应中,氧化剂是
您最近一年使用:0次
【推荐3】根据所学知识回答下列问题:
(1)在一定条件下,实现以下物质间转化,下列说法错误的是________
Ca CaO
CaO Ca(OH)2
Ca(OH)2 CaCO3
CaCO3 Ca(HCO3)2
Ca(HCO3)2
(2)在S2-、Fe2+、Cu2+、Na+中,既有氧化性又有还原性的是___________ 。
(3)某同学写出以下三个化学方程式(未配平)。
① NO + HNO3→ N2O3 + H2O
②N2O4 + H2O → HNO3 + HNO2
③ NH3 + NO → HNO2 + H2O
其中你认为一定不能实现的是___________ (填序号)。
(4)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①氧化剂是___________ (填化学式)。
②该反应中硝酸的作用是___________ (填字母)。
A.氧化剂 B.还原剂 C.酸性作用
③上述反应的离子方程式为___________ 。
④参加反应的HNO3与作为氧化剂的HNO3的个数之比为___________ 。
⑤配平反应________
___________ I2 + ___________ H2O +___________Cl2=___________ HIO3 + ___________ HCl
(1)在一定条件下,实现以下物质间转化,下列说法错误的是________
Ca
 CaO
CaO Ca(OH)2
Ca(OH)2 CaCO3
CaCO3 Ca(HCO3)2
Ca(HCO3)2| A.实现反应③只能向澄清石灰水中通入CO2气体 |
| B.反应①是氧化还原反应 |
| C.Ca→CaO的反应发生了化合反应 |
| D.CaCO3属于盐类物质,但是Ca(HCO3)2不属于盐类物质 |
(3)某同学写出以下三个化学方程式(未配平)。
① NO + HNO3→ N2O3 + H2O
②N2O4 + H2O → HNO3 + HNO2
③ NH3 + NO → HNO2 + H2O
其中你认为一定不能实现的是
(4)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①氧化剂是
②该反应中硝酸的作用是
A.氧化剂 B.还原剂 C.酸性作用
③上述反应的离子方程式为
④参加反应的HNO3与作为氧化剂的HNO3的个数之比为
⑤配平反应
___________ I2 + ___________ H2O +___________Cl2=___________ HIO3 + ___________ HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)在Fe2O3+3CO 2Fe+3CO2的反应中,氧化剂是
2Fe+3CO2的反应中,氧化剂是_________ ,被氧化的元素是_________ 。
(2)用单线桥表示上述反应的电子转移_________ 。
(3)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为_________ ;
②Ⅱ中铜丝上观察到的现象是_________ ;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_________ 。
(4)人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,在该氧化还原反应中,Fe2+是_________ 剂,Fe3+是_________ 产物。服用维生素C可以解毒。说明维生素C具有_________ 性(填“氧化”“还原”)。
(1)在Fe2O3+3CO
 2Fe+3CO2的反应中,氧化剂是
2Fe+3CO2的反应中,氧化剂是(2)用单线桥表示上述反应的电子转移
(3)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到的现象是
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(4)人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,在该氧化还原反应中,Fe2+是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。该反应中氧化剂是_____ ;若有0.75mol电子转移,则被还原的氧化剂粒子数为_______ (用NA表示)。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。维生素C的作用是_____ (氧化剂或还原剂)。
(3)下列方法中,可用来区分NaNO2和NaCl的是______ (填序号)。
A 焰色反应 B 分别滴加酸化的FeSO4溶液和KSCN溶液 C 分别滴加AgNO3溶液
| 药品 | NaNO2 (亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。该反应中氧化剂是
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。维生素C的作用是
(3)下列方法中,可用来区分NaNO2和NaCl的是
A 焰色反应 B 分别滴加酸化的FeSO4溶液和KSCN溶液 C 分别滴加AgNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)氯酸是一种强酸,氯酸的浓度超过40%就会迅速分解,反应的化学方程式为8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O。根据题意完成下列小题:
①在上述变化过程中,发生还原反应的过程是_____ →____ (填化学式)。
②该反应的氧化产物是________ (填化学式)。
(2)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3-、MnO4-、IO4-。有关反应的离子方程式为_____ 。
(3)工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
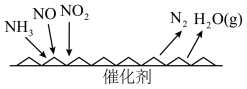
①由上图可知SCR技术中的氧化剂为_____________ 。
②用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:________ 。
①在上述变化过程中,发生还原反应的过程是
②该反应的氧化产物是
(2)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3-、MnO4-、IO4-。有关反应的离子方程式为
(3)工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

①由上图可知SCR技术中的氧化剂为
②用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:
您最近一年使用:0次



