某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:

(1)溶液Ⅰ中的溶质为_________ (填化学式,下同),溶液Ⅱ中的溶质为__________ 。
(2)上述第③步反应中,生成沉淀的离子方程式为____________ 。
(3)该合金中铝的含量为__________ 。

(1)溶液Ⅰ中的溶质为
(2)上述第③步反应中,生成沉淀的离子方程式为
(3)该合金中铝的含量为
更新时间:2020-01-30 19:38:18
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.写出下列物质在水溶液中的电离方程式。
(1) :
:___________ 。
(2)NaHCO3:___________ 。
II.
(3)写出用醋酸溶液与铁反应的离子方程式:___________ 。
(1)
 :
:(2)NaHCO3:
II.
(3)写出用醋酸溶液与铁反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】有以下几种物质:
A.硝酸钾固体 B.胆矾(CuSO4·5H2O)晶体 C.熔融的BaCl2 D.乙醇 E.干冰 F.铝 G.碳酸氢钠固体 H.硫酸钾溶液
按要求回答下列问题:
(1)①以上物质中能导电的是___________ (填字母,下同)。
②以上物质中属于电解质的是___________ 。
③以上物质中属于氧化物的是___________ 。
④以上物质中属于混合物的是___________ 。
(2)G溶于水的电离方程式为___________ ;C的水溶液与H反应的离子方程式为___________ 。
A.硝酸钾固体 B.胆矾(CuSO4·5H2O)晶体 C.熔融的BaCl2 D.乙醇 E.干冰 F.铝 G.碳酸氢钠固体 H.硫酸钾溶液
按要求回答下列问题:
(1)①以上物质中能导电的是
②以上物质中属于电解质的是
③以上物质中属于氧化物的是
④以上物质中属于混合物的是
(2)G溶于水的电离方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】图像分析是化学研究的一种重要的手段。某同学分析某无色透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH ,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
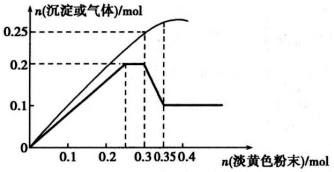
(1)根据图像所示,推测溶液中肯定有__ (写化学式)离子。
(2)过氧化钠物质的量在0.3~0.35mol时,粗的曲线出现下滑的现象,请用两个离子方程式解释该过程:__ 。
(3)溶液中Al3+、Mg2+、NH ,的物质的量之比为
,的物质的量之比为__ 。
 ,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
(1)根据图像所示,推测溶液中肯定有
(2)过氧化钠物质的量在0.3~0.35mol时,粗的曲线出现下滑的现象,请用两个离子方程式解释该过程:
(3)溶液中Al3+、Mg2+、NH
 ,的物质的量之比为
,的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氢氧化铝既可以与酸反应又可以与碱反应,是典型的两性氢氧化物。氢氧化铝和盐酸反应的化学方程式为______________________________________________ ;和NaOH溶液反应的化学方程式为______________________________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最活泼的非金属原子的原子结构示意图为____________ 。
(2)地壳中含量最多的金属元素是________________ (写元素符号) 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是________ ,碱性最强的是_________ ,呈两性的氢氧化物是____________ 。
(4)写出⑤与氢氧化钠反应的化学方程式:______________________ ,
写出⑤的氢氧化物与氢氧化钠溶液完全反应的离子方程式:___________________
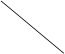 族 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)地壳中含量最多的金属元素是
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(4)写出⑤与氢氧化钠反应的化学方程式:
写出⑤的氢氧化物与氢氧化钠溶液完全反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】多元弱酸(或其酸酐)与更弱酸的盐溶液。如CO2通入到NaAlO2溶液中
(1)NaAlO2过量:_____________
(2)NaAlO2不足:_____________
(1)NaAlO2过量:
(2)NaAlO2不足:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列反应的离子方程式
(1)铝与氢氧化钾浓溶液反应______
(2)向偏铝酸钠溶液中通过量二氧化碳______
(3)向NaHSO4溶液中加入Ba(OH)2使溶液呈中性______
(4)过氧化钠与稀食盐水反应______
(1)铝与氢氧化钾浓溶液反应
(2)向偏铝酸钠溶液中通过量二氧化碳
(3)向NaHSO4溶液中加入Ba(OH)2使溶液呈中性
(4)过氧化钠与稀食盐水反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】实验中分离物质的方法常见的有:
A、过滤 ; B、蒸发; C、萃取; D、分液; E、蒸馏
海带中碘含量比较高,从海带提取碘的操作如下,除特殊说明外 ,请在空白处填上分离方法中的序号
(1)将干海带进行灼烧,海带灰中含有较多KI,将海带灰溶于水,然后______ 得到澄清滤液
(2)向上述滤液中加入硫酸和H2O2混合溶液,发生如下反应:H2O2+2I-+ 2H+ == 2H2O + I2 ,得到棕褐色含有单质碘的水溶液。该反应中H2O2是_______ 剂(本空填“氧化”或“还原”)。
(3)向上述碘的水溶液中加入适量CCl4, 振荡,静置,则I2会转入到CCl4层中,这个过程叫______ , 然后,再进行_________ ,将上下两层溶液分开。
(4) 上述操作后的______ (本空填“上”或“下”)层溶液为含有碘的CCl4溶液。利用CCl4的沸点较低,将混合物置于蒸馏烧瓶内进行________ 操作,可以粗略从CCl4溶液中分离出碘。
A、过滤 ; B、蒸发; C、萃取; D、分液; E、蒸馏
海带中碘含量比较高,从海带提取碘的操作如下,
(1)将干海带进行灼烧,海带灰中含有较多KI,将海带灰溶于水,然后
(2)向上述滤液中加入硫酸和H2O2混合溶液,发生如下反应:H2O2+2I-+ 2H+ == 2H2O + I2 ,得到棕褐色含有单质碘的水溶液。该反应中H2O2是
(3)向上述碘的水溶液中加入适量CCl4, 振荡,静置,则I2会转入到CCl4层中,这个过程叫
(4) 上述操作后的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氯化铁溶液常用作印刷电路铜板蚀刻液。请回答下列问题:
(1)常温下,若向某FeCl3溶液中加入一定量的澄清石灰水,调节溶液pH为4时,可得到红褐色沉淀,则溶液中Fe3+的物质的量浓度c(Fe3+)=_______ mol∙L−1。(已知:Ksp[(FeOH)3]=2.8×10−39)
(2)用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有Fe3+、Fe2+和Cu2+设计如图实验方案处理FeCl3溶液蚀刻铜板后的废液和资源回收。
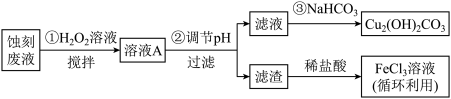
某些金属阳离子生成氢氧化物沉淀的pH如表:
①根据表中数据推测,步骤②应调节pH的范围是_______ ≤pH<_______ 。
②若步骤②中加入CuO调节pH,则反应的离子方程式为_______ 。
(1)常温下,若向某FeCl3溶液中加入一定量的澄清石灰水,调节溶液pH为4时,可得到红褐色沉淀,则溶液中Fe3+的物质的量浓度c(Fe3+)=
(2)用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有Fe3+、Fe2+和Cu2+设计如图实验方案处理FeCl3溶液蚀刻铜板后的废液和资源回收。

某些金属阳离子生成氢氧化物沉淀的pH如表:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
②若步骤②中加入CuO调节pH,则反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤
②不通入氨,冷却、加食盐,过滤。两种方法中___________ (填编号) 析出的氯化铵纯度更高
(2)氯气是一种黄绿色的有毒气体,工业上常用NH3来检验氯气是否发生泄漏,检验时若产生白烟,证明氯气发生了泄漏。则白烟的主要成份是___________ (填化学式)。写出产生白烟化学方程式___________ 。
(3)TiO2的熔沸点远高于CO2的原因是___________ ,MgTiO3的熔点高于BaTiO3的原因是___________ 。
(4)
②不通入氨,冷却、加食盐,过滤。两种方法中
(2)氯气是一种黄绿色的有毒气体,工业上常用NH3来检验氯气是否发生泄漏,检验时若产生白烟,证明氯气发生了泄漏。则白烟的主要成份是
(3)TiO2的熔沸点远高于CO2的原因是
(4)
| 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
| H2O(Br2) | ||
| 氯化镁溶液(氯化铁) |
您最近一年使用:0次




