人体中含有铁元素,+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。
(l)误服亚硝酸盐会使人中毒,是因为二价铁被___ (填“氧化”或“还原”)成三价铁,此 时服用维生素C可缓解亚硝酸盐中毒,维生素C在此过程中是作____ (填“氧化剂”或“还原剂”)。
(2)现有一瓶久置的FeSO4溶液,请设计实验检验其中是否含有Fe3+:___ 。Fe2+在空气中易发生氧化还原反应而变质,可加入____ (填化学式)来防止其变质,而又不会使溶液中有新的杂质。
(3)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaCIO氧化Fe(OH)3来制备,请配平反应方程式:____ ClO—+____ Fe(OH)3+____ OH— =____ FeO42—+_________ +____ Cl—。
(4)向制得的Na2FeO4溶液中加入适量的饱和KOH溶液会析出K2FeO4,写出该反应的化学方程式:____ 。
(l)误服亚硝酸盐会使人中毒,是因为二价铁被
(2)现有一瓶久置的FeSO4溶液,请设计实验检验其中是否含有Fe3+:
(3)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaCIO氧化Fe(OH)3来制备,请配平反应方程式:
(4)向制得的Na2FeO4溶液中加入适量的饱和KOH溶液会析出K2FeO4,写出该反应的化学方程式:
更新时间:2020-01-30 09:41:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】水中氰化物含量达0.lmg/L,就会使鱼类等生物死亡。因此对工业废水中氰化物含量控制很严,要求低于0.05mg/L。含氰废水可以在碱性条件下氧化处理,使CN-转变为CO2和N2。反应如下:
①CN-+ClO-=CNO-+Cl-
②2CNO-+4OH-+3C12=2CO2+N2+6Cl-+2H2O(CN-、CNO-中N的化合价为-3价)
(1)第二步反应中,___________ 元素被氧化,___________ 作氧化剂
(2)实际操作是向废水中加石灰乳并通入氯气。试填空:
①加入石灰乳的目的是___________
②通入过量氯气的目的是___________ (选填)
A.产生ClO- B.作氧化剂 C.漂白 D.杀菌
③加的是石灰乳而不是烧碱,主要是考虑到___________ 。
①CN-+ClO-=CNO-+Cl-
②2CNO-+4OH-+3C12=2CO2+N2+6Cl-+2H2O(CN-、CNO-中N的化合价为-3价)
(1)第二步反应中,
(2)实际操作是向废水中加石灰乳并通入氯气。试填空:
①加入石灰乳的目的是
②通入过量氯气的目的是
A.产生ClO- B.作氧化剂 C.漂白 D.杀菌
③加的是石灰乳而不是烧碱,主要是考虑到
您最近一年使用:0次
【推荐2】查资料得:HNO2是一种弱酸且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成 和Mn2+,请写出反应的离子方程式
和Mn2+,请写出反应的离子方程式_____________________________________ 。
(3)Fe与过量稀硫酸反应可制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________ (填序号)。
A.Cl2 B.Fe C.H2O2 D.HNO3
(4)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:_________
(_______)FeSO4+(________)K2O2→(_______)K2FeO4+(_______)K2O+(_______)K2SO4+(_______)O2↑
(5)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是___________________ 。
(1)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成
 和Mn2+,请写出反应的离子方程式
和Mn2+,请写出反应的离子方程式(3)Fe与过量稀硫酸反应可制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe C.H2O2 D.HNO3
(4)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
(_______)FeSO4+(________)K2O2→(_______)K2FeO4+(_______)K2O+(_______)K2SO4+(_______)O2↑
(5)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据题意写出对应的化学方程式或者离子方程式
(1)新房屋的墙壁(主要成份是熟石灰)经一段时间后“出水”且变得平滑僵硬(用化学方程式表示)__________________________________________________________________________ ;
(2)在充满CO2气体的铝制易拉罐中加入过量的浓NaOH溶液,立即把口封闭,发现易拉罐“咔咔”作响并且变瘪,随后易拉罐又会作响并鼓起来,写出易拉罐作响鼓起来的化学方程式_________________________
(3)Na2O2具有“魔术般”般的气体转换功能,常常被航天员或者宇航员用作供氧剂,写出相关的化学方程式_______________________________ 、________________________________
(4)实验室制备的酸性氯化亚铁溶液容易在空气中变质,写出相关的离子方程式______________________________________
(1)新房屋的墙壁(主要成份是熟石灰)经一段时间后“出水”且变得平滑僵硬(用化学方程式表示)
(2)在充满CO2气体的铝制易拉罐中加入过量的浓NaOH溶液,立即把口封闭,发现易拉罐“咔咔”作响并且变瘪,随后易拉罐又会作响并鼓起来,写出易拉罐作响鼓起来的化学方程式
(3)Na2O2具有“魔术般”般的气体转换功能,常常被航天员或者宇航员用作供氧剂,写出相关的化学方程式
(4)实验室制备的酸性氯化亚铁溶液容易在空气中变质,写出相关的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁是人体内一种微量元素,以 的形式存在。回答下列问题:
的形式存在。回答下列问题:
(1)下列微粒中,只有还原性的是___________ (填字母)。
A.Fe B. C.
C.
(2)维生素C可使食物中的 转化为
转化为 ,在此过程中
,在此过程中___________ 是还原剂
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸(HCl)反应的离子方程式___________ 。
 的形式存在。回答下列问题:
的形式存在。回答下列问题:(1)下列微粒中,只有还原性的是
A.Fe B.
 C.
C.
(2)维生素C可使食物中的
 转化为
转化为 ,在此过程中
,在此过程中(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸(HCl)反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】零价铁活化过硫酸盐耦合类芬顿体系可以产生强氧化性的羟基自由基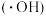 和硫酸根自由基(
和硫酸根自由基( ),被用于氧化降解废水中的抗生素。
),被用于氧化降解废水中的抗生素。
(1)该体系中产生自由基的机理如图所示。 在碱性溶液中可转化为
在碱性溶液中可转化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)为探究体系中 和
和 降解抗生素的能力,设计了自由基猝灭实验。
降解抗生素的能力,设计了自由基猝灭实验。 是
是 和
和 的猝灭剂,能与
的猝灭剂,能与 、
、 快速反应;
快速反应;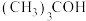 是
是 的猝灭剂,难和
的猝灭剂,难和 反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。
反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。 反应的原理是
反应的原理是 拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为
拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为___________ 。___________ 。
③降解抗生素的自由基主要是哪个,简述理由___________ 。
(3)探究 (PDS)的物质的量分数对抗生素去除率的影响。在
(PDS)的物质的量分数对抗生素去除率的影响。在 的废水中,PDS和H2O2总浓度为
的废水中,PDS和H2O2总浓度为 ,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。
,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。___________ 。
②PDS的物质的量分数降到0%时,抗生素残留率升高的原因是___________ 。
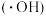 和硫酸根自由基(
和硫酸根自由基( ),被用于氧化降解废水中的抗生素。
),被用于氧化降解废水中的抗生素。(1)该体系中产生自由基的机理如图所示。

① 的结构为
的结构为 ,
, 的结构式为
的结构式为
 在碱性溶液中可转化为
在碱性溶液中可转化为 ,该反应的离子方程式为
,该反应的离子方程式为(2)为探究体系中
 和
和 降解抗生素的能力,设计了自由基猝灭实验。
降解抗生素的能力,设计了自由基猝灭实验。 是
是 和
和 的猝灭剂,能与
的猝灭剂,能与 、
、 快速反应;
快速反应;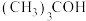 是
是 的猝灭剂,难和
的猝灭剂,难和 反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。
反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。
 反应的原理是
反应的原理是 拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为
拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为
③降解抗生素的自由基主要是哪个,简述理由
(3)探究
 (PDS)的物质的量分数对抗生素去除率的影响。在
(PDS)的物质的量分数对抗生素去除率的影响。在 的废水中,PDS和H2O2总浓度为
的废水中,PDS和H2O2总浓度为 ,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。
,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。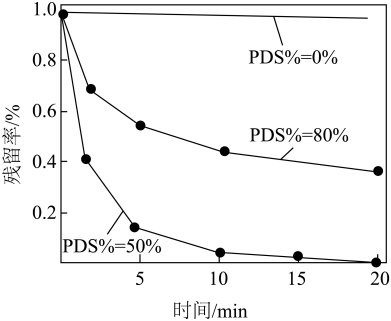
②PDS的物质的量分数降到0%时,抗生素残留率升高的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是________ 。
①赤铁矿的主要成分是Fe3O4
②向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液呈红色,说明红砖中含有氧化铁
③Fe2O3 FeCl3(aq)
FeCl3(aq) 无水FeCl3
无水FeCl3
④制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
⑤Fe3O4为红棕色晶体
⑥磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++ =3Fe3++NO↑+3H2O
=3Fe3++NO↑+3H2O
⑦氢氧化铁与HI溶液反应的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O
⑧Fe2O3不可与水反应得到Fe(OH)3,但能通过化合反应制取Fe(OH)3
⑨Fe(OH)2在空气中加热,可得到FeO
⑩图示装置 能较长时间观察到Fe(OH)2白色沉淀
能较长时间观察到Fe(OH)2白色沉淀
⑪FeO投入稀H2SO4和稀HNO3中均得到浅绿色溶液
⑫向一定量的Cu、Fe2O3的混合物中加入300mL1mol·L−1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为2.4g
①赤铁矿的主要成分是Fe3O4
②向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液呈红色,说明红砖中含有氧化铁
③Fe2O3
 FeCl3(aq)
FeCl3(aq) 无水FeCl3
无水FeCl3④制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
⑤Fe3O4为红棕色晶体
⑥磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++
 =3Fe3++NO↑+3H2O
=3Fe3++NO↑+3H2O⑦氢氧化铁与HI溶液反应的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O
⑧Fe2O3不可与水反应得到Fe(OH)3,但能通过化合反应制取Fe(OH)3
⑨Fe(OH)2在空气中加热,可得到FeO
⑩图示装置
 能较长时间观察到Fe(OH)2白色沉淀
能较长时间观察到Fe(OH)2白色沉淀⑪FeO投入稀H2SO4和稀HNO3中均得到浅绿色溶液
⑫向一定量的Cu、Fe2O3的混合物中加入300mL1mol·L−1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为2.4g
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:_________ 。
(2)现有一瓶胃舒平药片(复方氢氧化铝),请设计实验验证其主要成分。(写出实验步骤和实验现象):将药片碾碎,_______ 则说明其主要成分为氢氧化铝。
(3)自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:_______ 检验Fe3+常用的试剂除碱外,还可以用_______ (填化学式),现象是_______ 。
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)现有一瓶胃舒平药片(复方氢氧化铝),请设计实验验证其主要成分。(写出实验步骤和实验现象):将药片碾碎,
(3)自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:
您最近一年使用:0次

 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液 溶液褪色
溶液褪色

