根据下列问题,回答:
(1)金属钠投入到CuSO4溶液中所发生的化学反应方程式:_____________ ,__________________ ;
(2)在呼吸面具中,Na2O2起反应的化学方程式为:________________________ ,_____________ ;
(3)金属铝与氢氧化钠发生反应的离子反应方程式为_____________________ ;
(4)在MgCl2溶液中滴加少量的NaOH溶液,现象为__________________ ,继续加入过量的NaOH溶液,现象为_______________ ;在AlCl3溶液中滴加少量的NaOH溶液,现象为_______________ ,离子反应方程式为_________________ ,继续加入过量的NaOH溶液,现象为______________ ,离子反应方程式为____________ 。
(1)金属钠投入到CuSO4溶液中所发生的化学反应方程式:
(2)在呼吸面具中,Na2O2起反应的化学方程式为:
(3)金属铝与氢氧化钠发生反应的离子反应方程式为
(4)在MgCl2溶液中滴加少量的NaOH溶液,现象为
更新时间:2019-12-31 14:11:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】元素化合物在日常生活、化工生产和环境科学中有着重要的用途。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ 。
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:___________________________________________ 。
(3)当皮肤划破时可用FeCl3溶液应急止血,其主要作用是__________________ 。
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO + C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:
+ C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:__________ ,每生成1mol K2FeO4,转移的电子数是_________ 。
(5)合成氨及其相关工业中,部分物质间的转化关系如下:
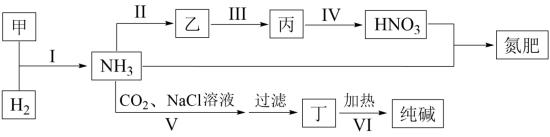
反应IV属于___________ 反应类型,氮肥主要成分的化学式为_______________ ,V的化学反应方程式为_________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)自然界中Cr主要以+3价和+6价形式存在。Cr2O
 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将Cr2O 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:(3)当皮肤划破时可用FeCl3溶液应急止血,其主要作用是
(4)高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式Fe(OH)3+ C1O-+ OH-→ FeO
 + C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:
+ C1-+ H2O(未配平),Fe(OH)3与 C1O-的计量数比为:(5)合成氨及其相关工业中,部分物质间的转化关系如下:

反应IV属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请用学过的知识分析其中的化学原理并写出化学方程式,属于离子反应的请写出离子方程式。
(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】_________________________________ 。
(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质__________________________ 。
(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸____________________ 、__________________ 。
(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用_______________ 。
(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:_____________
(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】
(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质
(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸
(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用
(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是______________ (写化学式)
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时)________________________________ 、_______________________________ 。
(3)烧碱、纯碱均可吸收CO2,当含0.1molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况。按吸收CO2由少到多的顺序,四种固体组成的化学式分别是:______ , ______ ,______ ,_________ 。
(1)从物质的分类角度看,不恰当的一种物质是
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时)
(3)烧碱、纯碱均可吸收CO2,当含0.1molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况。按吸收CO2由少到多的顺序,四种固体组成的化学式分别是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请根据所学知识,回答下列问题:
I.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)将Cu与稀硫酸混合,二者不能反应,滴入 后,溶液很快变成蓝色,该反应的化学方程式为
后,溶液很快变成蓝色,该反应的化学方程式为___________ 。
(3)利用 溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为___________ 。
(4)在潜水艇和消防员的呼吸面具中常装有 固体,工作时所发生的化学方程式为
固体,工作时所发生的化学方程式为___________ 、___________
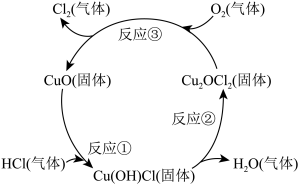
(5)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况___________ 。
I.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)将Cu与稀硫酸混合,二者不能反应,滴入
 后,溶液很快变成蓝色,该反应的化学方程式为
后,溶液很快变成蓝色,该反应的化学方程式为(3)利用
 溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为(4)在潜水艇和消防员的呼吸面具中常装有
 固体,工作时所发生的化学方程式为
固体,工作时所发生的化学方程式为(5)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.中国“奋斗号”载人潜水器在马里亚纳海沟成功坐底深度10909米,挑战了全球海洋最深处。国产新型钛合金、能源供给锂电池等功不可没。磷酸亚铁锂(LiFePO4)可作为锂电池的正极材料,请回答下列问题:
(1)潜水器外壳使用的钛合金
| A.耐高压 | B.耐腐蚀 | C.硬度小 | D.密度小 |
(2)磷酸亚铁锂(LiFePO4)中Fe的化合价为
(3)铁元素的相关信息如图所示,其相对原子质量是

(4)有关铁的性质,说法正确的是________。
| A.在空气中,加热Fe(OH)2可得FeO |
| B.一定条件下,Fe 能与水蒸气反应生成H2 |
| C.常温下,Fe与浓硫酸能反应生成SO2 |
| D.实验室用FeCl3溶液与NaOH溶液反应制备Fe(OH)3胶体 |
(5)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是________。
| A.Fe | B.FeO | C.Fe2O3 | D.Fe3O4 |
(6)要检验Fe3+,可选用的试剂是________。
| A.KSCN 溶液 | B.KMnO4溶液 | C.稀硝酸 | D.BaCl2溶液 |
Ⅱ.钠是生活中常见的金属元素,其多种化合物因其特殊性质在生活中都有广泛应用,例如,NaHCO3可用作食品膨松剂、Na2O2可用作供氧剂等。
(7)NaHCO3可用作膨松剂,原因是
(8)下列电离方程式正确的是________。
| A.NaOH = Na+ + O2-+ H+ | B.H2O = H+ + OH- |
C.HClO ClO-+ H+ ClO-+ H+ | D.CH3COONH4 CH3COO-+ NH4+ CH3COO-+ NH4+ |
(9)钠与滴加酚酞的水反应时
| A.钠浮在水面上 | B.钠熔成小球 | C.钠静止在水面上 | D.溶液变为红色 |
(10)Na2O2可作载人潜水器供氧剂,下列关于Na2O2说法正确的是________。
| A.只有离子键 | B.可在常温下由Na与O2反应制得 |
| C.Na2O2与H2O发生化合反应 | D.Na2O2与CO2反应有O2生成 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题
(1)实验室中将0.1 mol Na2O2加入水配制成溶液,写出相应的化学反应方程式___________ 。
(2)向(1)的溶液中加入一定量的NaHCO3固体,所得溶液中缓慢滴加一定浓度的盐酸,测得生成CO2的体积(已换算为标准状况下)与所加盐酸体积之间的关系如图所示。

①向(1)的溶液中加入的NaHCO3,固体质量为___________ g。
②滴加的盐酸物质的量浓度为___________ mol/L。
③图中:a=___________ 。
(1)实验室中将0.1 mol Na2O2加入水配制成溶液,写出相应的化学反应方程式
(2)向(1)的溶液中加入一定量的NaHCO3固体,所得溶液中缓慢滴加一定浓度的盐酸,测得生成CO2的体积(已换算为标准状况下)与所加盐酸体积之间的关系如图所示。

①向(1)的溶液中加入的NaHCO3,固体质量为
②滴加的盐酸物质的量浓度为
③图中:a=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】用一种试剂除去下列各物质中的杂质(括号内的物质),写出反应的离子方程式。
(1)CaCl2(HCl):离子方程式为___________ ;
(2)O2(CO2):离子方程式为___________ ;
(3)FeSO4溶液(CuSO4):离子方程式___________ ;
(4)Cu(MgO):离子方程式___________ 。
(1)CaCl2(HCl):离子方程式为
(2)O2(CO2):离子方程式为
(3)FeSO4溶液(CuSO4):离子方程式
(4)Cu(MgO):离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成。(提示:铝与氧化铁发生的反应称为铝热反应)
②另取20g A全部溶于0.15L 6.0mol·L-1盐酸中,得溶液C。
③将①中得到的单质B和溶液C反应,放出气体1.12L(标准状况下),同时生成溶液D,还残留固体B。
④用KSCN溶液检验时,溶液D不变色。
(1)反应①的产物中的单质B是________ 。
(2)②所发生各反应的化学方程式是:___________________________________ 。
(3)若溶液D的体积仍为0.15L,则该溶液中c(Mg2+)为________ ,c(Fe2+)为________ (保留小数点后两位)
①取适量A进行铝热反应,产物中有单质B生成。(提示:铝与氧化铁发生的反应称为铝热反应)
②另取20g A全部溶于0.15L 6.0mol·L-1盐酸中,得溶液C。
③将①中得到的单质B和溶液C反应,放出气体1.12L(标准状况下),同时生成溶液D,还残留固体B。
④用KSCN溶液检验时,溶液D不变色。
(1)反应①的产物中的单质B是
(2)②所发生各反应的化学方程式是:
(3)若溶液D的体积仍为0.15L,则该溶液中c(Mg2+)为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钠、铝、铁是三种重要的金属。
(1)将一小块金属钠投入水中,反应的离子方程式为___________ ;钠能与冷水剧烈反应而铁不能,证明金属活动性:钠___________ 铁(填“>”或“<”)。
(2)实验室常用Al2(SO4)3与氨水反应制备氢氧化铝,反应的离子方程式为___________
(3)某补铁剂(有效成分为FeSO4)因长期放置被氧化而失效,为检验其氧化产物(Fe3+),同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入___________ ,出现血红色溶液,证明氧化产物为Fe3+。
②乙同学另取少许溶液,加入淀粉-KI溶液,溶液变为___________ 色,证明氧化产物为Fe3+,该反应的离子方程式为___________ (已知:淀粉遇I2变蓝)。
(1)将一小块金属钠投入水中,反应的离子方程式为
(2)实验室常用Al2(SO4)3与氨水反应制备氢氧化铝,反应的离子方程式为
(3)某补铁剂(有效成分为FeSO4)因长期放置被氧化而失效,为检验其氧化产物(Fe3+),同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入
②乙同学另取少许溶液,加入淀粉-KI溶液,溶液变为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将一定量的钠铝合金置于水中,合金全部溶解,得到 20mL pH=14的溶液,然后用1 mol·L-1的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示:
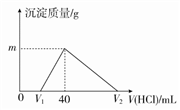
写出有关反应的化学方程式:
(1)______________________________ ;(2)______________________________ ;
(3)______________________________ ;(4)____________________________ ;
(5)____________________________ 。

写出有关反应的化学方程式:
(1)
(3)
(5)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,用化学方程式表示该反应的原理.___________________________________________
(2)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式
___________________________________
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,该反应的离子方程式为______________________ ;用此溶液进行以下反应,取少量溶液于一支试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为____________________ 。
(2)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,该反应的离子方程式为
您最近一年使用:0次



