(1)(填序号)下列实验操作或对实验事实的叙述正确的是______ 。
①用稀HNO3清洗做过银镜反应实验的试管
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
③用碱式滴定管量取20.00 mL 0.1000 mol·L-1KMnO4溶液
④用托盘天平称取10.50 g干燥的NaCl固体
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸
(2)为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试完成下列问题:
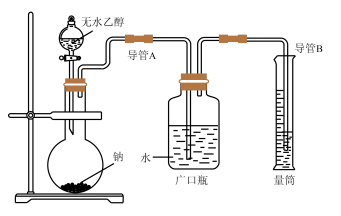
指出实验装置中的错误________ 。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将______ (填“偏大”、“偏小”或“不变”)。
③请指出能使该实验安全、顺利进行的关键实验步骤________________ (至少指出两个关键步骤)。
①用稀HNO3清洗做过银镜反应实验的试管
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
③用碱式滴定管量取20.00 mL 0.1000 mol·L-1KMnO4溶液
④用托盘天平称取10.50 g干燥的NaCl固体
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸
(2)为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试完成下列问题:

指出实验装置中的错误
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将
③请指出能使该实验安全、顺利进行的关键实验步骤
更新时间:2020-02-16 09:12:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】以下为五种有机物的有关信息,根据表中信息回答问题。
(1)A的官能团名称为_______ ,对A的描述正确的是_______ 。
①有毒 ②无色无味 ③密度比水小 ④与酸性高锰酸钾溶液反应使其褪色 ⑤在海带提碘实验中作萃取剂从碘水中提取碘单质 ⑥在热Cu丝作用下生成相对分子质量比它小2的有机物
A.①③⑤ B.②③④ C.③④⑥ D.④⑤⑥
为了鉴别A及A的一种常见同分异构体,某同学用一小块某元素的单质分别投入盛有这2种化合物的试管中,其中与该单质发生反应的化学方程式是_______ 。
(2)B的电子式为_______ ,实验室常用_______ 除去F中混有的少量B,发生了_______ 反应 填反应类型
填反应类型 。
。
(3)工业上,D来源于煤干馏后的液态产物煤焦油。D在浓硫酸、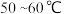 水浴中与浓硝酸发生取代反应,生成的有机物的结构简式为
水浴中与浓硝酸发生取代反应,生成的有机物的结构简式为_______ 。
(4)写出用 标记的A与不含
标记的A与不含 的E在一定条件下发生反应的化学方程式
的E在一定条件下发生反应的化学方程式 注明反应条件
注明反应条件
_______ 。
| A | B | D | E | F |
| ①由C、H、O三种元素组成的液体; ②医学上常用体积分数为  的该物质水溶液进行皮肤消毒。 的该物质水溶液进行皮肤消毒。 | 其产量用来衡量一个国家的石油化工水平。 | 比例模型为: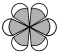 | ①可用于除水垢 ②在低于 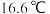 时,凝固成冰一样的晶体。 时,凝固成冰一样的晶体。 | 由5个原子组成的10个电子的共价分子。 |
①有毒 ②无色无味 ③密度比水小 ④与酸性高锰酸钾溶液反应使其褪色 ⑤在海带提碘实验中作萃取剂从碘水中提取碘单质 ⑥在热Cu丝作用下生成相对分子质量比它小2的有机物
A.①③⑤ B.②③④ C.③④⑥ D.④⑤⑥
为了鉴别A及A的一种常见同分异构体,某同学用一小块某元素的单质分别投入盛有这2种化合物的试管中,其中与该单质发生反应的化学方程式是
(2)B的电子式为
 填反应类型
填反应类型 。
。(3)工业上,D来源于煤干馏后的液态产物煤焦油。D在浓硫酸、
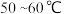 水浴中与浓硝酸发生取代反应,生成的有机物的结构简式为
水浴中与浓硝酸发生取代反应,生成的有机物的结构简式为(4)写出用
 标记的A与不含
标记的A与不含 的E在一定条件下发生反应的化学方程式
的E在一定条件下发生反应的化学方程式 注明反应条件
注明反应条件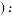
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I金属钠是中学化学常见的活泼金属,能与水,乙醇等物质反应。某同学按下图进行了实验,
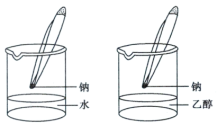
请回答下列问题:
(1)下列有关金属钠分别与水、乙醇反应的实验现象描述,正确的是_______ 。
A.反应开始时,金属钠浮在乙醇液面上
B.反应过程中,金属钠浮在水面上
C.钠与乙醇反应比钠与水反应更剧烈
D.钠与水反应比钠与乙醇反应更剧烈
(2)根据实验现象和金属钠的保存方法,下列推断合理的是_______ 。
A.乙醇分子中羟基上的氢原子与金属钠反应产生H2
B.乙醇分子中乙基上的氢原子与金属钠反应产生H2
C.乙醇分子中羟基上的氢原子比水分子中羟基上的氢原子活泼
D.乙醇分子中羟基上的氢原子比乙烷中氢原子活泼
II.下图为实验室制取乙酸乙酯的装置。请回答:
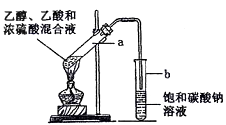
(1)检验该装置气密性的方法是_______ 。
(2)浓硫酸的作用是_______ 。
(3)下列有关该实验的说法中正确的是_______ 。
A.向a试管中加入碎资片,其作用是防止加热时液体暴沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明,密度比水大的油状液体
D.若原料为CH3COOH和CH3CH218OH,则乙酸乙酯中不含18O

请回答下列问题:
(1)下列有关金属钠分别与水、乙醇反应的实验现象描述,正确的是
A.反应开始时,金属钠浮在乙醇液面上
B.反应过程中,金属钠浮在水面上
C.钠与乙醇反应比钠与水反应更剧烈
D.钠与水反应比钠与乙醇反应更剧烈
(2)根据实验现象和金属钠的保存方法,下列推断合理的是
A.乙醇分子中羟基上的氢原子与金属钠反应产生H2
B.乙醇分子中乙基上的氢原子与金属钠反应产生H2
C.乙醇分子中羟基上的氢原子比水分子中羟基上的氢原子活泼
D.乙醇分子中羟基上的氢原子比乙烷中氢原子活泼
II.下图为实验室制取乙酸乙酯的装置。请回答:

(1)检验该装置气密性的方法是
(2)浓硫酸的作用是
(3)下列有关该实验的说法中正确的是
A.向a试管中加入碎资片,其作用是防止加热时液体暴沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明,密度比水大的油状液体
D.若原料为CH3COOH和CH3CH218OH,则乙酸乙酯中不含18O
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为研究乙醇结构及其部分的化学性质,进行实验。完成下列问题:
I.用如图装置来推测乙醇的结构式。
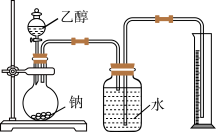
(1)实验中钠需要粉碎成很小的颗粒,其原因是_______ 。
(2)两次实验平均用乙醇1.15g,收集到H2体积平均为0.28L(换算成标准状态)。由实验数据可推测H2来自乙醇分子中_______ (填官能团名称)的氢原子。
(3)盛装乙醇的玻璃仪器是_______ 。
(4)写出乙醇与钠反应的化学方程式_______ 。
(5)实验测得量筒中水的体积是3.36L(标况下水是液态),则上述反应中转移______ mol电子。
II.利用下列装置进行乙醇的催化氧化实验,并检验其产物,其中C装置的试管中盛有无水乙醇。(固定和夹持装置已略去)
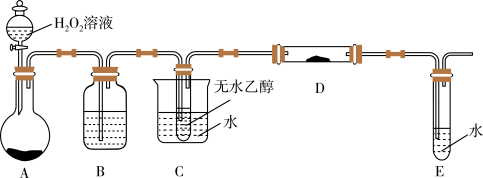
(6)装置A圆底烧瓶内的固体物质是____ ,B中的试剂是____ ;C的作用是____ 。
(7)本实验中需要加热的装置有_______ (填装置下的字母)。
(8)写出D处发生反应的化学方式_______ 。
(9)写出生成物E与银氨溶液反应的化学方程式_______ 。
(10)A中发生反应的化学方程式_______ 。
I.用如图装置来推测乙醇的结构式。

(1)实验中钠需要粉碎成很小的颗粒,其原因是
(2)两次实验平均用乙醇1.15g,收集到H2体积平均为0.28L(换算成标准状态)。由实验数据可推测H2来自乙醇分子中
(3)盛装乙醇的玻璃仪器是
(4)写出乙醇与钠反应的化学方程式
(5)实验测得量筒中水的体积是3.36L(标况下水是液态),则上述反应中转移
II.利用下列装置进行乙醇的催化氧化实验,并检验其产物,其中C装置的试管中盛有无水乙醇。(固定和夹持装置已略去)

(6)装置A圆底烧瓶内的固体物质是
(7)本实验中需要加热的装置有
(8)写出D处发生反应的化学方式
(9)写出生成物E与银氨溶液反应的化学方程式
(10)A中发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】ClO2作为一种广泛的消毒剂,它是一种易溶于水而难溶于有机溶剂的黄绿色气体,实验室用NaClO2与Cl2反应制得ClO2。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有液体(用于除去ClO2中的未反应的Cl2)。
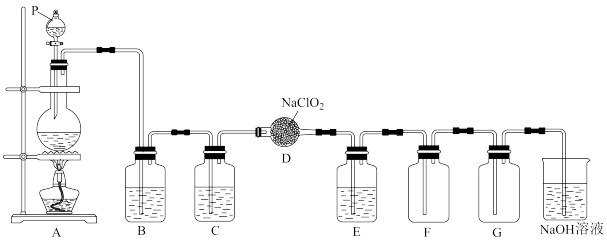
(1)仪器P的名称为____ 。
(2)请写出装置A圆底烧瓶内发生反应的化学方程式____ 。
(3)C装置中所盛试剂为____ ,G装置的作用____ 。
(4)装置D中发生反应的化学方程式为____ ,每生成1molClO2,转移的电子数目为____ 。

(1)仪器P的名称为
(2)请写出装置A圆底烧瓶内发生反应的化学方程式
(3)C装置中所盛试剂为
(4)装置D中发生反应的化学方程式为
您最近一年使用:0次
【推荐2】糠酸和糠醇均为重要的化工中间体,工业上可利用糠醛发生歧化反应制取这两种物质(该反应为强放热反应),反应原理如下:
2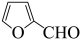 +OH-
+OH-
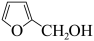 +
+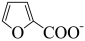 ΔH<0
ΔH<0
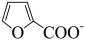 +H+
+H+
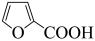
已知:①糠酸在热水中溶解度较大,微溶于冷水
②相关物质的熔点、沸点
实验步骤:
Ⅰ.向三颈烧瓶中加入8.2 mL密度为1.16 g/cm3新蒸馏的糠醛,通过仪器B向三颈烧瓶中缓慢滴加8 mL36%的NaOH溶液。
Ⅱ.通冷凝水,开启搅拌器,打开B的活塞,缓慢滴入8 mLNaOH溶液,保持反应温度8-12℃,回流20 min,得到粗产品。
Ⅲ.将粗产品倒入盛有10 mL水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取3次,分液得到水层和醚层。
Ⅳ.向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚和糠醇。
Ⅴ.向水层中分批滴加25%的盐酸,调至溶液的pH=3,冷却、结晶、抽滤、冷水洗涤、干燥,得到糠酸粗品。
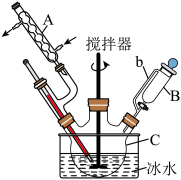
回答下列问题:
(1)仪器A的名称为___________ 。b管的作用是___________ 。
(2)该反应必须严格控制反应温度为8-12℃,实验中采用了哪些保障措施?___________ 、___________ 。
(3)步骤Ⅳ中分离乙醚和糠醇的实验操作为___________ 。
(4)步骤Ⅴ中洗涤粗糠酸用冷水的原因是___________ 。
(5)测定糠酸样品的纯度。准确称取1.120 g样品,配制成250 mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,加入几滴酚酞作指示剂,用0.0800 mol/LNaOH标准溶液滴定,平行测定3次,平均消耗标准溶液12.40 mL。
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为___________ 。
②产品的质量分数为___________ (保留4位有效数字)。
③该中和滴定实验中,若其他实验操作均正确,则下列实验操作造成测得的糠酸的纯度比实际偏高的是___________ (填标号)。
A.蒸馏水洗净后,未用NaOH标准溶液润洗碱式滴定管
B.锥形瓶内壁用蒸馏水洗净后,又用配制好的糠酸样品溶液润洗
C.在达到滴定终点时碱式滴定管出现了气泡
2
 +OH-
+OH-
 +
+ ΔH<0
ΔH<0 +H+
+H+

已知:①糠酸在热水中溶解度较大,微溶于冷水
②相关物质的熔点、沸点
| 糠酸 | 糠醛 | 糠醇 | 乙醚 | |
| 熔点(℃) | 133 | -38.7 | -29 | -116.2 |
| 沸点(℃) | 231 | 161.7 | 171 | -34.6 |
Ⅰ.向三颈烧瓶中加入8.2 mL密度为1.16 g/cm3新蒸馏的糠醛,通过仪器B向三颈烧瓶中缓慢滴加8 mL36%的NaOH溶液。
Ⅱ.通冷凝水,开启搅拌器,打开B的活塞,缓慢滴入8 mLNaOH溶液,保持反应温度8-12℃,回流20 min,得到粗产品。
Ⅲ.将粗产品倒入盛有10 mL水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取3次,分液得到水层和醚层。
Ⅳ.向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚和糠醇。
Ⅴ.向水层中分批滴加25%的盐酸,调至溶液的pH=3,冷却、结晶、抽滤、冷水洗涤、干燥,得到糠酸粗品。

回答下列问题:
(1)仪器A的名称为
(2)该反应必须严格控制反应温度为8-12℃,实验中采用了哪些保障措施?
(3)步骤Ⅳ中分离乙醚和糠醇的实验操作为
(4)步骤Ⅴ中洗涤粗糠酸用冷水的原因是
(5)测定糠酸样品的纯度。准确称取1.120 g样品,配制成250 mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,加入几滴酚酞作指示剂,用0.0800 mol/LNaOH标准溶液滴定,平行测定3次,平均消耗标准溶液12.40 mL。
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为
②产品的质量分数为
③该中和滴定实验中,若其他实验操作均正确,则下列实验操作造成测得的糠酸的纯度比实际偏高的是
A.蒸馏水洗净后,未用NaOH标准溶液润洗碱式滴定管
B.锥形瓶内壁用蒸馏水洗净后,又用配制好的糠酸样品溶液润洗
C.在达到滴定终点时碱式滴定管出现了气泡
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】苯甲酸乙酯是一种有芳香气味,无色液体,沸点为212℃,微溶于水,易溶于乙醚,常用作玫瑰、橙花、香石竹等化妆香精的调配,也用作纤维素脂、纤维素醚、树脂等的溶剂。
I.实验室利用苯甲酸、乙醇、环己烷和浓硫酸混合加热制备苯甲酸乙酯,此反应是个可逆反应,装置如图所示(省略了部分装置),
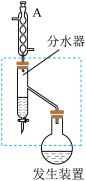
(1)写出实验室制备苯甲酸乙酯的化学方程式_______ 。
(2)加入的环己烷可提高苯甲酸乙酯产率的原因是_______ 。
(3)装置A的名称是_______ ,其作用是_______ 。
(4)及时打开分水器下端旋塞将水层移出反应体系的目的是_______ 。
II.从反应混合物中分离苯甲酸乙酯、苯甲酸和环己烷的流程如图。
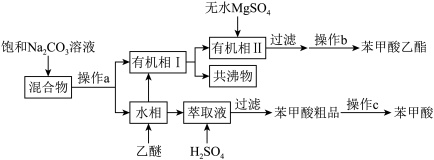
已知:环己烷沸点为80.8℃;乙醚的密度为0.834g/cm3,沸点34.5℃;乙醚-环己烷-水共沸物的沸点为62.1℃。
(5)向混合物中加入饱和Na2CO3溶液的目的是_______ 。
(6)操作b和操作c分别是_______ 、_______ 。
I.实验室利用苯甲酸、乙醇、环己烷和浓硫酸混合加热制备苯甲酸乙酯,此反应是个可逆反应,装置如图所示(省略了部分装置),

(1)写出实验室制备苯甲酸乙酯的化学方程式
(2)加入的环己烷可提高苯甲酸乙酯产率的原因是
(3)装置A的名称是
(4)及时打开分水器下端旋塞将水层移出反应体系的目的是
II.从反应混合物中分离苯甲酸乙酯、苯甲酸和环己烷的流程如图。

已知:环己烷沸点为80.8℃;乙醚的密度为0.834g/cm3,沸点34.5℃;乙醚-环己烷-水共沸物的沸点为62.1℃。
(5)向混合物中加入饱和Na2CO3溶液的目的是
(6)操作b和操作c分别是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】根据实验室中测定硫酸铜晶体(CuSO4·xH2O)结晶水含量的实验,填写下列空白:
(1)从下列仪器中选出所需仪器(用标号字母填写)_______ 。
A.电子天平 B.试管夹 C.酒精灯 D.蒸发皿 E.坩埚 F.石棉网
除上述仪器外,还需要的仪器是_______ 、_______ (任意填写二种)。
(2)某学生实验后得到表中数据:
①根据以上数据计算该硫酸铜晶体中结晶水x的值为_______ (精确到0.1)。
②该学生测定结果_______ (填“偏高”、“偏低”或“正确”)。
③从下列分析中选出该学生产生实验误差的原因可能是(填写字母)_______ 。
a.没有进行恒重操作
b.加热后在干燥器中冷却至室温后称量
c.加热固体到白色后,露置在空气中冷却
d.加热过程中晶体有少量溅失
(1)从下列仪器中选出所需仪器(用标号字母填写)
A.电子天平 B.试管夹 C.酒精灯 D.蒸发皿 E.坩埚 F.石棉网
除上述仪器外,还需要的仪器是
(2)某学生实验后得到表中数据:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
| 5.400 g | 7.900 g | 7.100 g |
②该学生测定结果
③从下列分析中选出该学生产生实验误差的原因可能是(填写字母)
a.没有进行恒重操作
b.加热后在干燥器中冷却至室温后称量
c.加热固体到白色后,露置在空气中冷却
d.加热过程中晶体有少量溅失
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氨基钠(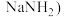 常用作有机合成的促进剂,是合成维生素A的原料.氨基钠的制备方法有高温加热法与低温催化法之分。如图装置(部分装置已省略)为低温催化法制备
常用作有机合成的促进剂,是合成维生素A的原料.氨基钠的制备方法有高温加热法与低温催化法之分。如图装置(部分装置已省略)为低温催化法制备
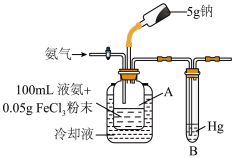
已知:①几种物质的熔沸点如表:
② 几乎不溶于液氨,易与水、氧气等反应.
几乎不溶于液氨,易与水、氧气等反应.
回答下列问题:
(1)制备
反应前先检查装置气密性确认不漏气,再通入氨气排尽密闭体系中空气,加入金属钠粒,搅拌,保持微沸下反应
①制备 的化学反应方程式为
的化学反应方程式为_______
②本实验温度为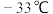 以下,冷却液选择液氨而不用液氯或液态二氧化硫,可能的原因是
以下,冷却液选择液氨而不用液氯或液态二氧化硫,可能的原因是_______ (任答一点)
③装置B的作用为_______
④反应得到粒状沉积物即 ,将混合体系在通风橱中,加热得固体产品
,将混合体系在通风橱中,加热得固体产品 。加热能够使产品与杂质分离的原因是
。加热能够使产品与杂质分离的原因是_______
⑤从整套装置的完整性分析,装置B的导气管末端出口最好应连接下列_______ (填字母代码)

(2)纯度分析
 在潮湿空气中易发生水解,产生两种碱性物质,假设
在潮湿空气中易发生水解,产生两种碱性物质,假设 是产品
是产品 的唯一杂质,可采用如下方法测定产品
的唯一杂质,可采用如下方法测定产品 纯度。准确称取
纯度。准确称取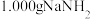 固体,溶于水,加热将产生的氨气蒸出,用蒸馏水吸收,得
固体,溶于水,加热将产生的氨气蒸出,用蒸馏水吸收,得 吸收液,取出
吸收液,取出 于锥形瓶中。再向瓶中加入1滴甲基橙,用
于锥形瓶中。再向瓶中加入1滴甲基橙,用 标准盐酸溶液滴定三次,滴定至终点时平均消耗盐酸溶液
标准盐酸溶液滴定三次,滴定至终点时平均消耗盐酸溶液 .则产品中的
.则产品中的 纯度为
纯度为_______
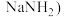 常用作有机合成的促进剂,是合成维生素A的原料.氨基钠的制备方法有高温加热法与低温催化法之分。如图装置(部分装置已省略)为低温催化法制备
常用作有机合成的促进剂,是合成维生素A的原料.氨基钠的制备方法有高温加热法与低温催化法之分。如图装置(部分装置已省略)为低温催化法制备
已知:①几种物质的熔沸点如表:
| 物质 |  |  |  |  | 备注 |
| 熔点/℃ | 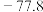 |  | 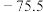 | 306 |  是一种共价化合物,受热易升华. 是一种共价化合物,受热易升华. |
| 沸点/℃ | 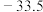 | 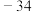 | 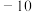 | 316 |
 几乎不溶于液氨,易与水、氧气等反应.
几乎不溶于液氨,易与水、氧气等反应.回答下列问题:
(1)制备
反应前先检查装置气密性确认不漏气,再通入氨气排尽密闭体系中空气,加入金属钠粒,搅拌,保持微沸下反应
①制备
 的化学反应方程式为
的化学反应方程式为②本实验温度为
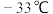 以下,冷却液选择液氨而不用液氯或液态二氧化硫,可能的原因是
以下,冷却液选择液氨而不用液氯或液态二氧化硫,可能的原因是③装置B的作用为
④反应得到粒状沉积物即
 ,将混合体系在通风橱中,加热得固体产品
,将混合体系在通风橱中,加热得固体产品 。加热能够使产品与杂质分离的原因是
。加热能够使产品与杂质分离的原因是⑤从整套装置的完整性分析,装置B的导气管末端出口最好应连接下列

(2)纯度分析
 在潮湿空气中易发生水解,产生两种碱性物质,假设
在潮湿空气中易发生水解,产生两种碱性物质,假设 是产品
是产品 的唯一杂质,可采用如下方法测定产品
的唯一杂质,可采用如下方法测定产品 纯度。准确称取
纯度。准确称取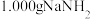 固体,溶于水,加热将产生的氨气蒸出,用蒸馏水吸收,得
固体,溶于水,加热将产生的氨气蒸出,用蒸馏水吸收,得 吸收液,取出
吸收液,取出 于锥形瓶中。再向瓶中加入1滴甲基橙,用
于锥形瓶中。再向瓶中加入1滴甲基橙,用 标准盐酸溶液滴定三次,滴定至终点时平均消耗盐酸溶液
标准盐酸溶液滴定三次,滴定至终点时平均消耗盐酸溶液 .则产品中的
.则产品中的 纯度为
纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下方案:①称取碱式碳酸镁样品mg;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用电子天平称量)。
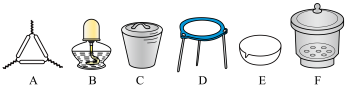
(1)下列仪器中,该方案不会用到的是________ 。___________ ;本实验至少需要称量___________ 次。
(3)某研究小组进行三次实验,数据记录如下:
通过计算,该样品中碱式碳酸镁的纯度为___________ 。(4MgCO3·Mg(OH)2·4H2O式量466;写出简要的步骤)
(4)有同学认为高温煅烧过程中会发生MgCO3+SiO2 MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?___________ (填“正确”或“错误”),请说明自己的理由:___________ 。
(1)下列仪器中,该方案不会用到的是
(3)某研究小组进行三次实验,数据记录如下:
| 样品质量/g | 剩余固体质量/g | |
| 实验1 | 18.000 | 8.000 |
| 实验2 | 18.000 | 8.020 |
| 实验3 | 18.000 | 7.980 |
(4)有同学认为高温煅烧过程中会发生MgCO3+SiO2
 MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室工作人员现用Na2CO3·10H2O晶体配制0.2mol·L-1的Na2CO3溶液480mL。请回答下列问题:
(1)配制溶液时下列仪器中:A.锥形瓶B.托盘天平C.烧杯D.胶头滴管E.药匙F.玻璃棒。不需要用到的是_______ (填序号),尚缺的玻璃仪器有_______ (写名称)。
(2)应称取Na2CO3·10H2O晶体的质量:_______ g。
(3)下列主要操作步骤的正确顺序是_______ (填序号)。
①称取一定质量的Na2CO3·10H2O晶体,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:
①Na2CO3·10H2O晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体(使用游码)
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有_______ (填序号,下同),无影响的有_______ 。
(5)配制过程中向容量瓶中转移溶液时不慎将溶液洒到容量瓶外面,此时的处理方法是:___ 。
(1)配制溶液时下列仪器中:A.锥形瓶B.托盘天平C.烧杯D.胶头滴管E.药匙F.玻璃棒。不需要用到的是
(2)应称取Na2CO3·10H2O晶体的质量:
(3)下列主要操作步骤的正确顺序是
①称取一定质量的Na2CO3·10H2O晶体,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:
①Na2CO3·10H2O晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体(使用游码)
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有
(5)配制过程中向容量瓶中转移溶液时不慎将溶液洒到容量瓶外面,此时的处理方法是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组需要0.1 mol·L−1 NaOH溶液480 mL。根据溶液的配制情况回答下列问题。
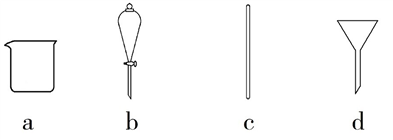
(1)根据计算,配制上述溶液用托盘天平称取的NaOH固体质量为_____ 克,在下图所示仪器中,配制上述溶液肯定不需要的是______ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是___________________ 。
(2)配制时,其正确的操作顺序是___________ (用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是_________ (填字母)。
A.②③④ B.②③ C.①②④ D.①②③④
(4)从该溶液中取出10 mL,其中NaOH的物质的量浓度为________ ,含NaOH的质量为________ 。
(5)下面操作造成所配NaOH溶液浓度偏高的是____________ (填字母)。
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
(1)根据计算,配制上述溶液用托盘天平称取的NaOH固体质量为

(2)配制时,其正确的操作顺序是
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是
A.②③④ B.②③ C.①②④ D.①②③④
(4)从该溶液中取出10 mL,其中NaOH的物质的量浓度为
(5)下面操作造成所配NaOH溶液浓度偏高的是
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
(1)配制100mL 0.10mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后) →洗涤(并将洗涤液移入容量瓶)→ → →将配制好的溶液倒入试剂瓶中,贴上标签。
②称量0.4g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、 。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①滴定达到终点的标志是 。
②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)
③如下图,排去碱式滴定管中气泡的方法应采用操作 ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 (多选扣分)。
A.滴定终点读数时俯视读数
B.碱式滴定管尖嘴部分有气泡,滴定后消失
C.锥形瓶水洗后未干燥
D.锥形瓶水洗后用待测稀盐酸溶液润洗
E.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
(1)配制100mL 0.10mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后) →洗涤(并将洗涤液移入容量瓶)→ → →将配制好的溶液倒入试剂瓶中,贴上标签。
②称量0.4g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、 。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)
③如下图,排去碱式滴定管中气泡的方法应采用操作 ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 (多选扣分)。
A.滴定终点读数时俯视读数
B.碱式滴定管尖嘴部分有气泡,滴定后消失
C.锥形瓶水洗后未干燥
D.锥形瓶水洗后用待测稀盐酸溶液润洗
E.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
您最近一年使用:0次



