.下列实验能达到预期目的的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入溴水,溴水褪色后加热观察能否恢复原色 | 验证SO2漂白的可逆性 |
| B | 将氯水加入淀粉KI溶液中 | 验证Cl的非金属性比I强 |
| C | 把铁块和铜块用导线连接插入浓硝酸中 | 组成原电池验证Fe比Cu活泼 |
| D | 加热氯化铵和碘单质的固体混合物 | 分离除去碘单质 |
| A.A | B.B | C.C | D.D |
9-10高三·重庆·阶段练习 查看更多[4]
(已下线)西南师大附中2010届高三第五次月考(理综)试题化学部分(已下线)2011届云南省德宏州潞西市芒市中学高三上学期期末统一测试化学试卷(已下线)2011届云南省芒市中学高三教学质检化学试卷(已下线)2012届山东省聊城市五校高三上学期期末联考化学试卷
更新时间:2012-02-13 20:36:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】氯气性质的微型实验装置如图所示。①是浓盐酸,⑥是高锰酸钾,②~⑤是滤纸条,依次滴有石蕊溶液、淀粉KI溶液、KBr溶液、含KSCN的FeCl2溶液,实验时滴入浓盐酸,下列说法不正确的是
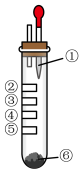

A.产生氯气的离子方程式为16H++10Cl-+2MnO =2Mn2++5Cl2↑+8H2O =2Mn2++5Cl2↑+8H2O |
| B.⑤处变红色,发生的反应为2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-=Fe(SCN)3 |
| C.②处先变红后褪色,说明氯气溶于水后,溶液有酸性和漂白性 |
| D.③处变蓝色,④处变橙色,说明氧化性:Cl2>Br2>I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】有一包白色粉末,可能含有NaCl、NaI、Mg(OH)2、Na2SO3中的一种或几种,为鉴定其成分,取少量样品进行以下实验:
(1)溶于足量水中,得到无色透明溶液,但仍有部分固体未溶解。
(2)取①的上层清液,滴加少量新制氯水,再加入CCl4,振荡,静置,CCl4层呈无色。
(3)取②反应后的上层清液,滴加BaCl2溶液,有白色沉淀生成。
(4)另取②反应后的上层清液,加入过量的AgNO3溶液和稀硝酸,有白色沉淀生成。
有关白色粉末成分的推断正确的是
(1)溶于足量水中,得到无色透明溶液,但仍有部分固体未溶解。
(2)取①的上层清液,滴加少量新制氯水,再加入CCl4,振荡,静置,CCl4层呈无色。
(3)取②反应后的上层清液,滴加BaCl2溶液,有白色沉淀生成。
(4)另取②反应后的上层清液,加入过量的AgNO3溶液和稀硝酸,有白色沉淀生成。
有关白色粉末成分的推断正确的是
| A.白色粉末中一定含有Mg(OH)2、Na2SO3和NaCl,一定不含有NaI |
| B.白色粉末中一定含有Mg(OH)2、Na2SO3,一定不含有NaI,可能含有NaCl |
| C.白色粉末中一定含有Mg(OH)2、Na2SO3,可能含有NaCl和NaI |
| D.白色粉末中一定含有Mg(OH)2,可能含有Na2SO3、NaCl,一定不含有NaI |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列离子方程式书写正确的是
A.向Na2SiO3溶液中通入过量CO2:Na2SiO3+2CO2+2H2O=H2SiO3↓+2HCO +2Na+ +2Na+ |
| B.向CaCl2溶液中通入CO2:Ca2+ + CO2 + H2O = CaCO3↓ + 2H+ |
C.用Na2SO3溶液吸收少量Cl2:3SO + Cl2 + H2O = 2HSO + Cl2 + H2O = 2HSO + 2Cl- +SO + 2Cl- +SO |
| D.向CH3COOH溶液中加氨水:CH3COOH + OH- = CH3COO- + H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是


| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5mol Na2O2,转移电子数为2NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是
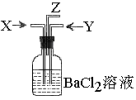

| A.洗气瓶中产生的沉淀是碳酸钡 | B.在Z导管出来的气体中无二氧化碳 |
| C.洗气瓶中产生的沉淀是亚硫酸钡 | D.在Z导管口有红棕色气体出现 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示电池是一种新型储氢材料—镍电池(MHn—Ni),(MHn中金属和氢都为 0 价)。下列有关说法不正确的是
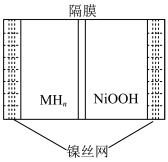

| A.放电时正极反应为 NiOOH+H2O+e-→Ni(OH)2+OH- |
| B.电池的电解液可为KOH 溶液 |
| C.充电时阴极反应为 MHn+nOH--e-→nH2O+M |
| D.MHn 是一类储氢材料,n 越大,电池的比能量越高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如下图所示,把锌片和铜片用导线相连后插入装有稀硫酸溶液的烧杯中构成原电池。下列叙述正确的是


| A.Zn是负极,发生还原反应 |
| B.电流从锌片流向铜片 |
| C.一段时间后,铜片质量减轻 |
| D.该装置将化学能转变为电能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用下列实验装置进行相应实验,不能达到实验目的的是
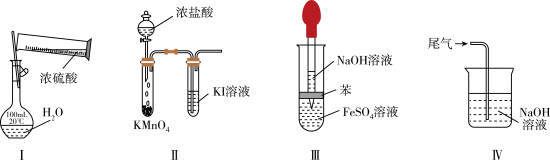

| A.实验Ⅰ:配制 100 mL 0.100 mol·L1稀硫酸 |
| B.实验Ⅱ:比较 KMnO4、Cl2、I2的氧化性强弱 |
| C.实验 III:制取并观察 Fe(OH)2沉淀 |
| D.实验Ⅳ:NO2尾气处理 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
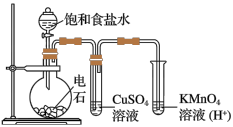

| A.将生成的气体直接通入到溴水中,溴水褪色,说明有乙炔生成 |
| B.酸性KMnO4溶液褪色,说明乙炔具有还原性 |
| C.逐滴加入饱和食盐水可控制生成乙炔的速率 |
| D.将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高 |
您最近一年使用:0次


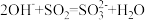


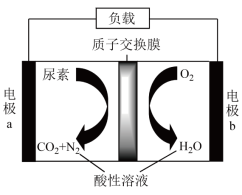
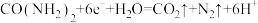
 ,电路中通过6 mol电子
,电路中通过6 mol电子

