(1)实验测得16g甲醇[CH3OH(l)]在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇燃烧热的热化学方程式:_______________________ .
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程.已知反应:N2(g)+3H2(g)⇌2NH3(g)△H=a kJ•mol﹣1.有关键能数据如表:
试根据表中所列键能数据估算a的数值_______________ .
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.已知:
C(s,石墨)+O2(g)═CO2(g) △H1=﹣393.5kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l) △H2=﹣571.6kJ•mol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l) △H3=﹣2599kJ•mol﹣1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的反应热为:△H=____________________ .
(4)在微生物作用下,NH4+经过两步反应被氧化成NO3﹣。两步反应的能量变化示意图如图:
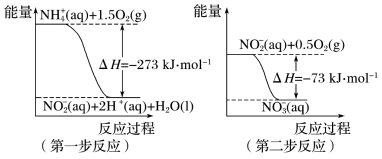
第一步反应是________ 反应(填“放热”或“吸热”),原因是_________________________
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程.已知反应:N2(g)+3H2(g)⇌2NH3(g)△H=a kJ•mol﹣1.有关键能数据如表:
| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
试根据表中所列键能数据估算a的数值
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.已知:
C(s,石墨)+O2(g)═CO2(g) △H1=﹣393.5kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l) △H2=﹣571.6kJ•mol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l) △H3=﹣2599kJ•mol﹣1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的反应热为:△H=
(4)在微生物作用下,NH4+经过两步反应被氧化成NO3﹣。两步反应的能量变化示意图如图:

第一步反应是
更新时间:2020-02-19 16:39:52
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】I、已知下列热化学方程式:
①2H2O(l)=2H2(g)+O2(g)△H=+570kJ/mol
②H2(g)+ O2(g)=H2O(l)△H=-285.6kJ/mol
O2(g)=H2O(l)△H=-285.6kJ/mol
③C(s)+ O2(g)=CO (g) △H=—110.5KJ/moL
O2(g)=CO (g) △H=—110.5KJ/moL
④C(s)+O2(g)=CO2(g) △H=—393.5KJ/moL。回答下列各问:
(1)上述反应中属于吸热反应的是_________________________ (填写对应序号)。
(2)H2的燃烧热△H=___ kJ/mol,C的燃烧热△H=_______ kJ/mol。
(3)燃烧10gH2生成液态水,放出的热量为____________ kJ。
(4)CO的燃烧热△H=__________ kJ/mol
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(5)图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______________________ 。
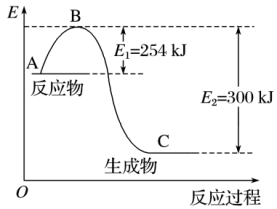
(6)该反应通常用铁触媒作催化剂,加铁触媒会使△H______ (填“变大”、“变小”或“不变”)
(7)若已知下列数据:
试根据表中及图中数据计算N—H的键能为_______ kJ/mol。
①2H2O(l)=2H2(g)+O2(g)△H=+570kJ/mol
②H2(g)+
 O2(g)=H2O(l)△H=-285.6kJ/mol
O2(g)=H2O(l)△H=-285.6kJ/mol ③C(s)+
 O2(g)=CO (g) △H=—110.5KJ/moL
O2(g)=CO (g) △H=—110.5KJ/moL ④C(s)+O2(g)=CO2(g) △H=—393.5KJ/moL。回答下列各问:
(1)上述反应中属于吸热反应的是
(2)H2的燃烧热△H=
(3)燃烧10gH2生成液态水,放出的热量为
(4)CO的燃烧热△H=
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(5)图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:

(6)该反应通常用铁触媒作催化剂,加铁触媒会使△H
(7)若已知下列数据:
| 化学键 | H—H | N≡N |
| 键能 (kJ/mol) | 435 | 943 |
试根据表中及图中数据计算N—H的键能为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在α-Fe(Ⅲ)铁原子簇表面,以N2和H2为原料合成氨的反应机理如下:
①H2(g)=2H(g),∆H1
②N2(g)+2H(g) 2(NH)(g),∆H2
2(NH)(g),∆H2
③(NH)(g)+H(g) (NH2)(g),∆H3
(NH2)(g),∆H3
④(NH2)(g)+H(g) NH3(g),∆H4
NH3(g),∆H4
总反应:N2(g)+3H2(g) 2NH3(g),∆H。则∆H4=
2NH3(g),∆H。则∆H4=___________ (用含∆H1、∆H2、∆H3、∆H的式子表示)。
①H2(g)=2H(g),∆H1
②N2(g)+2H(g)
 2(NH)(g),∆H2
2(NH)(g),∆H2③(NH)(g)+H(g)
 (NH2)(g),∆H3
(NH2)(g),∆H3④(NH2)(g)+H(g)
 NH3(g),∆H4
NH3(g),∆H4总反应:N2(g)+3H2(g)
 2NH3(g),∆H。则∆H4=
2NH3(g),∆H。则∆H4=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物的转化是资源利用和环境保护的重要研究课题。
(1)合成氨工业是最基本的无机化工之一,氨是化肥工业和基本有机化工的主要原料。合成氨反应中有关化学键键能数据如下表:
①已知:合成氨反应:N2(g)+3H2(g) 2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
 N2(g)+
N2(g)+ H2(g)的活化能Ea=
H2(g)的活化能Ea=_____ 。
②图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据如图中a点数据计算N2的平衡体积分数:_____ (保留3位有效数字)。
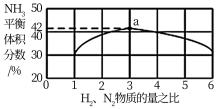
③依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,N2物质的量变化的曲线示意图_____ 。
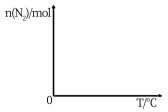
(2)选择性催化还原脱硝技术(SCR)是目前较成熟的烟气脱硝技术,该技术是指在温度300~420℃之间和催化剂条件下,用还原剂(如NH3)选择性地与NOx反应。
①SCR脱硝技术中发生的主要反应为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比
4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比 会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当
会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当 >1.0时,烟气中NO浓度反而增大,主要原因是
>1.0时,烟气中NO浓度反而增大,主要原因是_____ 。
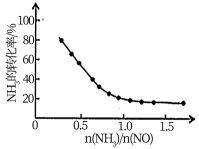
②碱性溶液处理烟气中的氮氧化物也是一种脱硝的方法,写出NO2被Na2CO3溶液吸收生成三种盐的化学反应方程式_____ 。
(1)合成氨工业是最基本的无机化工之一,氨是化肥工业和基本有机化工的主要原料。合成氨反应中有关化学键键能数据如下表:
| 化学键 | H—H | N≡N | N—H |
| E/kJ•mol-1 | 436 | 946 | 391 |
①已知:合成氨反应:N2(g)+3H2(g)
 2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
 N2(g)+
N2(g)+ H2(g)的活化能Ea=
H2(g)的活化能Ea=②图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据如图中a点数据计算N2的平衡体积分数:

③依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,N2物质的量变化的曲线示意图

(2)选择性催化还原脱硝技术(SCR)是目前较成熟的烟气脱硝技术,该技术是指在温度300~420℃之间和催化剂条件下,用还原剂(如NH3)选择性地与NOx反应。
①SCR脱硝技术中发生的主要反应为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比
4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比 会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当
会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当 >1.0时,烟气中NO浓度反而增大,主要原因是
>1.0时,烟气中NO浓度反而增大,主要原因是
②碱性溶液处理烟气中的氮氧化物也是一种脱硝的方法,写出NO2被Na2CO3溶液吸收生成三种盐的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1)①写出高温结构陶瓷氮化硅的化学式_______ ;
②写出硬脂酸甘油酯的结构简式_______ ;
(2)已知NaCN中C、N原子最外层均满足8电子结构,写出NaCN的电子式_______ 。
(3)甲醇的标准燃烧热为726.5kJ/mol,写出甲醇燃烧的热化学方程式_______ 。
(1)①写出高温结构陶瓷氮化硅的化学式
②写出硬脂酸甘油酯的结构简式
(2)已知NaCN中C、N原子最外层均满足8电子结构,写出NaCN的电子式
(3)甲醇的标准燃烧热为726.5kJ/mol,写出甲醇燃烧的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:_____________________________________ 。

(2)观察图a和图b,根据盖斯定律,写出ΔH1、ΔH2、ΔH3、ΔH4、ΔH5和ΔH6的关系。
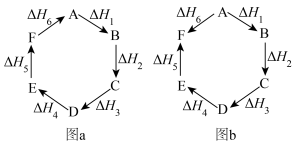
图a:__________________________________________________________ ;
图b:__________________________________________________________ 。

(2)观察图a和图b,根据盖斯定律,写出ΔH1、ΔH2、ΔH3、ΔH4、ΔH5和ΔH6的关系。

图a:
图b:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢能是一种无污染的能源,随着氢气需求的不断增长,制氢技术在不断进步。
(1)甲烷水蒸气重整制氢: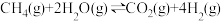

已知:a.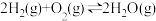
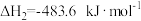 ;
;
b.
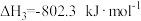 。
。
①
_______  ,为了得到更多的
,为了得到更多的 ,一般采用的反应条件是
,一般采用的反应条件是_______ (填“高温”、“低温”或“常温”)。
②工业上甲烷水蒸气重整制氢的过程中,经常加入 吸附剂
吸附剂 强化[
强化[
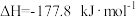 ],相比于甲烷水蒸气重整,吸附强化甲烷水蒸气重整的优点有
],相比于甲烷水蒸气重整,吸附强化甲烷水蒸气重整的优点有_______ 、_______ 。
(2)甲醇水蒸气重整制氢:甲醇和水蒸气重整时,未使用催化剂和使用催化剂两种反应进程中能量的变化曲线a和b如图所示。

①b过程第Ⅰ步反应和第Ⅱ步反应分别为_______ (填“放热反应”或“吸热反应”,下同)、_______ ,第Ⅰ步反应与第Ⅱ步反应的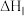
_______ (填“>”、“<”或“=”)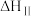 。
。
②甲醇和水蒸气重整时发生反应的热化学方程式为_______ 。
(1)甲烷水蒸气重整制氢:
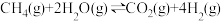

已知:a.
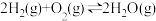
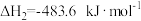 ;
;b.

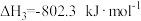 。
。①

 ,为了得到更多的
,为了得到更多的 ,一般采用的反应条件是
,一般采用的反应条件是②工业上甲烷水蒸气重整制氢的过程中,经常加入
 吸附剂
吸附剂 强化[
强化[
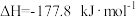 ],相比于甲烷水蒸气重整,吸附强化甲烷水蒸气重整的优点有
],相比于甲烷水蒸气重整,吸附强化甲烷水蒸气重整的优点有(2)甲醇水蒸气重整制氢:甲醇和水蒸气重整时,未使用催化剂和使用催化剂两种反应进程中能量的变化曲线a和b如图所示。

①b过程第Ⅰ步反应和第Ⅱ步反应分别为
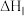
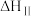 。
。②甲醇和水蒸气重整时发生反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】为了合理利用化学能,确保安全生产,进行化工设计时需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常可以通过实验进行测定,也可通过理论进行推算。
(1)实验测得,5 g液态甲醇( )在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,则1 mol液态甲醇充分燃烧生成二氧化碳气体和液态水的热化学方程式为
)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,则1 mol液态甲醇充分燃烧生成二氧化碳气体和液态水的热化学方程式为______ 。
(2)现有如下两个热化学方程式:

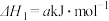

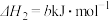
则
______ (填“>”“<”或“=”) 。
。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
已知:
 ,根据下表中所列键能数据可计算出
,根据下表中所列键能数据可计算出
______ 。
(1)实验测得,5 g液态甲醇(
 )在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,则1 mol液态甲醇充分燃烧生成二氧化碳气体和液态水的热化学方程式为
)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,则1 mol液态甲醇充分燃烧生成二氧化碳气体和液态水的热化学方程式为(2)现有如下两个热化学方程式:

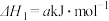

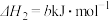
则

 。
。(3)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
已知:

 ,根据下表中所列键能数据可计算出
,根据下表中所列键能数据可计算出
| 化学键 | H-H | N-H |  |
键能/( ) ) | 436 | 391 | 946 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。有机物M经过太阳光光照可转化成N,转化过程如下:
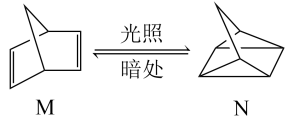 ΔH= + 88.6kJ/mol
ΔH= + 88.6kJ/mol
(1)则M、N相比,较稳定的是_______ 。
II.参考以下表格中的键能数据,回答下列问题:
(2)比较下列两组物质的熔点高低(填“>”或“<”):SiC_______ Si;SiCl4_______ SiO2。
(3)能不能根据键能的数据判断晶体硅和化合物SiCl4的熔点高低?_______ (填“能”或“不能”),理由是_______ 。
(4)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)=Si(s)+4HCl(g)。计算该反应的反应热△H为_______ kJ/mol。
 ΔH= + 88.6kJ/mol
ΔH= + 88.6kJ/mol(1)则M、N相比,较稳定的是
II.参考以下表格中的键能数据,回答下列问题:
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
(3)能不能根据键能的数据判断晶体硅和化合物SiCl4的熔点高低?
(4)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)=Si(s)+4HCl(g)。计算该反应的反应热△H为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请完成下列热化学方程式:
(1)1mol N2(气态)与适量O2(气态)起反应,生成NO2(气态),需吸收68kJ的热量___ ;
(2)卫星发射时可用N2H4为燃料。32gN2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534kJ的热量___ ;
(3)已知氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水放热2.444kJ,写出氢气和氧气反应生成液态水的热化学方程式___ ;
(4)已知:键能(H2—436kJ/mol,N2—946kJ/mol,N-H—391kJ/mol)请写出氮气与氢气合成氨气的热化学方程式___ 。
(1)1mol N2(气态)与适量O2(气态)起反应,生成NO2(气态),需吸收68kJ的热量
(2)卫星发射时可用N2H4为燃料。32gN2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534kJ的热量
(3)已知氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水放热2.444kJ,写出氢气和氧气反应生成液态水的热化学方程式
(4)已知:键能(H2—436kJ/mol,N2—946kJ/mol,N-H—391kJ/mol)请写出氮气与氢气合成氨气的热化学方程式
您最近一年使用:0次



