(1)35Cl-离子结构示意图_______ 。
(2)16.4 g NaR含有Na+ 0.2 mol,则NaR的摩尔质量为____ ,则含R-的质量为5.9 g的NaR的物质的量为_______ 。
(3)标准状况下,3.2 g甲烷(CH4)所占的体积为___ L,它与标准状况下__ L硫化氢(H2S)含有相同数目的氢原子。
(4)在200 g浓度为18 mol·L-1、密度为ρ (g·cm-3)的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积_____ 200 mL。(填“>”“<”、“=”)
(2)16.4 g NaR含有Na+ 0.2 mol,则NaR的摩尔质量为
(3)标准状况下,3.2 g甲烷(CH4)所占的体积为
(4)在200 g浓度为18 mol·L-1、密度为ρ (g·cm-3)的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积
19-20高二·浙江·期末 查看更多[1]
(已下线)【新东方】2020-31
更新时间:2020-02-28 10:42:49
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将含H2SO4 49 g的一定量的浓硫酸缓慢地加入水中,冷却至室温后,恰好得到稀硫酸1000mL。求:
(1)所得稀硫酸溶液中含H2SO4的物质的量是_____________ ?
(2)所得稀硫酸溶液中H+的物质的量浓度是________________ ?
(1)所得稀硫酸溶液中含H2SO4的物质的量是
(2)所得稀硫酸溶液中H+的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】化学计量在生产和科研中应用广泛。回答下列问题:
(1) 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为___________ ,其质子的物质的量为___________ 。
(2)某气态氧化物的化学式为 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(3)若 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为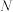 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为___________ (用含字母的代数式表示)。
(4)标准状况下将a LX气体(摩尔质量为 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为___________ 。
(5)将 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为___________ (忽略混合前后溶液体积的变化)。
(6)某混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
___________ 。
(1)
 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为(2)某气态氧化物的化学式为
 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为(3)若
 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为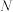 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为(4)标准状况下将a LX气体(摩尔质量为
 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)将
 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为(6)某混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求作答:
(1)乙醇和乙酸反应可生成乙酸乙酯,反应方程式为:_______ 。在密闭容器中,利用该反应制备乙酸乙酯,实验中若起始时在容器中加入3mol乙醇、1mol乙酸和一定量的浓硫酸,充分反应后容器中残留的乙醇可能为_______ 。
A.2mol B.2.6mol C.2.8mol D.3mol
(2)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀HNO3500 mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1 L 1 mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2 g。
①Cu与Cu2O 的物质的量之比为_______ 。
②HNO3的物质的量浓度为_______ mol·L-1。
(1)乙醇和乙酸反应可生成乙酸乙酯,反应方程式为:
A.2mol B.2.6mol C.2.8mol D.3mol
(2)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀HNO3500 mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1 L 1 mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2 g。
①Cu与Cu2O 的物质的量之比为
②HNO3的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】根据题意填空:
(1)在标准状况下,测得1.92g某气体的体积为672mL, 则该气体的摩尔质量为______ ;
(2)5.4gH2O所含氢原子数与_____ L (标准状况下)氨气所含氢原子数相等;
(3)在一定温度下,有摩尔质量为Mg/mol的某物质溶于适量的水中,得到物质的量浓度为c mol/L,密度为ρ g/mL的饱和溶液,则该温度下此物质的溶解度为____ 。
(4)CO和CO2的混合气体36g,完全燃烧后测得CO2的体积为22.4L(标准状况下),则混合气体中CO的质量为_________ ,原混 合气体中CO2体积为_____ (标准状况)。
(1)在标准状况下,测得1.92g某气体的体积为672mL, 则该气体的摩尔质量为
(2)5.4gH2O所含氢原子数与
(3)在一定温度下,有摩尔质量为Mg/mol的某物质溶于适量的水中,得到物质的量浓度为c mol/L,密度为ρ g/mL的饱和溶液,则该温度下此物质的溶解度为
(4)CO和CO2的混合气体36g,完全燃烧后测得CO2的体积为22.4L(标准状况下),则混合气体中CO的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)①NaOH溶液 ②铜丝 ③熔融NaCl ④SO2⑤稀硫酸 ⑥蔗糖晶体
a.属于电解质______ b.属于非电解质的是______
(2)下列所给出的几组物质中:含有分子数最少的是___________ ;含有原子数最多的是___________ ;标准状况下体积最小的是___________ 。
①1g H2②2.408×1023个CH4分子 ③10.8g H2O ④标准状况下6.72L CO2。
(3)8gCH4中含有a个原子,则阿伏加德罗常数是___________ mol-1(用 a表示)
(4)与0.1molOH-含有相同电子数的CH4在标状况下的体积为___________ L。
a.属于电解质
(2)下列所给出的几组物质中:含有分子数最少的是
①1g H2②2.408×1023个CH4分子 ③10.8g H2O ④标准状况下6.72L CO2。
(3)8gCH4中含有a个原子,则阿伏加德罗常数是
(4)与0.1molOH-含有相同电子数的CH4在标状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)标准状况下,3.4gNH3与________ LCO气体所含有电子数相同。
(2)0.2L0.5mol·L-1Al2(SO4)3溶液和0.5L0.5mol·L-1Na2SO4溶液,所含SO42-离子浓度之比为_________ 。
(3)标准状况下,NH3 与 CH4 组成的混合气体的平均密度为 0.75g/L,则 NH3 的体积分数为__________
(4)配制 100mL 2mol/L 的 H2SO4 溶液,取配制后的溶液 20mL,加入足量的锌,生成标况下 氢气的体积为_____ L。
(5)已知 16g A 和 20g B 恰好完全反应生成 0.04mol C 和 32g D,则 C 的摩尔质量为______
(2)0.2L0.5mol·L-1Al2(SO4)3溶液和0.5L0.5mol·L-1Na2SO4溶液,所含SO42-离子浓度之比为
(3)标准状况下,NH3 与 CH4 组成的混合气体的平均密度为 0.75g/L,则 NH3 的体积分数为
(4)配制 100mL 2mol/L 的 H2SO4 溶液,取配制后的溶液 20mL,加入足量的锌,生成标况下 氢气的体积为
(5)已知 16g A 和 20g B 恰好完全反应生成 0.04mol C 和 32g D,则 C 的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】现有m g某气体,它的摩尔质量为M g·mol-1。若阿伏伽德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol。
(2)该气体在标况下的密度为__________ g/L。
(3)该气体在标准状况下的体积为____________ L。
(4)该气体溶于0.1L水中(水的密度:1g·mL-1,且不考虑反应),其溶液中溶质的质量分数为_____ 。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____ mol/L。
(1)该气体的物质的量为
(2)该气体在标况下的密度为
(3)该气体在标准状况下的体积为
(4)该气体溶于0.1L水中(水的密度:1g·mL-1,且不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】在一定条件下,有下列物质:①8gCH4、②6.02×1023个HCl分子、③2mol O2。按由小到大的顺序填写下列空白(填写序号):
(1)摩尔质量____________________ 。
(2)物质的量____________________ 。
(3)分子数目____________________ 。
(4)原子数目____________________ 。
(5)质量____________________ 。
(1)摩尔质量
(2)物质的量
(3)分子数目
(4)原子数目
(5)质量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】铁和钴是重要的过渡元素。
(1)钴位于元素周期表中第___ 族,基态钴原子中未成对电子的个数为_____ 。
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为___ ;尿素分子中氮原子的杂化方式是___ ,尿素中所含非金属元素的电负性由大到小的顺序是___ 。
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀。
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为_____ 。
(4)离子化合物CaC2的一种晶体结构如图1所示,从钙离子看,属于____ 堆积,其配位数是_____ ;一个晶胞中平均含有的π键的个数为_____ 。

图1
(5)科学研究结果表明。碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH,其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是____ 。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为______ ,若晶体密度为ρg/cm3,则晶胞中最近的两个碳原子的距离为_____ pm(阿伏伽德罗常数的值用NA表示,写出计算式即可)。

图2
(1)钴位于元素周期表中第
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀。
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为
(4)离子化合物CaC2的一种晶体结构如图1所示,从钙离子看,属于

图1
(5)科学研究结果表明。碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH,其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为

图2
您最近一年使用:0次



