不同元素的原子吸引电子的能力大小可用一定数值X表示,X值越大,其原子吸引电子的能力越强,在所形成的化合物中为带负电荷的一方。下表是某些元素的X值:
(1)通过分析X值的变化规律,确定 、
、 的X值范围:
的X值范围:______ 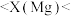
______ ;______ 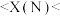
______ 。
(2)推测X值与原子半径的关系为______ 。
(3)某有机化合物的结构为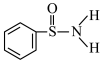 ,其中
,其中 键中,你认为共用电子对偏向
键中,你认为共用电子对偏向______ (填元素符号)。
(4)如果X值为电负性的数值,试推断 中化学键的类型为
中化学键的类型为______ 。
(5)预测元素周期表中X值最小的元素(放射性元素除外)是______ (填元素符号)。
| 元素符号 |  |  |  |  |  |  |
| X值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素符号 |  |  |  |  |  |  |
| X值 | 0.93 | 1.60 | 1.90 | 2.19 | 2.55 | 3.16 |
 、
、 的X值范围:
的X值范围: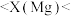
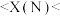
(2)推测X值与原子半径的关系为
(3)某有机化合物的结构为
 ,其中
,其中 键中,你认为共用电子对偏向
键中,你认为共用电子对偏向(4)如果X值为电负性的数值,试推断
 中化学键的类型为
中化学键的类型为(5)预测元素周期表中X值最小的元素(放射性元素除外)是
更新时间:2020-03-05 11:30:39
|
相似题推荐
【推荐1】根据题给信息回答问题
(1)某元素原子的价电子构型为4s24p1,它属于第___________ 周期第___________ 族,属于___________ 区元素。
(2)在1~18号元素中,除稀有气体元素外,原子半径最大的元素是___________ (用元素符号表示,下同),电负性最大的元素是___________ ;第一电离能最大的元素是___________ 。第三周期原子半径最小的主族元素的价电子排布式为___________ 。
(3)写出Cu+的核外电子排布式:___________ 。按电子排布,可将周期表中的元素划分成五个区域,第四周期元素中属于s区的元素有___________ 种,
(4)某元素原子的3p轨道有1个未成对电子,该元素为___________ (用元素符号表示)。
(1)某元素原子的价电子构型为4s24p1,它属于第
(2)在1~18号元素中,除稀有气体元素外,原子半径最大的元素是
(3)写出Cu+的核外电子排布式:
(4)某元素原子的3p轨道有1个未成对电子,该元素为
您最近一年使用:0次
【推荐2】按要求完成下列填空。
(1)在元素周期表中电负性最大的元素是_______ (填元素符号);短周期中第一电离能最小的元素基态原子的价层电子排布图为_______ 。
(2)基态原子的2p轨道上有两个未成对电子的元素有_______ (填元素符号)。前四周期元素中,未成对电子数最多的元素基态原子的价层电子排布式为_______ 。
(3) 中
中 原子的杂化方式为
原子的杂化方式为_______ ,属于_______ (“极性”或“非极性”)分子。
(4)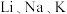 熔沸点依次降低的原因是
熔沸点依次降低的原因是_______ 。
(1)在元素周期表中电负性最大的元素是
(2)基态原子的2p轨道上有两个未成对电子的元素有
(3)
 中
中 原子的杂化方式为
原子的杂化方式为(4)
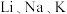 熔沸点依次降低的原因是
熔沸点依次降低的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键元素间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,原子之间通常形成共价键。表中是某些元素的电负性值:
观察上述数据,回答下列问题:
(1)通过分析电负性值变化规律,确定Mg元素电负性值的最小范围:_______ 。
(2)请归纳元素的电负性和金属性、非金属性的关系_______ 。
(3)某有机化合物结构中含S-N键,其共用电子对偏向_______ (写原子名称)。
(4)从电负性角度,判断AlCl3是离子化合物,还是共价化合物的方法是_______ (写出判断的方法和结论);请设计一个实验方案证明上述所得到的结论:_______ 。
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
观察上述数据,回答下列问题:
(1)通过分析电负性值变化规律,确定Mg元素电负性值的最小范围:
(2)请归纳元素的电负性和金属性、非金属性的关系
(3)某有机化合物结构中含S-N键,其共用电子对偏向
(4)从电负性角度,判断AlCl3是离子化合物,还是共价化合物的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料,光伏材料又称太阳能材料,只有半导体材料具有这种功能。硅(Si)、镓(Ga)、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:___________ 。硅烷很难像烷烃一样形成长链,这是因为硅的原子半径___________ (填“大于”“小于”或“等于”)碳的原子半径,因此键长___________ (填“长”或“短”),键能小。丁硅烯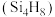 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是___________ 。
(3)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是___________ 。
(4)硅和锗都能与氯元素形成四氯化物 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:___________ 。
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
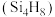 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近一年使用:0次
【推荐2】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是___________ ,占据该能层电子的电子云轮廓图形状为___________ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:___________ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是___________ 。
(4)已知铁是26号元素,写出Fe的价层电子排布式___________ ;在元素周期表中,该元素在_____________ 填“s”“p”“d”“f”或“ds”)区。
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为___________ 。电负性的顺序是___________ 。
(6)写出C的核外电子排布图为:___________ 。
(7)Zn2+的核外电子排布式为___________ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(6)写出C的核外电子排布图为:
(7)Zn2+的核外电子排布式为
您最近一年使用:0次



