根据题给信息回答问题
(1)某元素原子的价电子构型为4s24p1,它属于第___________ 周期第___________ 族,属于___________ 区元素。
(2)在1~18号元素中,除稀有气体元素外,原子半径最大的元素是___________ (用元素符号表示,下同),电负性最大的元素是___________ ;第一电离能最大的元素是___________ 。第三周期原子半径最小的主族元素的价电子排布式为___________ 。
(3)写出Cu+的核外电子排布式:___________ 。按电子排布,可将周期表中的元素划分成五个区域,第四周期元素中属于s区的元素有___________ 种,
(4)某元素原子的3p轨道有1个未成对电子,该元素为___________ (用元素符号表示)。
(1)某元素原子的价电子构型为4s24p1,它属于第
(2)在1~18号元素中,除稀有气体元素外,原子半径最大的元素是
(3)写出Cu+的核外电子排布式:
(4)某元素原子的3p轨道有1个未成对电子,该元素为
20-21高二下·吉林通化·期末 查看更多[5]
吉林省通化县综合高级中学2020-2021学年高二下学期期末考试化学试题(已下线)第一章 原子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)黑龙江省齐齐哈尔市第八中学2021-2022学年高二下学期开学考试化学试题广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题(已下线)专题01 物质的结构与性质-备战2023-2024学年高二化学下学期期末真题分类汇编(辽宁、黑龙江、吉林专用)
更新时间:2021-07-20 00:25:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
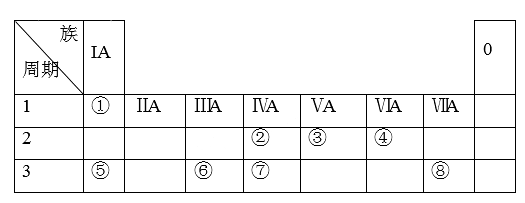
(1)①的元素符号为______ ;②的元素符号为______ ;③的元素符号为______ ;④的元素符号为______ ;⑤的元素符号为______ ;⑥的元素符号为______ ;⑦的元素符号为______ ;⑧的元素符号为_______
(2)⑥的原子结构示意图为_________ 。
(3)⑧的气态氢化物为_____________ (填化学式)。
(4)⑤对应的碱的化学式为__________ ;③的最高价含氧酸为___________ 。(填化学式)
(5)⑤、⑥元素的金属性强弱依次为___________ 。(填“增大”、“减小”或“不变”)

(1)①的元素符号为
(2)⑥的原子结构示意图为
(3)⑧的气态氢化物为
(4)⑤对应的碱的化学式为
(5)⑤、⑥元素的金属性强弱依次为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I. 填空:
(1)写出表示含有8个质子、10个中子的原子的化学符号:_________ 。
(2)元素周期表中位于第8纵行的铁元素属于_________ 族。
(3)元素周期表中最活泼的非金属元素位于第_________ 纵行。
(4)所含元素超过18种的周期是第_________ 周期。
II. 4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
(1)元素x在周期表中的位置是第________ 周期、第________ 族。
(2)四种元素最高价氧化物的水化物中,酸性最强的是_____ ,碱性最强的是_____ (填化学式)。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)元素周期表中位于第8纵行的铁元素属于
(3)元素周期表中最活泼的非金属元素位于第
(4)所含元素超过18种的周期是第
II. 4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是第
(2)四种元素最高价氧化物的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表中的一部分元素,用元素符号或化学式回答下列问题:
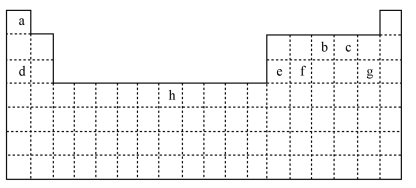
(1)h元素在周期表中的位置是_______ ;
(2)表中所列元素中,金属性最强的是____ ;元素最高价含氧酸酸性最强的是____ ;(填化学式)
(3)c、d、e、g中,离子半径最小的是____ ;(填离子符号)
(4)a和b化合时形成_____ 键;a和d化合时形成______ 键;
(5)由a、c、d形成的化合物的电子式为__________ 。

(1)h元素在周期表中的位置是
(2)表中所列元素中,金属性最强的是
(3)c、d、e、g中,离子半径最小的是
(4)a和b化合时形成
(5)由a、c、d形成的化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】A~R 9种元素在元素周期表中的位置如图。
回答下列问题:
(1)E的原子结构示意图为_______ 。
(2)常温下, 的状态为
的状态为_______ (填“液”、“固”或“气”)态。
(3)写出单质A与 在加热条件下发生反应的化学方程式:
在加热条件下发生反应的化学方程式:_______ 。
(4)化合物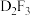 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为_______ 。
(5)H元素形成的单质的用途有_______ (填一种即可)。
(6)最高价氧化物对应水化物的碱性:C_______ (填“>”、“<”或“=”)A,判断的理由为_______ 。
(7)化合物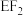 所含分子中的电子总数为
所含分子中的电子总数为_______ ,与其具有相同电子数的化合物分子为_______ (填标号)。
a. b.
b. c.
c. d.
d.
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | A | E | F | |||||
| 3 | C | D | G | H | ||||
| 4 | B | R | ||||||
(1)E的原子结构示意图为
(2)常温下,
 的状态为
的状态为(3)写出单质A与
 在加热条件下发生反应的化学方程式:
在加热条件下发生反应的化学方程式:(4)化合物
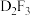 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为(5)H元素形成的单质的用途有
(6)最高价氧化物对应水化物的碱性:C
(7)化合物
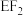 所含分子中的电子总数为
所含分子中的电子总数为a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区元素的是________ (填元素符号)。
(2)⑥和⑦形成的分子中各个原子均满足8电子稳定结构,其立体构型为________ 。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子和⑦形成的分子,中心原子上的价层电子对数为_______ 。
(4)元素⑦和⑧形成的化合物的电子式为__________ 。
(5)元素⑩的基态+2价离子的电子排布式是__________ 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:___________ 。

请回答下列问题:
(1)表中属于d区元素的是
(2)⑥和⑦形成的分子中各个原子均满足8电子稳定结构,其立体构型为
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子和⑦形成的分子,中心原子上的价层电子对数为
(4)元素⑦和⑧形成的化合物的电子式为
(5)元素⑩的基态+2价离子的电子排布式是
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为______________________________________ 。
(2)MX3-的空间构型__________________________ (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是_____________________________________________________ 。
(4)根据等电子原理,WX分子的结构式为_______________________ 。
(5)1 mol WX2中含有的σ键数目为_______________________ 。
(6)H2X分子中X原子轨道的杂化类型为_______________________ 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式_______________________ 。
(1)Y3+基态的电子排布式可表示为
(2)MX3-的空间构型
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是
(4)根据等电子原理,WX分子的结构式为
(5)1 mol WX2中含有的σ键数目为
(6)H2X分子中X原子轨道的杂化类型为
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】该反应曾用于检测司机是否酒后驾驶:2Cr2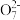 +3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
(1)基态Cr3+的核外电子排布式为_______ ;配合离子[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______ (填元素符号)。
(2)CH3COOH中C原子的杂化轨道类型为_______ 和_______ ;1molCH3COOH分子中含有σ键的数目为_______ 。
(3)H2O与CH3CH2OH可以任意比例互溶,原因是_______ 、_______ (回答两点)。
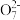 +3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH(1)基态Cr3+的核外电子排布式为
(2)CH3COOH中C原子的杂化轨道类型为
(3)H2O与CH3CH2OH可以任意比例互溶,原因是
您最近一年使用:0次
【推荐3】1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:
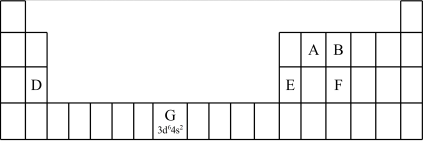
①在元素周期表中,第ⅠB、ⅡB元素属于___________ 区。
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的___________ ,该元素M能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D___________ E(填“>”“<”或“=”)。
②气态氢化物的沸点:B___________ F(填“>”“<”或“=”),理由是___________ 。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E、F六种元素的原子序数依次递增,前四种元素为短周期元素。A位于元素周期表s区,电子层数与未成对电子数相等;B基态原子中电子占据三种能量不同的原子轨道,且每轨道中的电子总数相同;D原子核外成对电子数为未成对电子数的3倍;F位于第四周期d区,最高能级的原子轨道内只有2个未成对电子;E的一种氧化物具有磁性。
(1)E基态原子的价层电子排布式为__________________ 。第二周期基态原子未成对电子数与F相同且电负性最小的元素名称为____________ 。
(2)CD3- 的空间构型为_______________ 。
(3)A、B、D三元素组成的一种化合物X是家庭装修材料中常含有的一种有害气体,X分子中的中心原子采用_____________ 杂化。
(4)F(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________ 。根据等电子原理,B、D 分子内σ键与π键的个数之比为______________ 。
(5)一种EF的合金晶体具有面心立方最密堆积的结构。在晶胞中,F位于顶点,E位于面心,该合金中EF的原子个数之比为_________________ 。若晶胞边长a pm,则合金密度为______________ g·cm3(列式表达,不计算)。
(1)E基态原子的价层电子排布式为
(2)CD3- 的空间构型为
(3)A、B、D三元素组成的一种化合物X是家庭装修材料中常含有的一种有害气体,X分子中的中心原子采用
(4)F(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(5)一种EF的合金晶体具有面心立方最密堆积的结构。在晶胞中,F位于顶点,E位于面心,该合金中EF的原子个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键元素间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,原子之间通常形成共价键。表中是某些元素的电负性值:
观察上述数据,回答下列问题:
(1)通过分析电负性值变化规律,确定Mg元素电负性值的最小范围:_______ 。
(2)请归纳元素的电负性和金属性、非金属性的关系_______ 。
(3)某有机化合物结构中含S-N键,其共用电子对偏向_______ (写原子名称)。
(4)从电负性角度,判断AlCl3是离子化合物,还是共价化合物的方法是_______ (写出判断的方法和结论);请设计一个实验方案证明上述所得到的结论:_______ 。
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
观察上述数据,回答下列问题:
(1)通过分析电负性值变化规律,确定Mg元素电负性值的最小范围:
(2)请归纳元素的电负性和金属性、非金属性的关系
(3)某有机化合物结构中含S-N键,其共用电子对偏向
(4)从电负性角度,判断AlCl3是离子化合物,还是共价化合物的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填写下列空白[第(1)~(4)小题用元素符号填写]。
(1)第三周期原子半径最小的元素________ 。
(2)第一电离能最大的元素________ 。
(3)电负性最大的元素________ 。
(4)第四周期中第一电离能最小的元素________ 。
(5)含有8个质子,10个中子的原子的化学符号________ 。
(6)最外层电子排布为4s24p1的原子的核电荷数为________ 。
(7)周期表中最活泼的非金属元素原子的轨道表示式为___________________ 。________________ ,它位于________ 区。
(1)第三周期原子半径最小的元素
(2)第一电离能最大的元素
(3)电负性最大的元素
(4)第四周期中第一电离能最小的元素
(5)含有8个质子,10个中子的原子的化学符号
(6)最外层电子排布为4s24p1的原子的核电荷数为
(7)周期表中最活泼的非金属元素原子的轨道表示式为
(8)某元素核外有三个电子层,最外层电子数是核外电子总数的 ,写出该元素原子的电子排布式是
,写出该元素原子的电子排布式是
您最近一年使用:0次



