下列图示与对应的叙述相符的是
A.图甲表示升高温度醋酸钠的水解程度增大,溶液碱性增强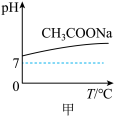 |
B.图乙表示氢氟酸为弱酸,且a点Kw的数值比b点Kw的数值大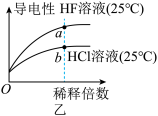 |
C.图丙表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,曲线d的压强比曲线c的压强大 3C(g)+D(s)的影响,曲线d的压强比曲线c的压强大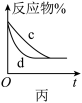 |
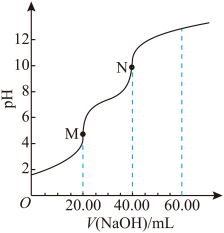
D.图丁表示用0.1000mol·L-1 NaOH溶液滴定20.00mL0.1000mol·L-1 CH3COOH溶液的滴定曲线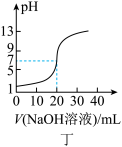 |
更新时间:2020-03-17 10:24:01
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,在用标准盐酸滴定NaOH溶液的实验中,对下列图示的叙述正确的是


| A.盛装NaOH溶液后,排滴定管内气泡的操作如图①所示 |
| B.滴定过程中,眼睛的视线如图②所示 |
| C.如图③所示,所用标准盐酸的体积为26.10 mL |
| D.滴定过程中,随标准盐酸的滴入,混合溶液的pH变化如图④所示 |
您最近半年使用:0次
【推荐2】25℃时,用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H3AO3溶液,溶液中所有含A微粒的分布分数δ(平衡时某含A微粒的浓度占各含A微粒浓度之和的分数)与pH的关系如图所示(已知100.2=1.58):
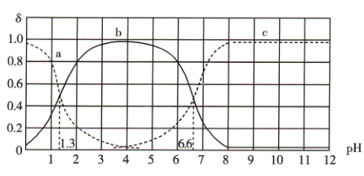
下列说法错误的是

下列说法错误的是
| A.H3AO3属于二元酸 |
| B.第一次滴定终点时可用甲基橙作指示剂 |
C.当溶液呈中性时,溶液中 约为6 约为6 |
D.当加入30mLNaOH溶液时,2c(Na+)=6c(HAO )+3c(H3AO3) )+3c(H3AO3) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各选项中所述的两个量,前者一定大于后者的是
| A.1 L 0.3 mol/L CH3COOH溶液和3 L 0.1 mol/L CH3COOH溶液中的H+数 |
| B.pH=1的CH3COOH溶液和盐酸的物质的量浓度 |
| C.pH=12的氨水和NaOH溶液的导电能力 |
| D.pH相同的等体积的盐酸和醋酸溶液分别与足量锌粒反应产生的气体体积 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
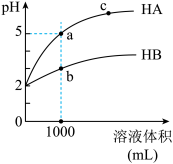
【推荐2】室温下,pH均为2的两种一元酸HA和HB各 ,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是
,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是
 ,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是
,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是
| A.HA的酸性比HB的酸性弱 |
| B.a点溶液的导电性比c点溶液的导电性强 |
| C.溶液中水的电离程度a>c |
D.对a、b两点溶液同时升高温度,则 增大 增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向 0.1 mol/L 醋酸溶液中加水稀释,下列变化叙述错误的是
| A.溶液的 pH 逐渐增大 | B.溶液中的 c(OH-)逐渐减小 |
| C.醋酸的电离程度逐渐增大 | D.溶液的导电能力逐渐减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列有关各溶液的叙述正确的是
A. 的溶液中不可能存在醋酸分子 的溶液中不可能存在醋酸分子 |
B. 的醋酸钠溶液与 的醋酸钠溶液与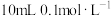 的盐酸混合后溶液显酸性: 的盐酸混合后溶液显酸性: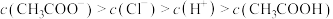 |
C. 醋酸的 醋酸的 , , 的醋酸的 的醋酸的 ,则 ,则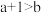 |
D.已知酸性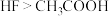 ,pH相等的 ,pH相等的 与 与 溶液中 溶液中 |
您最近半年使用:0次

 )>c(
)>c( )>c(
)>c( )
) 醋酸溶液的
醋酸溶液的 可证明醋酸是弱电解质
可证明醋酸是弱电解质
 的盐酸稀释至1L,
的盐酸稀释至1L, 约为
约为
 物质的量不同
物质的量不同 和
和 各
各 分别稀释2倍后,再分别加入
分别稀释2倍后,再分别加入 锌粉,在相同条件下充分反应。下列有关说法正确的是
锌粉,在相同条件下充分反应。下列有关说法正确的是
 的质量:
的质量:


