在FeBr2和FeI2混合溶液中逐渐通入氯气,可能发生反应的离子方程式是
| A.Fe2+ + Cl2 → Fe3+ + 2Cl- |
| B.2Fe2+ + 2Br- + 2I- + 3Cl2 → 2Fe3+ + I2 + Br2 + 6Cl- |
| C.2Fe2+ + 4Br- + 2I- + 4Cl2 → 2Fe3+ + I2 + 2Br2 + 8Cl- |
| D.4Fe2+ + 2Br-+ 2I- + 4Cl2 → 4Fe3+ + I2 + Br2 + 8Cl- |
更新时间:2020-03-22 15:14:00
|
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】某水体溶有Ca2+、Mg2+、HCO3-三种离子,可先加足量消石灰,再加足量纯碱以除去Ca2+、Mg2+。以下离子方程式肯定不符合反应事实的是
| A.Mg2++2HCO3-+Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O |
| B.Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
| C.Mg2++3HCO3-+3Ca2++5OH-=Mg(OH)2↓+3CaCO3↓+3H2O |
| D.Ca2++CO32-=CaCO3↓ |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】下列实验,能正确描述其反应的离子方程式是
A.用Na2SO3溶液吸收少量C12:3 +C12+H2O=2 +C12+H2O=2 +2C1-+ +2C1-+ |
| B.向H2O2溶液中滴加少量FeC13:2Fe3++H2O2=O2+2H++2Fe2+ |
C.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应:Ba2++ =BaSO4 =BaSO4 |
D.向体积、等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合: +Ba2++OH-=BaCO3↓+H2O +Ba2++OH-=BaCO3↓+H2O |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐3】下列离子方程式正确的是
A.将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO +OH- →CaCO3↓+H2O +OH- →CaCO3↓+H2O |
| B.Fe(OH)3溶于氢碘酸:2Fe(OH)3 + 6H+ + 2Iˉ →2Fe2+ + I2 + 6H2O |
| C.向硫酸铝铵[NH4Al(SO4)2]溶液中加入氢氧化钡溶液至SO42ˉ离子沉淀完全Al3+ + 2SO42ˉ + 2Ba2+ + 4OHˉ →AlO2ˉ + 2BaSO4↓+ 2H2O |
| D.4mol·L-1的NaAlO2溶液和7mol·L-1的HCl等体积互相均匀混合4AlO2-+ 7H+ + H2O→ 3Al(OH)3↓+ Al3+ |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】用微生物燃料电池作电源进行模拟消除酸性工业废水中的重铬酸根离子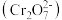 的示意图如下,反应一段时间后,在装置②中得到
的示意图如下,反应一段时间后,在装置②中得到 和
和 两种沉淀。下列说法错误的是
两种沉淀。下列说法错误的是
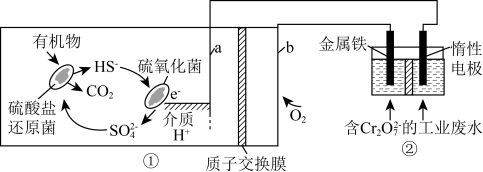
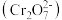 的示意图如下,反应一段时间后,在装置②中得到
的示意图如下,反应一段时间后,在装置②中得到 和
和 两种沉淀。下列说法错误的是
两种沉淀。下列说法错误的是
| A.装置②中惰性电极为阴极 |
| B.装置①中a极区pH逐渐减小 |
C.装置①中b极上消耗的 与装置②中惰性电极上生成的n(生成物)相等 与装置②中惰性电极上生成的n(生成物)相等 |
D.装图②中,生成 的反应式: 的反应式: |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】铬铁渣是火法炼铬所产生的废渣,其中铬以低价态的 存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示
存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示 存在,在碱性介质中以
存在,在碱性介质中以 存在。下列说法错误的是
存在。下列说法错误的是
 存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示
存在,主要杂质为铁、铝、硅的氧化物,从铬铁渣中提取铬的一种流程如图所示
 存在,在碱性介质中以
存在,在碱性介质中以 存在。下列说法错误的是
存在。下列说法错误的是A.焙烧后,含铬化合物主要以 存在 存在 |
| B.加水浸取过滤,滤渣1的主要成分应含有铁元素 |
| C.除铝步骤,为使杂质沉淀彻底,应加入足量稀硫酸 |
D.还原步骤发生的离子反应是: |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】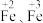 水体中存在的
水体中存在的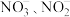 等致癌阴离子对人体健康造成严重威胁,采用Pd-
等致癌阴离子对人体健康造成严重威胁,采用Pd- 双催化剂可实现用
双催化剂可实现用 消除酸性废水中的
消除酸性废水中的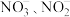 ,
, 中含有
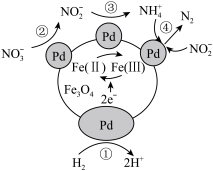
中含有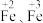 ,分别表示为Fe(II)、Fe(III),其反应历程如图所示。下列说法错误的是
,分别表示为Fe(II)、Fe(III),其反应历程如图所示。下列说法错误的是
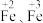 水体中存在的
水体中存在的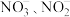 等致癌阴离子对人体健康造成严重威胁,采用Pd-
等致癌阴离子对人体健康造成严重威胁,采用Pd- 双催化剂可实现用
双催化剂可实现用 消除酸性废水中的
消除酸性废水中的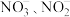 ,
, 中含有
中含有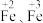 ,分别表示为Fe(II)、Fe(III),其反应历程如图所示。下列说法错误的是
,分别表示为Fe(II)、Fe(III),其反应历程如图所示。下列说法错误的是
A.过程①在Pd催化剂作用下将 中Fe(III)转化为Fe(II) 中Fe(III)转化为Fe(II) |
B.过程②在Pd催化下发生的离子反应为 |
C.过程③每生成1个 以及过程④每生成1个 以及过程④每生成1个 ,都转移3个电子 ,都转移3个电子 |
| D.用该法处理后水体的酸性增强 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】废旧锂离子电池经处理得到的正极活性粉体中含有 、
、 、
、 、
、 、Fe、C、Al、Cu等。采用以下工艺流程可从废旧锂离子电池中分离回收钴、镍、锰,制备正极材料的前驱体(
、Fe、C、Al、Cu等。采用以下工艺流程可从废旧锂离子电池中分离回收钴、镍、锰,制备正极材料的前驱体( )。
)。

下列说法错误的是
 、
、 、
、 、
、 、Fe、C、Al、Cu等。采用以下工艺流程可从废旧锂离子电池中分离回收钴、镍、锰,制备正极材料的前驱体(
、Fe、C、Al、Cu等。采用以下工艺流程可从废旧锂离子电池中分离回收钴、镍、锰,制备正极材料的前驱体( )。
)。
下列说法错误的是
A.“酸浸”时 的作用是氧化剂 的作用是氧化剂 |
B.除铁时加入的物质X为 |
C.除铝时发生的反应为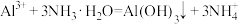 |
D.滤液④中的溶质为 |
您最近一年使用:0次

 、
、 和
和 ,流程如图所示。下列说法错误的是
,流程如图所示。下列说法错误的是
 过程中氧化剂与还原剂物质的量之比为1∶1
过程中氧化剂与还原剂物质的量之比为1∶1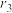 过程中发生反应的离子方程式为
过程中发生反应的离子方程式为
 过程中每生成
过程中每生成 ,转移电子的物质的量为
,转移电子的物质的量为

 的一种制备方法如下图所示:
的一种制备方法如下图所示: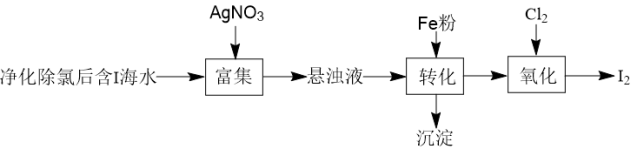
 的海水可通过加
的海水可通过加 溶液得到含I海水
溶液得到含I海水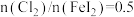 时,氧化产物为
时,氧化产物为
 ,单质碘的产率会降低,原因是碘挥发
,单质碘的产率会降低,原因是碘挥发

