铁是人类利用最为广泛的金属之一,工业炼铁一般用一氧化碳作还原剂。
(1)已知Fe2O3在高炉中有下列反应:Fe2O3+CO 2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是
2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是_________ 。
a.7:3 b.21: 8 c.14: 5 d.7:2
(2)若m(Fe):m(O)=3:1,则Fe2O3与FeO的物质的量之比为_________ ,Fe2O3被CO还原的物质的量分数为____________ 。
(3)3.04 g Fe2O3和FeO的混合固体粉末在加热条件下用足量CO使金属氧化物完全还原,生成的CO2气体通入含0.04 mol Ca(OH)2的澄清石灰水后,产生3.00 g白色沉淀。计算固体粉末中Fe2O3的质量。(保留1位小数)____________
(4)常温下,称取不同铁锈样品溶入足量盐酸,向溶液中加入足量NaOH溶液生成沉淀,然后过滤、洗涤、灼烧,得到Fe2O3固体,实验过程中产品无损失。
实验数据记录如下:
上述实验①②③④所用铁锈均不含杂质,且实验数据可靠。通过计算,分析和比较上表4组数据,给出结论。_______________
(1)已知Fe2O3在高炉中有下列反应:Fe2O3+CO
 2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是
2FeO+CO2。反应形成的Fe2O3和FeO固体混合物中,元素铁和氧的质量比m(Fe):m(O)不可能是a.7:3 b.21: 8 c.14: 5 d.7:2
(2)若m(Fe):m(O)=3:1,则Fe2O3与FeO的物质的量之比为
(3)3.04 g Fe2O3和FeO的混合固体粉末在加热条件下用足量CO使金属氧化物完全还原,生成的CO2气体通入含0.04 mol Ca(OH)2的澄清石灰水后,产生3.00 g白色沉淀。计算固体粉末中Fe2O3的质量。(保留1位小数)
(4)常温下,称取不同铁锈样品溶入足量盐酸,向溶液中加入足量NaOH溶液生成沉淀,然后过滤、洗涤、灼烧,得到Fe2O3固体,实验过程中产品无损失。
实验数据记录如下:
实验序号 | 铁锈质量/g | 氧化铁质量/g |
① | 0.856 | 0.640 |
② | 1.424 | 1.280 |
③ | 0.979 | 0.880 |
④ | 1.070 | 0.800 |
上述实验①②③④所用铁锈均不含杂质,且实验数据可靠。通过计算,分析和比较上表4组数据,给出结论。
14-15高三上·上海黄浦·期末 查看更多[1]
(已下线)上海市黄浦区2014届高三上学期期末考试(即一模)化学试题
更新时间:2020-03-24 08:53:28
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在日常生活和工业生产中有重要应用.
Ⅰ.2022年6月,“神舟十四号”载人飞船顺利进入预定轨道,发射飞船的火箭用偏二甲肼 做燃料,四氧化二氮
做燃料,四氧化二氮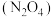 作推进剂,回答下列问题:
作推进剂,回答下列问题:
(1) 中含有的N原子数为
中含有的N原子数为__________ ,与__________  中含有的N原子数相同.
中含有的N原子数相同.
Ⅱ.阅读下面一段材料并回答问题.
【化学式】
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温卡稳定,在强碱溶液中稳定,随着 减小,稳定性下降,与水反应放出氧气.
减小,稳定性下降,与水反应放出氧气. 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质.
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质. 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用
胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化 水投放
水投放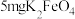 即可达到卫生标准
即可达到卫生标准
……
(2) 中铁元素的化合价为
中铁元素的化合价为__________ .
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是__________ .
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)工业制备 需要在碱性环境下进行,现提供反应体系中7种物质,
需要在碱性环境下进行,现提供反应体系中7种物质,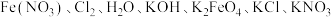 请写出制备
请写出制备 的化学反应方程式
的化学反应方程式__________ .
(5)将 与水反应的化学方程式补充完整并配平:
与水反应的化学方程式补充完整并配平:__________
__________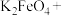 __________
__________ __________
__________ (胶体)+__________+__________
(胶体)+__________+__________
该反应消耗 时,转移的电子数为
时,转移的电子数为__________
(6)消毒净化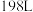 水,按照卫生标准投入
水,按照卫生标准投入 ,则
,则 与水充分反应后产生的
与水充分反应后产生的 质量为
质量为__________ g.
Ⅰ.2022年6月,“神舟十四号”载人飞船顺利进入预定轨道,发射飞船的火箭用偏二甲肼
 做燃料,四氧化二氮
做燃料,四氧化二氮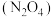 作推进剂,回答下列问题:
作推进剂,回答下列问题:(1)
 中含有的N原子数为
中含有的N原子数为 中含有的N原子数相同.
中含有的N原子数相同.Ⅱ.阅读下面一段材料并回答问题.
高铁酸钾使用说明书
【化学式】

【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温卡稳定,在强碱溶液中稳定,随着
 减小,稳定性下降,与水反应放出氧气.
减小,稳定性下降,与水反应放出氧气. 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质.
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质. 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用
胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化
 水投放
水投放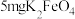 即可达到卫生标准
即可达到卫生标准……
(2)
 中铁元素的化合价为
中铁元素的化合价为(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)工业制备
 需要在碱性环境下进行,现提供反应体系中7种物质,
需要在碱性环境下进行,现提供反应体系中7种物质,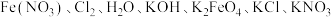 请写出制备
请写出制备 的化学反应方程式
的化学反应方程式(5)将
 与水反应的化学方程式补充完整并配平:
与水反应的化学方程式补充完整并配平:__________
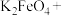 __________
__________ __________
__________ (胶体)+__________+__________
(胶体)+__________+__________
该反应消耗
 时,转移的电子数为
时,转移的电子数为(6)消毒净化
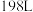 水,按照卫生标准投入
水,按照卫生标准投入 ,则
,则 与水充分反应后产生的
与水充分反应后产生的 质量为
质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)某无色溶液只含有Na+、Ba2+、Al3+、Fe3+、Br-、SO42-、CO32-中两种或多种离子,取少量逐滴滴入NaOH溶液至过量,先出现白色沉淀后消失的现象;另取少量往其中滴加氯水,溶液为橙黄色;则原溶液一定不存在__________ (填离子符号)。写出原溶液加入过量的NaOH溶液反应的离子方程式_______________ 。
(2)KClO3和浓盐酸在一定温度下的化学方程式为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。浓盐酸在反应中表现出来的性质是__________ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性。
反应中,若氧化产物比还原产物多0.1mol,则电子转移的物质的量为__________ mol。
(2)KClO3和浓盐酸在一定温度下的化学方程式为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性。
反应中,若氧化产物比还原产物多0.1mol,则电子转移的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(方程式未配平,不考虑2NO2 N2O4)。
N2O4)。
(1)0.004molCu被硝酸完全溶解后,Cu失去的电子数是_______ NA,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是__________ ,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为____________ 。
(2)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式___________________ 。
 N2O4)。
N2O4)。(1)0.004molCu被硝酸完全溶解后,Cu失去的电子数是
(2)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列八种物质,其合金用量最大、用途最广的是______________ (填字母代号,下同),做红色油漆和涂料的是____________ ,做干燥剂的是____________ ,做漂白剂的是____________ 。
A.铁 B.氧化铁 C.次氯酸钠 D.硅胶
E.铜 F.四氧化三铁 G.硫酸铝钾 H.硅酸钠
A.铁 B.氧化铁 C.次氯酸钠 D.硅胶
E.铜 F.四氧化三铁 G.硫酸铝钾 H.硅酸钠
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】由地壳中含量最高的金属元素和非金属组成的化合物的名称是________ ,铁红常用于制造红色油漆和涂料,它的化学式是____________ .
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在 溶液中加入
溶液中加入 ,调节溶液
,调节溶液 ,可以得到不同沉淀。
,可以得到不同沉淀。 ,得到沉淀
,得到沉淀 ;
; ,得到沉淀
,得到沉淀 。
。 在氧气中加热升温过程中固体的质量变化如图:
在氧气中加热升温过程中固体的质量变化如图:

(1)配制 溶液时,不能将
溶液时,不能将 固体直接溶于水,而是将固体溶于浓硝酸中,然后加水稀释,其目的是
固体直接溶于水,而是将固体溶于浓硝酸中,然后加水稀释,其目的是______________ 。
(2)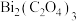 在热水中会与水反应生成
在热水中会与水反应生成 ,该反应的化学方程式是
,该反应的化学方程式是____________ 。
(3) 在足量的氧气中加热至300℃时,所得的固体残留物为
在足量的氧气中加热至300℃时,所得的固体残留物为 ,测得所得气体中仅含有
,测得所得气体中仅含有 、
、______ 和______ 等三种气体(填化学式)。
(4)根据以上实验数据计算,确定 中x的值
中x的值_______ (写出计算过程)。
 溶液中加入
溶液中加入 ,调节溶液
,调节溶液 ,可以得到不同沉淀。
,可以得到不同沉淀。 ,得到沉淀
,得到沉淀 ;
; ,得到沉淀
,得到沉淀 。
。 在氧气中加热升温过程中固体的质量变化如图:
在氧气中加热升温过程中固体的质量变化如图:
(1)配制
 溶液时,不能将
溶液时,不能将 固体直接溶于水,而是将固体溶于浓硝酸中,然后加水稀释,其目的是
固体直接溶于水,而是将固体溶于浓硝酸中,然后加水稀释,其目的是(2)
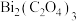 在热水中会与水反应生成
在热水中会与水反应生成 ,该反应的化学方程式是
,该反应的化学方程式是(3)
 在足量的氧气中加热至300℃时,所得的固体残留物为
在足量的氧气中加热至300℃时,所得的固体残留物为 ,测得所得气体中仅含有
,测得所得气体中仅含有 、
、(4)根据以上实验数据计算,确定
 中x的值
中x的值
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】煤燃烧产生的SO2是形成酸雨的重要原因之一,工业上可采用多种方法减少SO2的排放。回答下列问题:
(1)酸雨的形成过程中,SO2发生的反应方程式为_______ 。
(2)利用“双碱法”除去烟气中的SO2。先将SO2通入NaOH溶液,再加入CaO可使NaOH再生。
NaOH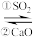 Na2SO3,写出过程①的离子方程式:
Na2SO3,写出过程①的离子方程式:_______ 。
(3)对煤进行预处理是减少SO2排放的重要手段。
①在煤中添加适量生石灰,可使煤燃烧过程中产生的SO2转化为硫酸钙,该反应的化学方程式为_______ ,检验脱硫废气中还含有SO2的方法是_______ 。
②煤炭中硫以FeS2形式存在。可以采用微生物脱硫技术除去:
FeS2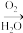 Fe2+、SO
Fe2+、SO
 Fe3+、SO
Fe3+、SO
24g FeS2完全转化为Fe3+和SO 时,消耗的O2在标准状况下的体积为
时,消耗的O2在标准状况下的体积为_______ L。
(4)为测定制得的 的纯度,称取
的纯度,称取 样品,配成
样品,配成 酸性溶液,取出
酸性溶液,取出 ,加入适量
,加入适量 和
和 溶液,加热使
溶液,加热使 全部氧化成
全部氧化成 ,用
,用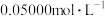 的
的 溶液滴定冷却后的含锰溶液至终点(滴定过程中
溶液滴定冷却后的含锰溶液至终点(滴定过程中 被还原为
被还原为 ),用去
),用去 溶液
溶液 ,计算该
,计算该 样品的纯度(写出计算过程)
样品的纯度(写出计算过程) _______ 。
(1)酸雨的形成过程中,SO2发生的反应方程式为
(2)利用“双碱法”除去烟气中的SO2。先将SO2通入NaOH溶液,再加入CaO可使NaOH再生。
NaOH
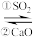 Na2SO3,写出过程①的离子方程式:
Na2SO3,写出过程①的离子方程式:(3)对煤进行预处理是减少SO2排放的重要手段。
①在煤中添加适量生石灰,可使煤燃烧过程中产生的SO2转化为硫酸钙,该反应的化学方程式为
②煤炭中硫以FeS2形式存在。可以采用微生物脱硫技术除去:
FeS2
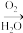 Fe2+、SO
Fe2+、SO
 Fe3+、SO
Fe3+、SO
24g FeS2完全转化为Fe3+和SO
 时,消耗的O2在标准状况下的体积为
时,消耗的O2在标准状况下的体积为(4)为测定制得的
 的纯度,称取
的纯度,称取 样品,配成
样品,配成 酸性溶液,取出
酸性溶液,取出 ,加入适量
,加入适量 和
和 溶液,加热使
溶液,加热使 全部氧化成
全部氧化成 ,用
,用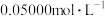 的
的 溶液滴定冷却后的含锰溶液至终点(滴定过程中
溶液滴定冷却后的含锰溶液至终点(滴定过程中 被还原为
被还原为 ),用去
),用去 溶液
溶液 ,计算该
,计算该 样品的纯度(写出计算过程)
样品的纯度(写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是某企业设计的硫酸-磷肥-水泥联产、海水-淡水多用、盐-热-电联产的三大生态产业链流程图:。

根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤可以实现能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①__________ 、②__________ 、③_________ 、④________ 、⑤__________ 。
(2)沸腾炉中发生反应的化学方程式为______________________ 。磷肥厂的主要产品是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙的化学方程式为____________ 。
(3)用1t硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸___________ t。
(4)热电厂的冷却水是___________ ,该流程中浓缩盐水除提取盐以外还可提取的物质有___________ (写出一种即可)。
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。___________ ,___________ (写出两点即可)。

根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤可以实现能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①
(2)沸腾炉中发生反应的化学方程式为
(3)用1t硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸
(4)热电厂的冷却水是
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。
您最近一年使用:0次

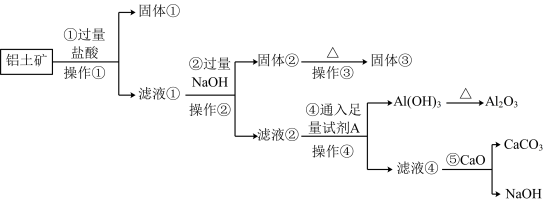
 ,还含有
,还含有 、
、 )提取氧化铝做冶炼铝的原料(纯净的
)提取氧化铝做冶炼铝的原料(纯净的