20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构。用价层电子对互斥理论(VSEPR)判断下列分子或离子的空间构型
| 分子或 离子 | BeCl2 | H3O+ | ClO4- |
| 空间 构型 |
更新时间:2020-03-28 14:09:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1) 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中的阴离子空间构型是
中的阴离子空间构型是_______ ,中心原子的杂化形式为_______ 。
(2)根据价层电子对互斥理论, 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
(3)《中华本草》等中医典籍中,记载了炉甘石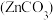 入药,可用于治疗皮肤炎症或表面创伤.
入药,可用于治疗皮肤炎症或表面创伤. 中,阴离子空间构型为
中,阴离子空间构型为_______ ,C原子的杂化形式为_______ 。
(4) X射线衍射测定等发现, 中存在
中存在 离子,
离子, 离子的几何构型为
离子的几何构型为_______ ,中心原子的杂化形式为_______ 。
 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中的阴离子空间构型是
中的阴离子空间构型是(2)根据价层电子对互斥理论,
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(3)《中华本草》等中医典籍中,记载了炉甘石
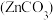 入药,可用于治疗皮肤炎症或表面创伤.
入药,可用于治疗皮肤炎症或表面创伤. 中,阴离子空间构型为
中,阴离子空间构型为(4) X射线衍射测定等发现,
 中存在
中存在 离子,
离子, 离子的几何构型为
离子的几何构型为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1) X射线衍射测定等发现, 中存在
中存在 。
。 的空间结构为
的空间结构为_______ ,中心原子的杂化形式为_______ 。
(2)我国科学家最近成功合成了世界上首个五氮阴离子盐 (用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
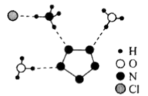
回答下列问题:
①从结构角度分析,R中两种阳离子的相同之处为_______ ,不同之处为_______ 。
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.空间结构
D.共价键类型
②R中阴离子 中的
中的 键总数为
键总数为_______ 。分子中的大 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为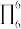 ),则
),则 中的大
中的大 键应表示为
键应表示为_______ 。
 中存在
中存在 。
。 的空间结构为
的空间结构为(2)我国科学家最近成功合成了世界上首个五氮阴离子盐
 (用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
回答下列问题:
①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.空间结构
D.共价键类型
②R中阴离子
 中的
中的 键总数为
键总数为 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为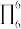 ),则
),则 中的大
中的大 键应表示为
键应表示为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g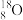 中含有的中子数为NA
中含有的中子数为NA
D.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g
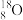 中含有的中子数为NA
中含有的中子数为NAD.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
您最近半年使用:0次
【推荐1】I.铁(26Fe)、镍(28Ni)的单质及其化合物在医药、材料等领域有广泛的应用。回答下列问题:
(1)基态Fe原子核外电子排布式为______ ,Ni位于元素周期表的_______ 区。
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是______ 。
II.回答下列问题:
(3)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为______ ,中心原子的杂化方式为_______ ,COCl2中心原子的VSEPR模型为_______ ,COCl2分子的空间构型为______ 。
(4)As4O6的分子结构如图所示,其中As原子的杂化方式为______ 。

(5)AlH 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为_____ ;列举与AlH 空间构型相同的一种离子和一种分子:
空间构型相同的一种离子和一种分子:______ 、______ (填化学式)。
(6)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为_______ ,SnBr2分子中Br-Sn-Br的键角_______ 120°(填“>”“<”或“=”)。
(1)基态Fe原子核外电子排布式为
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是
II.回答下列问题:
(3)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(4)As4O6的分子结构如图所示,其中As原子的杂化方式为

(5)AlH
 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为 空间构型相同的一种离子和一种分子:
空间构型相同的一种离子和一种分子:(6)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1) X射线衍射测定等发现, 中存在
中存在 。
。 的空间结构为
的空间结构为_______ ,中心原子的杂化形式为_______ 。
(2)我国科学家最近成功合成了世界上首个五氮阴离子盐 (用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

回答下列问题:
①从结构角度分析,R中两种阳离子的相同之处为_______ ,不同之处为_______ 。
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.空间结构
D.共价键类型
②R中阴离子 中的
中的 键总数为
键总数为_______ 。分子中的大 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为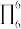 ),则
),则 中的大
中的大 键应表示为
键应表示为_______ 。
 中存在
中存在 。
。 的空间结构为
的空间结构为(2)我国科学家最近成功合成了世界上首个五氮阴离子盐
 (用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
回答下列问题:
①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.空间结构
D.共价键类型
②R中阴离子
 中的
中的 键总数为
键总数为 键可用符号
键可用符号 表示,其中
表示,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为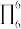 ),则
),则 中的大
中的大 键应表示为
键应表示为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】硒化锌是一种透明黄色半导体,也可作红外光学材料,熔点1520℃。
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性Se
(3)H2Se的分子构型是
(4)H2O的沸点
(5)晶体Zn为六方最密堆积,其配位数是
(6)在硒化锌ZnSe晶胞中,Se2—离子作面心立方最密堆积,且Se2—与Se2—之间的最短距离为a nm,则晶胞边长为
(7)假设阿伏伽德罗常数值为NA,则144g 硒化锌ZnSe晶体中的晶胞数是
您最近半年使用:0次



