常温下,氧化性强弱顺序为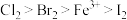 ,下列说法正确的是( )
,下列说法正确的是( )
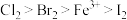 ,下列说法正确的是( )
,下列说法正确的是( )A.在溶液中 可以将 可以将 氧化: 氧化: |
B.将足量的 通入 通入 溶液中,只发生反应 溶液中,只发生反应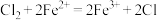 |
C. 和 和 都可以将 都可以将 氧化成 氧化成 ,而I2不能 ,而I2不能 |
D.I-可以被 还原成I2 还原成I2 |
更新时间:2020-03-26 15:23:41
|
相似题推荐
【推荐1】向FeI2,FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:2Fe2++Br2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是。
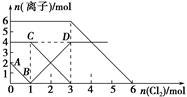

| A.线段BD表示Fe3+物质的量的变化 |
| B.原混合溶液中FeI2的物质的量为1mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶3∶1 |
您最近一年使用:0次
【推荐2】已知反应:
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3。
下列说法正确的是
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3。
下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.氧化性由强到弱顺序为KBrO3>KClO3>Cl2>Br2 |
| C.反应②中氧化剂和还原剂的物质的量之比为1∶6 |
| D.反应③中若有1 mol还原剂参加反应,则氧化剂得到电子的物质的量为5 mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】室温下,下列实验探究方案能达到探究目的的是
| 选项 | 实验探究方案 | 探究目的 |
| A | 用pH计测量相同浓度CH3COONa和Na2CO3溶液的pH | 比较CH3COOH和H2CO3的酸性 |
| B | 将铁锈溶于浓盐酸,再向溶液中滴入几滴KMnO4溶液,观察溶液颜色变化 | 铁锈中含有二价铁 |
| C | 常温下,向10mL0.1mol·L-1NaCl溶液中滴加5滴0.1mol·L-1AgNO3溶液,充分反应后,再滴加5滴0.1mol·L-1KI溶液,观察沉淀颜色变化 | Ksp(AgCl)>Ksp(AgI) |
| D | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液,观察溶液颜色 | 氧化性:H2O2>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
| 粒子组 | 判断和分析 | |
| A |     | 能大量共存,粒子间不反应 |
| B |     |  和 和 因双水解而不能共存 因双水解而不能共存 |
| C |      | 粒子可以量共存 |
| D |     | 粒子因产生 沉淀而不能共存 沉淀而不能共存 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】酸性 溶液和
溶液和 混合时,发生的反应如下:
混合时,发生的反应如下: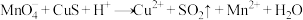 (未配平),下列有关该反应的说法中正确的是
(未配平),下列有关该反应的说法中正确的是
 溶液和
溶液和 混合时,发生的反应如下:
混合时,发生的反应如下: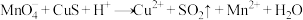 (未配平),下列有关该反应的说法中正确的是
(未配平),下列有关该反应的说法中正确的是A.被氧化的元素是 和 和 |
B. 的还原性强于 的还原性强于 的还原性 的还原性 |
C.氧化剂与还原剂的物质的量之比为 |
D.若生成 (标准状况下) (标准状况下) ,转移电子的物质的量是 ,转移电子的物质的量是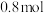 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】已知酸性 溶液可与
溶液可与 反应生成
反应生成 和
和 。现将硫酸酸化的
。现将硫酸酸化的 溶液与
溶液与 溶液混合,充分反应后再向所得溶液中加入
溶液混合,充分反应后再向所得溶液中加入 溶液,混合溶液中
溶液,混合溶液中 的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中正确的是
的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中正确的是

 溶液可与
溶液可与 反应生成
反应生成 和
和 。现将硫酸酸化的
。现将硫酸酸化的 溶液与
溶液与 溶液混合,充分反应后再向所得溶液中加入
溶液混合,充分反应后再向所得溶液中加入 溶液,混合溶液中
溶液,混合溶液中 的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中正确的是
的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中正确的是
A.图中 段的氧化剂为 段的氧化剂为 |
B.图中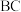 段发生的反应为 段发生的反应为 |
C. 与 与 反应的方程式中二者系数之比为 反应的方程式中二者系数之比为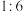 |
D.开始加入的 为 为 |
您最近一年使用:0次
【推荐2】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示生成一种含氧酸(HIO3),且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是( )
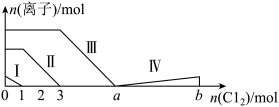

| A.线段Ⅱ表示Fe2+的变化情况 |
| B.线段Ⅳ发生反应的离子方程式为:I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O |
| C.根据图象可计算a=6 |
| D.原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列反应对应的离子方程式书写正确的是 ( )
| A.向FeBr2溶液中通入等物质的量Cl2: 2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
B.以惰性电极电解AlCl3水溶液: 2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
| C.向Ca(ClO)2溶液中通入少量SO2 : Ca2++ClO-+H2O+SO2=Cl-+CaSO4↓+2H+ |
D.饱和碳酸钠溶液中通入足量的二氧化碳: 2Na++CO +CO2+H2O=2NaHCO3↓ +CO2+H2O=2NaHCO3↓ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】向200mL1.5mol·L-lFeBr2溶液中逐渐通入Cl2,其中n(Fe2+)、n(Br-)随通入Cl2的物质的量n(Cl2)变化如图所示,下列说法错误的是


| A.①代表Fe2+,②代表Br- |
| B.还原性强弱:Fe2+>Br- |
| C.n(Cl2)=0.35mol时,溶液中c(Fe3+)=c(Br-) |
| D.n(Cl2)=0.45mol时,总的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次

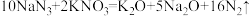 。若氧化产物比还原产物多
。若氧化产物比还原产物多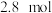 ,则下列判断正确的是
,则下列判断正确的是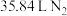 (标准状况)
(标准状况)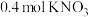 被氧化
被氧化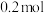

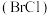 属于卤素互化物,性质与卤素相似,下列推测
属于卤素互化物,性质与卤素相似,下列推测 比
比 强
强 反应生成
反应生成


