下列有关说法正确的是
| A.反应CaC2(s)+N2(g)=CaCN2(s)+C(s)能自发进行,则该反应ΔS>0 |
| B.常温下向0.1 mol·L-1CH3COOH溶液中通入少量HCl气体,c(H+)·c(CH3COO-)增大 |
| C.将1 mol Cl2溶于水中,反应中转移的电子数为6.02×1023个 |
| D.2H2(g)+O2(g)=2H2O(g)的反应物键能总和大于生成物键能总和 |
更新时间:2020-03-26 19:45:39
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】以 、
、 为原料生产重要的高效氮肥—尿素[CO(NH2)2],反应过程中能量(
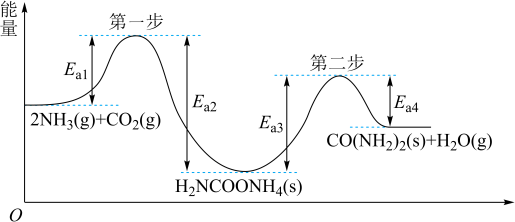
为原料生产重要的高效氮肥—尿素[CO(NH2)2],反应过程中能量(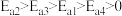 )变化如图所示,下列说法正确的是
)变化如图所示,下列说法正确的是
 、
、 为原料生产重要的高效氮肥—尿素[CO(NH2)2],反应过程中能量(
为原料生产重要的高效氮肥—尿素[CO(NH2)2],反应过程中能量(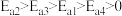 )变化如图所示,下列说法正确的是
)变化如图所示,下列说法正确的是
A.由图知 和 和 在一定条件下发生有效碰撞直接生成了 在一定条件下发生有效碰撞直接生成了 和 和 |
| B.第二步反应是合成尿素的决速步骤 |
| C.该过程的总反应在高温条件下有利于自发进行 |
D.合成尿素的热化学方程式为  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】关于下列各图的叙述中,不正确的是
 |  |  |  |
| ① | ② | ③ | ④ |
| A.图①所示曲线,表示该反应是放热反应 |
| B.图②所示柱形图,纵坐标表示第二周期元素最高正价随原子序数的变化 |
| C.用装置③可进行钾在空气中燃烧实验,验证钾比钠活泼 |
| D.装置④为原电池,总反应是:Fe+2Fe3+=3Fe2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】一种以太阳能为热源分解水的历程,如图所示:
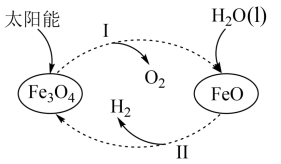
已知:2H2O(l)=2H2(g)+O2(g) △H=571.0 kJ·mol-1
过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=313.2 kJ·mol-1
下列说法错误的是

已知:2H2O(l)=2H2(g)+O2(g) △H=571.0 kJ·mol-1
过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=313.2 kJ·mol-1
下列说法错误的是
| A.过程I、II中能量转化的形式依次是:太阳能→化学能→热能 |
| B.转化过程中Fe3O4作催化剂 |
| C.破坏2 mol液态水中化学键所需能量高于形成2 mol氢气和1 mol氧气中化学键释放的能量 |
| D.过程II热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=128.9 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在不同浓度(c)、不同温度(T)下,某物质发生分解的瞬时反应速率如下表所示:
下列推断正确的是
| c/mol·L-1 v/mol·L-1·s-1 T/K | 1.00 | 0.08 | 0.06 | 0.04 |
| 273.15 | 3.00 | 2.40 | 1.80 | 1.20 |
| 298.15 | 6.00 | 5.00 | 4.00 | 3.00 |
| T3 | 5.40 | 5.04 | 4.68 | 4.32 |
| A.T3<273.15 |
| B.同时改变起始浓度和温度,瞬时速率可能相等 |
| C.该物质最适宜的分解条件是,温度为298.15 K,起始浓度为 1.0 mol·L-1 |
| D.该分解反应一定是熵增、焓增反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】向刚性容器中,按物质的量之比为3:1充入H2和CO2发生反应:2CO2(g)+6H2(g)  C2H4(g)+4H2O(g)。反应相同时间,CO2(g)的转化率随温度的变化关系如图所示,下列说法错误的是
C2H4(g)+4H2O(g)。反应相同时间,CO2(g)的转化率随温度的变化关系如图所示,下列说法错误的是

 C2H4(g)+4H2O(g)。反应相同时间,CO2(g)的转化率随温度的变化关系如图所示,下列说法错误的是
C2H4(g)+4H2O(g)。反应相同时间,CO2(g)的转化率随温度的变化关系如图所示,下列说法错误的是
| A.H2(g)的转化率随温度的变化关系图与上图完全相同 |
| B.该反应在低温下能自发进行 |
C.T2℃时容器内压强为p0,该反应的Kp=( )3 )3 |
| D.M、N两点时容器内压强相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】2021年1月20日中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转化为甲烷的新型催化转化方法:CO2+4H2=CH4+2H2O,这是迄今最接近人造光合作用的方法。CO2加氢制CH4的一种催化机理如图,下列说法正确的是
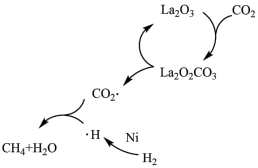

| A.反应中La2O3是中间产物 |
| B.反应中La2O2CO3可以释放出带负电荷的CO2· |
| C.H2经过Ni活性中心裂解产生活化态H·的过程中ΔS>0 |
| D.使用TiO2作催化剂可以降低反应的焓变,从而提高化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列措施能够使水的离子积常数增大的是( )
| A.温度不变,加入一定量的硫酸 | B.温度不变,加入一定量的NaOH |
C.升高温度 | D.降低温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】醋酸的电离方程式为CH3COOH(aq)⇌H+(aq)+CH3COO-(aq) ΔH>0,25℃时,0.1mol/L醋酸溶液Ka=1.75×10-5(Ka表示酸的电离常数)。下列说法正确的是
| A.升高温度,c(H+)增大,Ka变大 |
| B.该溶液中加少量CH3COONa固体,平衡正向移动 |
| C.该温度下0.01mol/L醋酸溶液Ka<1.75×10-5 |
| D.向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小 |
您最近一年使用:0次

 ,下列说法正确的是
,下列说法正确的是 固体,温度保持不变,平衡常数减小
固体,温度保持不变,平衡常数减小 浓度增大
浓度增大

