0.80gCuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
请回答下列问题:
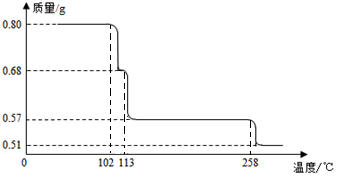
(1)试通过计算确定200℃时固体物质的化学式__________ ;
(2)取270℃所得样品,于570℃灼烧得到的两种产物,黑色粉末和气体,该反应的化学方程式为___________ 。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体存在的最高温度是_____________ 。
请回答下列问题:

(1)试通过计算确定200℃时固体物质的化学式
(2)取270℃所得样品,于570℃灼烧得到的两种产物,黑色粉末和气体,该反应的化学方程式为
19-20高二·浙江·阶段练习 查看更多[1]
(已下线)【新东方】高中化学X007
更新时间:2020-04-01 04:13:55
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】把2.0mol/L CuSO4溶液和2.0mol/L H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。则:
(1)混合溶液中H+、Cu2+、 的物质的量浓度分别为:
的物质的量浓度分别为:____________ ;
(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为___________ ;
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式______ ,并计算残渣的质量__________ (不计操作带来的损失)。
(1)混合溶液中H+、Cu2+、
 的物质的量浓度分别为:
的物质的量浓度分别为:(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将5.6 g 铁粉放入100 mL CuSO4溶液中,充分反应后,再向溶液中加入足量的稀硫酸,又产生1.12 L气体(标准状况下)。试计算:
(1)最后所得溶液中FeSO4的物质的量__________ ;
(2)原CuSO4溶液的物质的量浓度__________ 。
(1)最后所得溶液中FeSO4的物质的量
(2)原CuSO4溶液的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸铜晶体受热脱水是分步进行的。现取1.60gCuSO4·5H2O样品,在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。
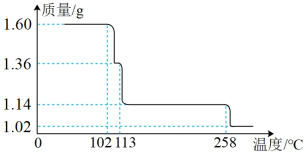
请回答下列问题:
(1)试确定200℃时:①固体物质的化学式___ ;
②写出推断计算过程:___ 。
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉未和一种氧化性气体,该反应的化学方程式为___ 。把该黑色粉未溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为___ ,其存在的最高温度是___ ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为___ 。

请回答下列问题:
(1)试确定200℃时:①固体物质的化学式
②写出推断计算过程:
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉未和一种氧化性气体,该反应的化学方程式为
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】多钒酸盐在催化、医学等领域有着重要的应用。某多钒酸铵晶体的化学式为(NH4)xH6-xV10O28·10H2O。为测定其组成, 进行下列实验:
①称取样品0.9291 g,加入过量20% NaOH溶液,加热煮沸一段时间,生成的NH3用50.00 mL 0.1000 mol·L-1 盐酸吸收。加入指示剂,用0.1000 mol·L-1 NaOH标准溶液滴定剩余的HCl,终点时消耗NaOH标准溶液20.00 mL。
②另称取样品0. 9291 g,加过量1.5 mol·L-1 H2SO4,微热溶解。加入3 g NaHSO3,搅拌,使五价钒V10O286-完全转化为四价钒VO2+。加热煮沸一段时间,然后用0. 06000 mol·L-1 KMnO4标准溶液滴定(还原产物为Mn2+),终点时消耗KMnO4标准溶液25.00 mL。
(1)在实验②中,煮沸的目的是____ 。
(2)KMnO4滴定时,将VO2+氧化为五价的VO2+,该反应的离子方程式为____ 。
(3)根据实验结果,确定该多钒酸铵晶体的化学式。____
①称取样品0.9291 g,加入过量20% NaOH溶液,加热煮沸一段时间,生成的NH3用50.00 mL 0.1000 mol·L-1 盐酸吸收。加入指示剂,用0.1000 mol·L-1 NaOH标准溶液滴定剩余的HCl,终点时消耗NaOH标准溶液20.00 mL。
②另称取样品0. 9291 g,加过量1.5 mol·L-1 H2SO4,微热溶解。加入3 g NaHSO3,搅拌,使五价钒V10O286-完全转化为四价钒VO2+。加热煮沸一段时间,然后用0. 06000 mol·L-1 KMnO4标准溶液滴定(还原产物为Mn2+),终点时消耗KMnO4标准溶液25.00 mL。
(1)在实验②中,煮沸的目的是
(2)KMnO4滴定时,将VO2+氧化为五价的VO2+,该反应的离子方程式为
(3)根据实验结果,确定该多钒酸铵晶体的化学式。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下:
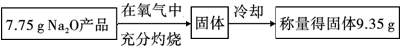
该Na2O产品中Na2O的质量分数为_______ 。

该Na2O产品中Na2O的质量分数为
您最近一年使用:0次

 溶液,取其中
溶液,取其中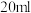 加入
加入
 溶液,得到
溶液,得到 沉淀(不考虑其他沉淀的生成),再用
沉淀(不考虑其他沉淀的生成),再用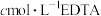 标准溶液滴定剩余
标准溶液滴定剩余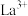 (
( 与
与 按
按 配合),消耗
配合),消耗 ,则氟化稀土样品中氟的质量分数为
,则氟化稀土样品中氟的质量分数为

