正丁醚是一种用途很广的化工产品,毒性和危险性小,是安全性很高的有机溶剂,对许多天然及合成油脂、树脂、橡胶、有机酸酯、生物碱等都有很强的溶解能力,还可作为电子级清洗剂和多种有机合成材料。可通过以下反应原理制取正丁醚:
2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
已知相关物质的部分信息如下:
某课外化学学习小组查阅相关资料设计了以下实验步骤合成正丁醚:
①在100 mL两口烧瓶中加入30.0 mL正丁醇、5.0 mL浓硫酸和几粒沸石,充分摇匀。在分水器中加入3.0 mL饱和食盐水,按图甲组装仪器,接通冷凝水;
②反应:在电热套上加热,使瓶内液体微沸,回流反应约1小时。当馏液充满分水器时,打开分水器放出一部分水。当水层不再变化,瓶中反应温度达150℃,反应已基本完成,停止加热;
③蒸馏:待反应液冷却后,拆下分水器,将仪器改成蒸馏装置如图丙,再加几粒沸石,蒸馏,收集馏分;
④精制:将馏出液倒入盛有10 mL水的分液漏斗中,充分振摇,静置弃去水液,有机层依次用5 mL水,3 mL 5% NaOH溶液、3 mL水和3 mL饱和氯化钙溶液洗涤,分去水层,将产物放入洁净干燥的小锥形瓶中,然后加入0.2~0.4 9无水氯化钙,再将液体转入装置丙中进行蒸馏,收集到馏分9.0 mL。
甲.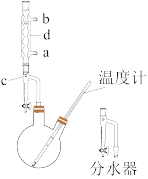 乙.
乙. 丙.
丙.
请根据以上操作回答下列问题:
(1)制备正丁醚的反应类型是___ ,仪器d的名称是____ 。
(2)在步骤①中添加试剂的顺序是____ 。相比装置乙,装置甲的优点是___ 。
(3)在步骤②中采用电热套加热而不采用酒精灯直接加热的原因可能是____ 。
(4)在步骤③中收集馏分适宜的温度范围为____ (填正确答案标号)。
A.115℃~ll9℃B.140℃~144℃C. 148℃~152℃
(5)在精制中,有机层在____ 层(填“上”或“下”),加入无水氯化钙的作用是____ 。
(6)本小组实验后所得正丁醚的产率约为___ %(计算结果保留一位小数)。
2CH3CH2CH2CH2OH
 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O已知相关物质的部分信息如下:
| 沸点(℃) | 密度(g/cm3) | 溶解度(g) | 相对分子质量 | |
| 正丁醇 | 117.7 | 0.81 | 7.9 | 74 |
| 正丁醚 | 142 | 0.77 | 不溶于水 | 130 |
①在100 mL两口烧瓶中加入30.0 mL正丁醇、5.0 mL浓硫酸和几粒沸石,充分摇匀。在分水器中加入3.0 mL饱和食盐水,按图甲组装仪器,接通冷凝水;
②反应:在电热套上加热,使瓶内液体微沸,回流反应约1小时。当馏液充满分水器时,打开分水器放出一部分水。当水层不再变化,瓶中反应温度达150℃,反应已基本完成,停止加热;
③蒸馏:待反应液冷却后,拆下分水器,将仪器改成蒸馏装置如图丙,再加几粒沸石,蒸馏,收集馏分;
④精制:将馏出液倒入盛有10 mL水的分液漏斗中,充分振摇,静置弃去水液,有机层依次用5 mL水,3 mL 5% NaOH溶液、3 mL水和3 mL饱和氯化钙溶液洗涤,分去水层,将产物放入洁净干燥的小锥形瓶中,然后加入0.2~0.4 9无水氯化钙,再将液体转入装置丙中进行蒸馏,收集到馏分9.0 mL。
甲.
 乙.
乙. 丙.
丙.
请根据以上操作回答下列问题:
(1)制备正丁醚的反应类型是
(2)在步骤①中添加试剂的顺序是
(3)在步骤②中采用电热套加热而不采用酒精灯直接加热的原因可能是
(4)在步骤③中收集馏分适宜的温度范围为
A.115℃~ll9℃B.140℃~144℃C. 148℃~152℃
(5)在精制中,有机层在
(6)本小组实验后所得正丁醚的产率约为
更新时间:2020-04-04 22:29:30
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】已知:①具有一个甲基支链的化合物A的分子式为C4H6O2,A可以使Br2的四氯化碳溶液褪色,1molA和1mol NaHCO3能完全反应。②化合物B含有C、H、O三种元素,相对分子质量为60,其中碳的质量分数为60%,氢的质量分数为13.3% 。B在催化剂Cu的作用下被氧气氧化成C,C能发生银镜反应。③A和B在浓硫酸加热条件下可生成有水果香味的D。回答下列问题:
(1)写出与A具有相同官能团的A的所有同分异构体的结构简式:______
(2)C所具有的官能团名称为______
(3)A和B生成D的化学方程式是:______
(1)写出与A具有相同官能团的A的所有同分异构体的结构简式:
(2)C所具有的官能团名称为
(3)A和B生成D的化学方程式是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】乳酸乙酯E是白酒香气的成分之一,广泛用作食品香精,适量添加可增加白酒中酯的浓度,增加白酒的香气。已知乳酸乙酯能发生如图的变化(其中A烃是衡量一个国家石油化工发展水平的重要标志)。
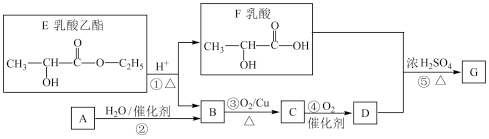
(1)F中官能团的名称为_______ 。
(2)③的化学方程式是_______ 。
(3)F和D反应生成G的化学方程式为_______ ,反应类型为_______ 。
(4)绿色化学的核心内容之一是“原子经济性”,即原子的理论利用率为100%。下列转化过程符合绿色化学要求的是_______ (填序号)。
a.上图中反应① b.甲烷制备 c.
c.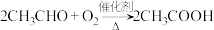
(5)1mol乳酸与足量金属 反应,消耗金属
反应,消耗金属 的质量为
的质量为_______ g。

(1)F中官能团的名称为
(2)③的化学方程式是
(3)F和D反应生成G的化学方程式为
(4)绿色化学的核心内容之一是“原子经济性”,即原子的理论利用率为100%。下列转化过程符合绿色化学要求的是
a.上图中反应① b.甲烷制备
 c.
c.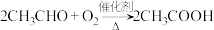
(5)1mol乳酸与足量金属
 反应,消耗金属
反应,消耗金属 的质量为
的质量为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】氢化阿托醛 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下:
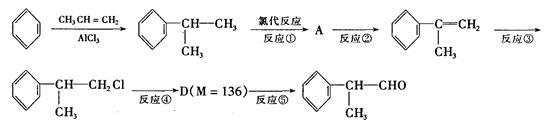
(1)在合成路线上②③的反应类型分别为②______________ ③____________ 。
(2)由 反应的化学方程式为
反应的化学方程式为_________________ 。
(3)1mol氢化阿托醛发生银镜反应最多可生成_________ molAg。
(4)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为___________________ 。D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有_________ 种。
 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下:
(1)在合成路线上②③的反应类型分别为②
(2)由
 反应的化学方程式为
反应的化学方程式为(3)1mol氢化阿托醛发生银镜反应最多可生成
(4)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硫酸铜晶体里结晶水的测定实验中,首先应将晶体放在________ 中研碎,晶体应在_________ 中加热,冷却时应将其放在___________ 中进行,如果不这样冷却则实验结果会_______ (填“偏高”或“偏低”或“无影响”)。此实验至少量______ 次。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯是一种黄绿色具有刺激性气味的气体,常用于自来水消毒和果蔬保鲜等方面。氯酸钠还原法是目前使用较为广泛的 制备方法,其中是用
制备方法,其中是用 与
与 在催化剂、
在催化剂、 时,发生反应得到
时,发生反应得到 ,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:
① 的浓度较大时易分解,实验室用稳定剂吸收
的浓度较大时易分解,实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体
一种气体
② 与KI反应的离子方程式为:
与KI反应的离子方程式为: 。
。
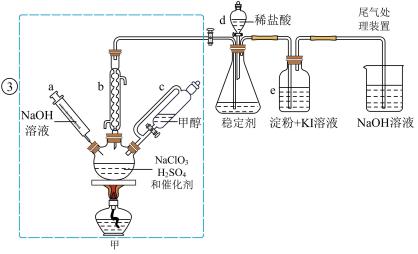
(1)仪器b在装置中的作用是______________ ;比较仪器c和d,实验中c的优点是_____________ 。
(2)制备装置甲中需改进的一项措施是________________ 。
(3)反应中甲醇被氧化为甲酸,写出制备 的化学方程式:
的化学方程式:________________ ;该制备法可选用不同的还原性物质作为还原剂,例如草酸,相比甲醇法,草酸法的优点是________________ 。
(4)下列有关说法正确的是__________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的
B.装置e主要用于检验是否有 生成
生成
C.在 释放实验中,发生的离子反应方程式是:
释放实验中,发生的离子反应方程式是: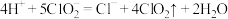
D. 和
和 都为强氧化剂,在相同条件下,等物质的量时
都为强氧化剂,在相同条件下,等物质的量时 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍
(5)自来水厂用碘量法检测水中 的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
标准溶液滴定碘单质 ,达到滴定终点时用去15.00mL
,达到滴定终点时用去15.00mL 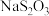 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为__________  。
。
 制备方法,其中是用
制备方法,其中是用 与
与 在催化剂、
在催化剂、 时,发生反应得到
时,发生反应得到 ,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。已知:
①
 的浓度较大时易分解,实验室用稳定剂吸收
的浓度较大时易分解,实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体
一种气体②
 与KI反应的离子方程式为:
与KI反应的离子方程式为: 。
。| 物质 |  |  |  |
| 沸点 | 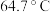 | 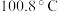 | 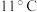 |

(1)仪器b在装置中的作用是
(2)制备装置甲中需改进的一项措施是
(3)反应中甲醇被氧化为甲酸,写出制备
 的化学方程式:
的化学方程式:(4)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的

B.装置e主要用于检验是否有
 生成
生成C.在
 释放实验中,发生的离子反应方程式是:
释放实验中,发生的离子反应方程式是: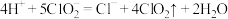
D.
 和
和 都为强氧化剂,在相同条件下,等物质的量时
都为强氧化剂,在相同条件下,等物质的量时 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍(5)自来水厂用碘量法检测水中
 的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
标准溶液滴定碘单质 ,达到滴定终点时用去15.00mL
,达到滴定终点时用去15.00mL 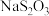 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】香豆素存在于黑香豆、香蛇鞭菊、野香荚兰、兰花中,具有新鲜干草香和香豆香,是一种口服抗凝药物。实验室合成香豆素的反应和实验装置如下:
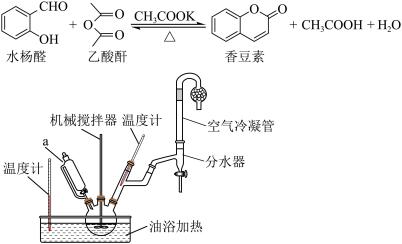
可能用到的有关性质如下:
合成反应:
向三颈烧瓶中加入95%的水杨醛38.5g、新蒸过的乙酸酐73g和1g无水乙酸 钾,然后加热升温,三颈烧瓶内温度控制在145~150℃,控制好蒸汽温度。此时,乙酸开始蒸出。当蒸出量约15g时,开始滴加15g乙酸酐,其滴加速度应与乙酸蒸出的速度相当。乙酸酐滴加完毕后,隔一定时间,发现气温不易控制在120℃时,可继续提高内温至208℃左右,并维持15min至半小时,然后自然冷却。
分离提纯:
当温度冷却至80℃左右时,在搅拌下用热水洗涤,静置分出水层,油层用10%的 碳酸钠溶液进行中和,呈微碱性,再用热水洗涤至中性,除去水层,将油层进行减压蒸馏,收集150~160℃/1866Pa馏分为粗产物。将粗产物用95%乙醇(乙醇与粗产物的质量比为1:1)进行重结晶,得到香豆素纯品35.0g。
(1)装置a的名称是_________ 。
(2)乙酸酐过量的目的是___________ 。
(3)分水器的作用是________ 。
(4)使用油浴加热的优点是________ 。
(5)合成反应中,蒸汽温度的最佳范围是_____ (填正确答案标号)。
a.100~110℃ b.117.9~127.9℃ c.139~149℃
(6)判断反应基本完全的现象是___________ 。
(7)油层用10%的碳酸钠溶液进行中和时主要反应的离子方程式为______ 。
(8)减压蒸馏时,应该选用下图中的冷凝管是_____ (填正确答案标号)。
a.直形冷凝管 b.球形冷凝管
b.球形冷凝管 c.蛇形冷凝管
c.蛇形冷凝管
(9)本实验所得到的香豆素产率是______ 。

可能用到的有关性质如下:
相对分子质量 | 熔点(℃) | 沸点(℃) | 溶解性 | |
水杨醛 | 122 | -7 | 197 | 微溶于水,溶于乙醚等有机溶剂 |
乙酸酐 | 102 | -73 | 139 | 有吸湿性,溶于氯仿和乙醚,缓慢地溶于水形成乙酸 |
香豆素 | 146 | 69 | 298 | 不溶于冷水,易溶于热水、醇、乙醚、氯仿和氢氧化钠溶液 |
乙酸 | 60 | 16.6 | 117.9 | 能溶于水、乙醇、乙醚、四氯化碳及甘油等有机溶剂 |
向三颈烧瓶中加入95%的水杨醛38.5g、新蒸过的乙酸酐73g和1g无水乙酸 钾,然后加热升温,三颈烧瓶内温度控制在145~150℃,控制好蒸汽温度。此时,乙酸开始蒸出。当蒸出量约15g时,开始滴加15g乙酸酐,其滴加速度应与乙酸蒸出的速度相当。乙酸酐滴加完毕后,隔一定时间,发现气温不易控制在120℃时,可继续提高内温至208℃左右,并维持15min至半小时,然后自然冷却。
分离提纯:
当温度冷却至80℃左右时,在搅拌下用热水洗涤,静置分出水层,油层用10%的 碳酸钠溶液进行中和,呈微碱性,再用热水洗涤至中性,除去水层,将油层进行减压蒸馏,收集150~160℃/1866Pa馏分为粗产物。将粗产物用95%乙醇(乙醇与粗产物的质量比为1:1)进行重结晶,得到香豆素纯品35.0g。
(1)装置a的名称是
(2)乙酸酐过量的目的是
(3)分水器的作用是
(4)使用油浴加热的优点是
(5)合成反应中,蒸汽温度的最佳范围是
a.100~110℃ b.117.9~127.9℃ c.139~149℃
(6)判断反应基本完全的现象是
(7)油层用10%的碳酸钠溶液进行中和时主要反应的离子方程式为
(8)减压蒸馏时,应该选用下图中的冷凝管是
a.直形冷凝管
 b.球形冷凝管
b.球形冷凝管 c.蛇形冷凝管
c.蛇形冷凝管
(9)本实验所得到的香豆素产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】环己烯是重要的化工原料。其实验室制备流程如下:
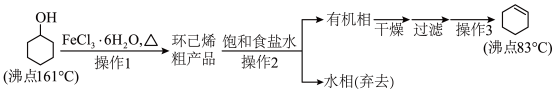
操作1的实验装置如图所示(加热和夹持装置已略去)。

回答下列问题:
(1)烧瓶A中进行反应的化学方程式为_______ ,浓硫酸也可作该反应的催化剂。相比浓硫酸,选择 作催化剂的优点是
作催化剂的优点是_______ (写出一条即可)。
(2)已知环己烯的密度为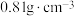 ,进行操作2前加饱和食盐水而不加蒸馏水的原因是
,进行操作2前加饱和食盐水而不加蒸馏水的原因是_______ 。
(3)操作2为分液,下列关于分液漏斗的使用,叙述正确的是_______。
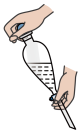
(4)操作3的步骤:安装蒸馏装置,加入待蒸馏的物质和_______ ,通冷凝水,加热,弃去前馏分,收集83℃馏分的质量为7.6g,则环己烯的产率为_______ %(已知环己醇的密度为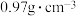 ,计算结果保留1位小数)。
,计算结果保留1位小数)。

操作1的实验装置如图所示(加热和夹持装置已略去)。

回答下列问题:
(1)烧瓶A中进行反应的化学方程式为
 作催化剂的优点是
作催化剂的优点是(2)已知环己烯的密度为
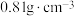 ,进行操作2前加饱和食盐水而不加蒸馏水的原因是
,进行操作2前加饱和食盐水而不加蒸馏水的原因是(3)操作2为分液,下列关于分液漏斗的使用,叙述正确的是_______。

| A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞处不漏水即可使用 |
| B.分液时环己烯应从上口倒出 |
| C.振荡萃取操作应如图所示,并打开玻璃塞不断放气 |
| D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔 |
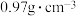 ,计算结果保留1位小数)。
,计算结果保留1位小数)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制取1,2-二溴乙烷,其中A和F中装有乙醇和浓硫酸的混合液,D中的试管里装有液溴,可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚(夹持装置已略去)。

有关数据列表如下:
填写下列空白:
(1)A中主要发生的是乙醇的脱水反应,即消去反应,请写出乙醇消去反应的化学方程式:_________________________________ 。
(2)D中发生反应的化学方程式为_________________________________ 。
(3)安全瓶B可以防止倒吸,并可以检查实验进行时导管是否发生堵塞,请写出发生堵塞时瓶B中的现象是_________________________________ 。
(4)在装置C中应加入_____ (填字母序号),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c. 氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)容器E中NaOH溶液的作用是__________________________________ 。
(6)若产物中有少量副产物乙醚,可用____________________ (填操作名称)的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是_________________________ 。

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷. | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.7 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)A中主要发生的是乙醇的脱水反应,即消去反应,请写出乙醇消去反应的化学方程式:
(2)D中发生反应的化学方程式为
(3)安全瓶B可以防止倒吸,并可以检查实验进行时导管是否发生堵塞,请写出发生堵塞时瓶B中的现象是
(4)在装置C中应加入
a.水 b.浓硫酸 c. 氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)容器E中NaOH溶液的作用是
(6)若产物中有少量副产物乙醚,可用
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】CS2是实验室常用的溶剂(熔点:-112℃,沸点:46℃,不溶于水,溶于乙醇、乙醚等多数有机溶剂)。某校课外小组的同学依据文献资料,设计实验利用CH4和S(熔点:118℃,沸点:445℃,不溶于水,易溶于CS2等有机溶剂)制取CS2并进行提纯,制备装置如下:
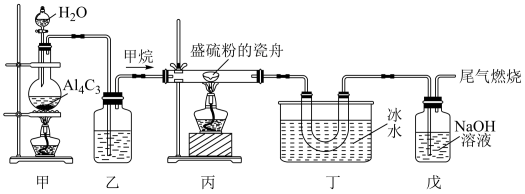
回答下列问题:
(1)装置乙中盛放的试剂为___________ ;实验开始时,首先点燃装置___________ (填“甲”或“丙”)处的酒精灯。
(2)装置丙中生成 的同时生成
的同时生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)装置戊的作用是___________ 。
(4)将装置丁中收集到的粗二硫化碳进行提纯,步骤如下:
Ⅰ.加入粉碎的高锰酸钾充分摇动,静置分离出上层液体于烧瓶中;Ⅱ.向上层液体中加少量 摇动,静置分离出上层液体于烧瓶中;Ⅲ.加入适量硫酸汞摇动,以消除臭味;Ⅳ。加入无水
摇动,静置分离出上层液体于烧瓶中;Ⅲ.加入适量硫酸汞摇动,以消除臭味;Ⅳ。加入无水 ;Ⅴ。蒸馏。
;Ⅴ。蒸馏。
①步骤Ⅰ中加入 是为了除去杂质
是为了除去杂质___________ (填化学式);步骤Ⅱ中加入 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
②下图是某学生的蒸馏操作示意图,其操作不规范的是___________ (填标号)。
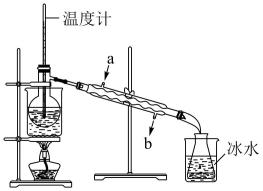
A.温度计的水银球插入液面以下 B.蒸馏烧瓶中加入碎瓷片
C.用图示冷凝管冷凝 D.水从a处进入冷凝管中
E.蒸馏烧瓶和锥形瓶分别放在热水浴和冰水浴中

回答下列问题:
(1)装置乙中盛放的试剂为
(2)装置丙中生成
 的同时生成
的同时生成 ,该反应的化学方程式为
,该反应的化学方程式为(3)装置戊的作用是
(4)将装置丁中收集到的粗二硫化碳进行提纯,步骤如下:
Ⅰ.加入粉碎的高锰酸钾充分摇动,静置分离出上层液体于烧瓶中;Ⅱ.向上层液体中加少量
 摇动,静置分离出上层液体于烧瓶中;Ⅲ.加入适量硫酸汞摇动,以消除臭味;Ⅳ。加入无水
摇动,静置分离出上层液体于烧瓶中;Ⅲ.加入适量硫酸汞摇动,以消除臭味;Ⅳ。加入无水 ;Ⅴ。蒸馏。
;Ⅴ。蒸馏。①步骤Ⅰ中加入
 是为了除去杂质
是为了除去杂质 发生反应的化学方程式为
发生反应的化学方程式为②下图是某学生的蒸馏操作示意图,其操作不规范的是

A.温度计的水银球插入液面以下 B.蒸馏烧瓶中加入碎瓷片
C.用图示冷凝管冷凝 D.水从a处进入冷凝管中
E.蒸馏烧瓶和锥形瓶分别放在热水浴和冰水浴中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下:
环己醇和环己酮的部分物理性质见下表:
现以20 mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯。分离提纯过程中涉及的主要步骤(未排序):
a.蒸馏,除去乙醚后,收集151~156℃馏分;
b.水层用乙醚(乙醚沸点34.6 ℃,易燃烧)萃取,萃取液并入有机层;
c.过滤;
d.往液体中加入NaCl固体至饱和,静置,分液;
e.加入无水MgSO4固体,除去有机物中少量水。
回答下列问题:
(1)上述分离提纯步骤的正确顺序是__________ (填字母)。
(2)b中水层用乙醚萃取的目的是_______ 。
(3)以下关于萃取分液操作的叙述中,不正确的是__________ 。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,如图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是__________ 。蒸馏除乙醚的操作中采用的加热方式为________ 。
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是______ 。

环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
a.蒸馏,除去乙醚后,收集151~156℃馏分;
b.水层用乙醚(乙醚沸点34.6 ℃,易燃烧)萃取,萃取液并入有机层;
c.过滤;
d.往液体中加入NaCl固体至饱和,静置,分液;
e.加入无水MgSO4固体,除去有机物中少量水。
回答下列问题:
(1)上述分离提纯步骤的正确顺序是
(2)b中水层用乙醚萃取的目的是
(3)以下关于萃取分液操作的叙述中,不正确的是
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,如图用力振荡

B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】对氯苯氧乙酸是植物生长调节剂的中间体,实验室合成如下。
Ⅰ.实验步骤:
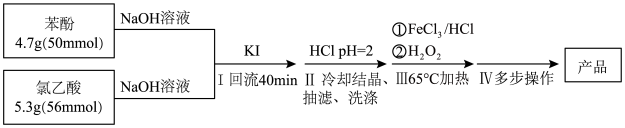
Ⅱ.反应原理:
主反应: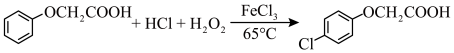
副反应:
Ⅲ.实验装置
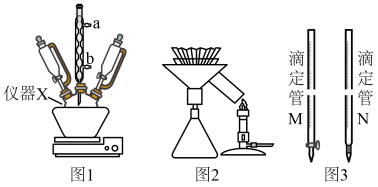
请回答:
(1)用10mL20%NaOH溶液溶解苯酚固体的原因(用化学方程式表示)_______ 。
(2)下列说法正确的是_______
A.图1中仪器X名称为三颈烧瓶,其加热方式只能用水浴或垫石棉网加热
B.图1冷凝管中的冷却水从导管a进入、导管b流出,利用逆流原理冷却效果好
C.图2热过滤时固液混合物液面要低于滤纸边缘,滤纸要低于漏斗边缘
D.图2热过滤优点防止温度降低引起产品损耗,从而提高产品收率
(3)步骤Ⅳ为粗产品的纯化,从下列选项中的操作合理排序:粗产品→用热的乙醇溶解→_______ →_______ →加蒸馏水→_______ →_______ →_______ →干燥→4.76g产品。本实验的产率为_______ (保留整数)
a.自然冷却 b.趁热过滤 c.洗涤 d.煮沸 e.抽滤
(4)为了测定对氯苯氧乙酸产品的纯度,可采用中和滴定法:准确称取0.2g产品,置于锥形瓶中,加30mL乙醇溶解,滴加酚酞指示剂,以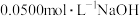 标准溶液滴定至微红色出现并持续30s不变色,即为终点,重复实验,数据如下:
标准溶液滴定至微红色出现并持续30s不变色,即为终点,重复实验,数据如下:
①装标准溶液时选择图3中规格为50mL的滴定管_______ (填“M”或“N”)。
②对氯苯氧乙酸产品的纯度为_______ (小数点后保留一位)。
Ⅰ.实验步骤:

Ⅱ.反应原理:
主反应:
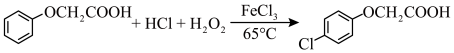
(相对分子质量:186.5)
副反应:

Ⅲ.实验装置

请回答:
(1)用10mL20%NaOH溶液溶解苯酚固体的原因(用化学方程式表示)
(2)下列说法正确的是
A.图1中仪器X名称为三颈烧瓶,其加热方式只能用水浴或垫石棉网加热
B.图1冷凝管中的冷却水从导管a进入、导管b流出,利用逆流原理冷却效果好
C.图2热过滤时固液混合物液面要低于滤纸边缘,滤纸要低于漏斗边缘
D.图2热过滤优点防止温度降低引起产品损耗,从而提高产品收率
(3)步骤Ⅳ为粗产品的纯化,从下列选项中的操作合理排序:粗产品→用热的乙醇溶解→
a.自然冷却 b.趁热过滤 c.洗涤 d.煮沸 e.抽滤
(4)为了测定对氯苯氧乙酸产品的纯度,可采用中和滴定法:准确称取0.2g产品,置于锥形瓶中,加30mL乙醇溶解,滴加酚酞指示剂,以
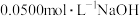 标准溶液滴定至微红色出现并持续30s不变色,即为终点,重复实验,数据如下:
标准溶液滴定至微红色出现并持续30s不变色,即为终点,重复实验,数据如下:序号 | 滴定前读数/mL | 滴定终点读数/mL |
1 | 0.20 | 20.22 |
2 | 20.22 | 40.52 |
3 | 1.54 | 21.52 |
②对氯苯氧乙酸产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某校同学设计实验用乙烯与Br2的CCl4溶液反应制备1,2—二溴乙烷。回答下列问题:
(1)甲组同学设计下列装置制备Br2的CC14溶液,实验装置如下:

①装置中烧瓶及广口瓶口上的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,其目的是____________________________________________ 。
②装置C的作用是_______________________________________________ 。
③烧瓶中主要生成NaHSO4、MnSO4和Br2,该反应的化学方程式为__________________ 。
(2)乙同学利用甲制得的Br2的CCl4溶液及下列装置制备1,2—二溴乙烷。

已知;I.烧瓶中主要发生的反应为C2H5OH C2H4↑+H2O
C2H4↑+H2O
主要副反应为C2H5OH+6H2SO4(浓) 6SO2↑+2CO2↑+9H2O
6SO2↑+2CO2↑+9H2O
Ⅱ.1,2—二溴乙烷的沸点为131.5℃,CC14的沸点为76.8℃,酸性高锰酸钾溶液会与乙烯反应。
①制得的乙烯经纯化后用于制取1,2—二溴乙烷的四氯化碳溶液并净化尾气(部分装置可重复使用),各玻璃接口连接的顺序为a→_____________ (填小写字母)。
②烧瓶中加入碎瓷片的作用是______________________________________ 。
③生成1,2—二溴乙烷的化学方程式为___________________________ ;判断Br2已完全反应的依据是_______________________________________ 。
(3)丙同学设计实验对乙同学得到的混合溶液进行分离提纯,下列玻璃仪器不需要的是____________ (填标号)。

(1)甲组同学设计下列装置制备Br2的CC14溶液,实验装置如下:

①装置中烧瓶及广口瓶口上的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,其目的是
②装置C的作用是
③烧瓶中主要生成NaHSO4、MnSO4和Br2,该反应的化学方程式为
(2)乙同学利用甲制得的Br2的CCl4溶液及下列装置制备1,2—二溴乙烷。

已知;I.烧瓶中主要发生的反应为C2H5OH
 C2H4↑+H2O
C2H4↑+H2O主要副反应为C2H5OH+6H2SO4(浓)
 6SO2↑+2CO2↑+9H2O
6SO2↑+2CO2↑+9H2OⅡ.1,2—二溴乙烷的沸点为131.5℃,CC14的沸点为76.8℃,酸性高锰酸钾溶液会与乙烯反应。
①制得的乙烯经纯化后用于制取1,2—二溴乙烷的四氯化碳溶液并净化尾气(部分装置可重复使用),各玻璃接口连接的顺序为a→
②烧瓶中加入碎瓷片的作用是
③生成1,2—二溴乙烷的化学方程式为
(3)丙同学设计实验对乙同学得到的混合溶液进行分离提纯,下列玻璃仪器不需要的是

您最近一年使用:0次



