16. 二氧化锰可作过氧化氢分解的催化剂,兴趣小组想探究过氧化氢分解有没有其他催化剂。影响过氧化氢分解的因素,除催化剂外,还有什么?
Ⅰ.【提出问题】氧化铁能否作过氧化氢分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| ①分别取5mL 5%过氧化氢溶液放入A、B两支试管中,向A中加入1g氧化铁粉末,并分别在A、B试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| ②待A中没有现象发生时,重新加入过氧化氢溶液,把带火星的木条伸入试管,如此反复3次。 | 试管中均产生气泡,带火星木条均复燃 |
| ③将步骤②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量为ag。 |
|
| ④分别取5mL 5%过氧化氢溶液放入C、D两支试管中,向C中加入1g氧化铁粉末,向D中加入1g二氧化锰粉末,观察现象。 |
|
【实验结论】
步骤②证明氧化铁的
______在反应前后没有发生变化。③中如果a=
_______,证明氧化铁的
______在反应前后没有发生变化。氧化铁可以作过氧化氢分解的催化剂。
【实验评价】设计实验步骤④的目的是
______。
Ⅱ.探究过氧化氢溶液浓度对过氧化氢分解速率的影响。
【交流讨论】可以通过测定相同条件下不同浓度过氧化氢溶液
______来探究。
A.产生相同体积氧气的时间
B.产生氧气的质量
C.产生氧气的总体积
D.单位时间内产生氧气的体积
【实验探究】按图1装置进行实验:水浴温度控制在21℃,二氧化锰均为0.5g,过氧化氢溶液均为5mL,三颈瓶容积为250mL,恒压漏斗(漏斗的支管与三颈瓶相连)的作用是使过氧化氢溶液自行下滴。数字传感器数据绘制图像如图2、3。
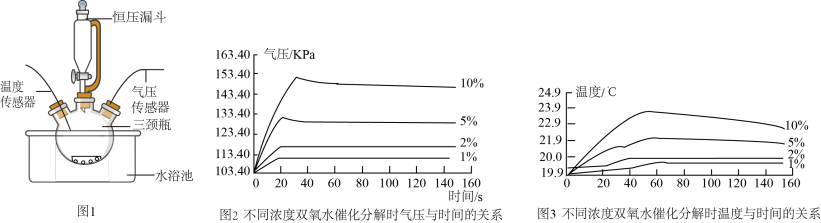
【实验结论】图2说明过氧化氢溶液浓度与反应速率关系是
______。以10% H
2O
2溶液为例,三颈瓶内气压由高缓慢降低的原因是
______。
图3说明从温度看,过氧化氢溶液浓度越高,反应越
______(填“剧烈”或“平稳”)。