28. 为了探究影响氯酸钾分解速率的因素,小明把实验温度恒定在330℃或380℃,(其他实验条件见表),并设计了以下实验。
| 实验编号 | 氯酸钾的质量 | 催化剂及其质量/g | 温度/℃ | 反应的时间/s | 待测值 |
| ① | 2.0 | 无 | 330 | 100 |
|
| ② | 2.0 | 氧化铁0.5 | 330 | 100 |
|
| ③ | 2.0 | 二氧化锰0.5 | 330 | 100 |
|
| ④ | 2.0 | 二氧化锰 |
| 100 |
|
(1)通过比较待测值大小来判断反应的速率,则待测值指的是
________。
(2)进行实验②和③,并进行对比,其实验目的是
________。
(3)要说明氧化铁对氯酸钾分解速率的影响,则要选用实验
________和实验
________进行对比。
(4)用实验③和④探究温度对氯酸钾分解速率的影响,则二氧化锰的质量是
________g,控制的温度是
________℃。若实验③的待测值小于④,则得到的实验结论:
________;实验③反应的文字或符号表达式:
________。
II.探究氯酸钾和氧化铁(Fe
2O
3)的质量比会不会影响反应的快慢?
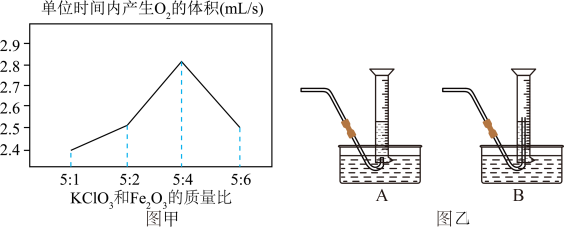
(5)调节KClO
3和Fe
2O
3的质量比制备氧气,整理数据绘制出图图甲,从图甲中得出KC1O
3和Fe
2O
3反应的最佳质量比是
________。
(6)测量气体体积时,可以将反应的发生装置和倒置量筒连接(如图图乙所示),为了提高测量结果的准确率,则收集气体应选图中的
________(填A或B)。
(7)测量气体体积开始前,量筒内上方未排出的空气,使测量结果
________(填偏大,偏小或不变)。读数操作正确的情况下,测得的气体体积比理论上生成的氧气体积大,可能原因是
________。
(8)如图甲所示,在KClO
3和Fe
2O
3质量比为5:4之前,氧化铁质量越多,反应越快的原因是:
________。