26. 中和反应是中学化学中重要的学习内容,其在日常生活和工农业生产中有广泛的应用。
实验活动一:将氢氧化钾溶液与稀硫酸混合,无明显现象,小组三位同学进行以下实验。
(1)测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将
_______ (填字母序号)。
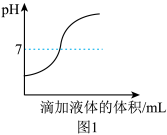
a.氢氧化钾溶液滴入稀硫酸中
b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化
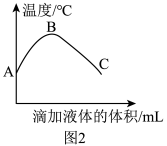
乙同学在实验过程中测得混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是放热反应。图2中B点的含义是
_______。
(3)借助于酸碱指示剂
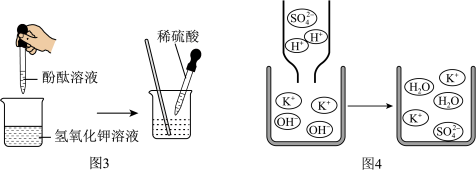
丙同学通过图3所示实验,他观察到溶液
_______,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为
_______。如图4所示信息,可知氢氧化钾和稀硫酸反应的实质是
_______。
(交流反思)对于无明显现象的化学反应,可通过检验有新物质生成或检验的方法来证明物质间发生反应。
实验活动二:实验后发现废液桶内剩余很多含硫酸的废水,需经处理至中性。小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(4)定性检测废水
检测废水呈酸性的方法是
_______。
(5)定量测定废水
取酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图5所示。(废水中其他成分不与氢氧化钾反应且不含硫酸钾)
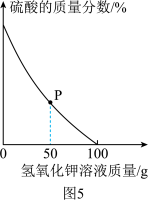
①P点对应溶液中一定存在的阳离子有
_______(填离子符号)。
②酸性废水中硫酸的质量分数为
_______(用百分数表示,保留到0.1%)。
③计算当废水处理至中性时,溶液中硫酸钾的质量分数
_______。(写出计算过程,结果用百分数表示,保留到0.1%)。