向AgNO3和Fe(NO3)2的混合溶液中加入一定量Zn粉,充分反应后过滤,得到滤渣和滤液,滤渣中一定含有______ (化学式),滤液中一定含有______ (化学式),溶液中可能发生反应的化学方程式为______ 。
2021·黑龙江·中考真题 查看更多[7]
2023年内蒙古赤峰市红山区中考一模化学试题2022年山东省临沂市临沭县中考二模化学试题河南省驻马店市汝南县2021-2022学年九年级上学期期末化学试题(已下线)专题06 金属及金属材料的利用-2022年初三毕业班化学常考点归纳与变式演练(通用版)(已下线)专题11 金属和金属矿物-2021年中考化学真题分项汇编(全国通用)(第03期)黑龙江省龙东地区2021年中考化学试题黑龙江省龙东地区(农垦 森工)2021年中考化学试题
更新时间:2021-06-27 21:26:49
|
相似题推荐
【推荐1】能源与材料是人类生存和发展的基础。
(1)我国氢能汽车采用了第四代以氢气为燃料的电池技术。氢气作为理想能源前景广阔,氢气燃烧的化学方程式为_____ ,氢能源的优点是_____ (答出一点即可)。
(2)中国空间站舱外宇航服的最外层使用了玻璃纤维和一种叫“特氟隆”的合成纤维,足以抵御像枪弹一般的微陨石的袭击,它具有的特性是_____ (合理即可)
(3)某同学在探究金属与盐溶液反应的实验时,向铝粉和锌粉的混合物中加入一定质量的Mg(NO3)2和AgNO₃混合溶液,充分反应后过滤,可得到滤渣和滤液。若滤渣中含有三种金属,则此时滤液中的溶质是_____ (填化学式)。
(1)我国氢能汽车采用了第四代以氢气为燃料的电池技术。氢气作为理想能源前景广阔,氢气燃烧的化学方程式为
(2)中国空间站舱外宇航服的最外层使用了玻璃纤维和一种叫“特氟隆”的合成纤维,足以抵御像枪弹一般的微陨石的袭击,它具有的特性是
(3)某同学在探究金属与盐溶液反应的实验时,向铝粉和锌粉的混合物中加入一定质量的Mg(NO3)2和AgNO₃混合溶液,充分反应后过滤,可得到滤渣和滤液。若滤渣中含有三种金属,则此时滤液中的溶质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】同学们到实验室进行“探究金属的性质”实验。将镁粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有______ (填写化学式,下同),可能含有______ ;
②滤渣中一定含有______ ;
(2)若反应后所得滤液呈无色,则滤渣中一定含有______ (填写化学式)。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有
②滤渣中一定含有
(2)若反应后所得滤液呈无色,则滤渣中一定含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
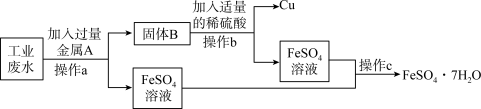
【推荐3】某工厂排放的工业废水中含大量的硫酸亚铁和硫酸铜,可能还含有较多的硫酸。为了减少污染并变废为宝,工厂技术人员首先对废水进行检验确定其成分,再从该废水中回收铜及硫酸亚铁。请回答下列问题:______ ,说明废水中不含硫酸。
(2)从(1)实验中取出铁片,发现铁片表面有紫红色物质析出,溶液由蓝色变成浅绿色,该反应的化学方程式为______ 。
(3)固体B的成分是______ 。
(4)a和b涉及的操作中,玻璃棒的作用是______ 。
(5)进行操作b之前加入的稀硫酸不能用稀盐酸代替的原因是______ 。
(2)从(1)实验中取出铁片,发现铁片表面有紫红色物质析出,溶液由蓝色变成浅绿色,该反应的化学方程式为
(3)固体B的成分是
(4)a和b涉及的操作中,玻璃棒的作用是
(5)进行操作b之前加入的稀硫酸不能用稀盐酸代替的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属铁、铝、铜在生产和生活中有广泛的应用:
(1)地壳中含量最多的金属元素是______ (填名称);
(2)金属铜做导线是利用其延展性和______ 性;
(3)铁是应用最广泛的金属。工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为______ ;
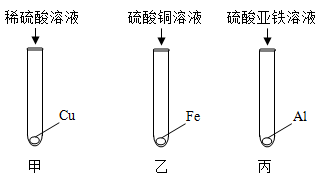
(4)实验室中用如下实验来研究铁、铝、铜三种金属活 动顺序及其在活动顺序表中相对氢的位置。
①乙实验的现象为______ ;
②若将上述实验之一替换掉一种药品,即可达成实验目的。说明具体的改进方法:____ ;
③按如图实验结束后,将乙、丙实验后的剩余物倾倒至一个烧杯中,充分反应。然后将甲实验的剩余物倒入此烧杯,无气泡产生。以下说法正确的是______ (填序号)。
A.最后烧杯中的溶液一定有颜色
B.乙实验中铁一定反应完全
C.乙、丙混合过程中,一定发生化学变化
D.最后烧杯中的溶液,一定含有 Al2(SO4)3、FeSO4、H2SO4,可能含有 CuSO4
(1)地壳中含量最多的金属元素是
(2)金属铜做导线是利用其延展性和
(3)铁是应用最广泛的金属。工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为
(4)实验室中用如下实验来研究铁、铝、铜三种金属活 动顺序及其在活动顺序表中相对氢的位置。
①乙实验的现象为
②若将上述实验之一替换掉一种药品,即可达成实验目的。说明具体的改进方法:
③按如图实验结束后,将乙、丙实验后的剩余物倾倒至一个烧杯中,充分反应。然后将甲实验的剩余物倒入此烧杯,无气泡产生。以下说法正确的是

A.最后烧杯中的溶液一定有颜色
B.乙实验中铁一定反应完全
C.乙、丙混合过程中,一定发生化学变化
D.最后烧杯中的溶液,一定含有 Al2(SO4)3、FeSO4、H2SO4,可能含有 CuSO4
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属活动性顺序
(1)阅读教材,完成教材中实验,填写下表。
(2)金属活动性顺序从强到弱是_____ 、Ca、_____ 、_____ 、Al、_____ 、_____ 、Sn、Pb、(H)、_____ 、Hg、_____ 、Pt、_____ 。
(3)活动性_____ 的金属能把活动性_____ 的金属从它们的化合物的溶液中置换出来,反之不能。因此,可以用金属能否与另一种金属化合物的溶液反应来判断金属活动性强弱。
(1)阅读教材,完成教材中实验,填写下表。
| 实验 | 现象 | 反应的化学方程式 |
| 铝丝浸入硫酸铜溶液中 | 铝丝表面 | |
| 铜丝浸入硝酸银溶液中 | 铜丝的表面 | |
| 铜丝浸入硫酸铝溶液中 | 无明显现象 | 无 |
(3)活动性
您最近一年使用:0次



