阅读下列材料,回答问题。
2022年11月30日,神舟十五号3名航天员顺利进驻“天和”核心舱与神舟十四号航天员乘组首次实现“太空会师”,核心舱使用了第三代半导体砷化镓(GaAs)太阳能电池翼,航天员在“天和”核心舱中生活所需要的氧气来自水的电解。航天员在核心舱的饮用水来自“水处理”系统,“水处理”系统将核心舱内产生的污水收集后,通过RO反渗透膜(只允许水分子和少部分离子通过)进行渗透净化处理,实现污水变净水,达到饮用水的标准。
2022年6月17日,我国第三艘航空母舰“福建舰”下水,“福建舰”是我国完全自主设计建造的首艘弹射型航空母舰,使用了许多包括特种合金钢、铁合金等在内的高性能材料,请回答下列问题。
(1)RO反渗透膜利用的净化方法相当于化学实验中的______ 操作实现污水变净水。
(2)写出核心舱内电解水的化学方程式:_______ 。
(3)下列说法正确的是_____ 。
(4)舰体易遭受高盐、高湿度的海洋气候侵蚀,为防止航母中钢铁制品锈蚀,你认为下列措施可行的是______。
(5)为了探究航母材料中锌、铁、铜三种金属的活动性强弱,某同学用形状大小相同并用砂纸打磨过的铁片设计了下列实验。
2022年11月30日,神舟十五号3名航天员顺利进驻“天和”核心舱与神舟十四号航天员乘组首次实现“太空会师”,核心舱使用了第三代半导体砷化镓(GaAs)太阳能电池翼,航天员在“天和”核心舱中生活所需要的氧气来自水的电解。航天员在核心舱的饮用水来自“水处理”系统,“水处理”系统将核心舱内产生的污水收集后,通过RO反渗透膜(只允许水分子和少部分离子通过)进行渗透净化处理,实现污水变净水,达到饮用水的标准。
2022年6月17日,我国第三艘航空母舰“福建舰”下水,“福建舰”是我国完全自主设计建造的首艘弹射型航空母舰,使用了许多包括特种合金钢、铁合金等在内的高性能材料,请回答下列问题。
(1)RO反渗透膜利用的净化方法相当于化学实验中的
(2)写出核心舱内电解水的化学方程式:
(3)下列说法正确的是_____ 。
| A.电解水产生氢气和氧气的质量比为2:1 |
| B.通过RO反渗透膜进行渗透净化处理后的水为纯净物 |
| C.第三代半导体砷化镓(GaAs)太阳能电池翼供电将太阳能转化为电能 |
| A.用抗锈蚀性能优异的合金制造航母零部件 | B.刷防锈漆 |
| C.船体表面镀一层黄金 | D.给某些部位涂油 |
| 实验步骤 | 实验现象 | 实验结论 |
| 将其中一块铁片放入硫酸锌溶液中 | 金属活动性:Zn>Fe | |
| 将另一块铁片放入 | 金属活动性: |
更新时间:2023-06-02 15:10:16
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某品牌电器的废旧电路板中含有Fe、Cu、Ag、Ni(镍,银白色金属)等金属,如图是某车间回收部分金属的工艺流程,已知: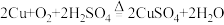 。
。
回答下列问题:

(1)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni_________ (填“>”或“<”)Fe。
(2)滤液③中的溶质为_________ 。(填化学式)
(3)滤渣③回收的主要金属是_________ 。固体A除铜外,还含有一定量的铁,为进一步提纯铜,可向固体A中加入适量的稀硫酸,发生反应的化学方程式为_________ 。
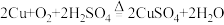 。
。回答下列问题:

(1)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni
(2)滤液③中的溶质为
(3)滤渣③回收的主要金属是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】比较、分析、归纳是学习化学的有效方法。
现有反应:①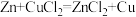 ;
;
②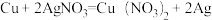 ;
;
③ ;
;
④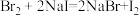 。
。
(1)通过比较、分析,可以发现上述四个反应有相似之处:均属于四种基本反应类型中的____________ 反应。再分析这四个反应前后各元素的化合价,我们还会发现一个相似之处:_____________________ 。
(2)分析反应①和②,可以得到:Zn、Cu、Ag三种金属的活动性由强到弱的顺序是_____________ 。根据反应③和④,用相似的思维方法,我们还可以得到:Cl2、Br2、I2三种非金属的活泼性由强到弱的顺序为__________ 。试判断将Cl2通入KI溶液中能否发生反应?若能发生反应请写出化学方程式,若不能发生反应请简述理由___________ 。
现有反应:①
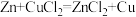 ;
; ②
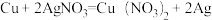 ;
;③
 ;
; ④
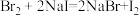 。
。(1)通过比较、分析,可以发现上述四个反应有相似之处:均属于四种基本反应类型中的
(2)分析反应①和②,可以得到:Zn、Cu、Ag三种金属的活动性由强到弱的顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】金属材料与人类的生产和生活密切相关。请回答:
(1)下列用品中,主要利用金属导电性的是____ (填字母)。
A 铂金饰品 B 铁锅 C 铝导线
(2)生活中的下列物品所使用的主要材料属于合金的是_______ 。
①不锈钢菜刀 ②橡胶手套 ③纯棉围裙 ④塑料袋 ⑤防盗门 ⑥自行车支架
(3)请用化学方程式表示铝制品耐腐蚀的原因_______ 。
(4)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是____ (填序号)
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(5)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是____ 。
(1)下列用品中,主要利用金属导电性的是
A 铂金饰品 B 铁锅 C 铝导线
(2)生活中的下列物品所使用的主要材料属于合金的是
①不锈钢菜刀 ②橡胶手套 ③纯棉围裙 ④塑料袋 ⑤防盗门 ⑥自行车支架
(3)请用化学方程式表示铝制品耐腐蚀的原因
(4)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(5)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属是重要的资源,与我们的生活息息相关。
(1)医用口罩的鼻梁夹大多选用铝或铁,铝、铁能压成条,是利用了金属的_______ 性。
(2)①在铁制品表面喷涂防锈涂料,可防止铁制品生锈,其防锈原理是_______ 。除防止金属腐蚀外,请写出一条保护金属资源的有效途径:_______ 。
②若使用的铁矿石是磁铁矿,请写出炼铁炉中利用生成的一氧化碳将铁从磁铁矿中还原出来的化学方程式_______ 。
③不断翻炒液态生铁,是为了_______ (填“降低”或“升高”)碳元素的含量以制钢。
(3)图甲、图乙为利用数字化仪器测得的室温下,足量的镁片与20mL10%的稀盐酸充分反应产生氢气的量与时间的关系曲线。(产生氢气的量由气体压强表示,在等温条件下,产生氢气体积与装置内压强成正比)。_______ 。
②实验测得的实际值比通过计算得到的理论值偏大,可能的原因为_______ (答一条)。
(1)医用口罩的鼻梁夹大多选用铝或铁,铝、铁能压成条,是利用了金属的
(2)①在铁制品表面喷涂防锈涂料,可防止铁制品生锈,其防锈原理是
②若使用的铁矿石是磁铁矿,请写出炼铁炉中利用生成的一氧化碳将铁从磁铁矿中还原出来的化学方程式
③不断翻炒液态生铁,是为了
(3)图甲、图乙为利用数字化仪器测得的室温下,足量的镁片与20mL10%的稀盐酸充分反应产生氢气的量与时间的关系曲线。(产生氢气的量由气体压强表示,在等温条件下,产生氢气体积与装置内压强成正比)。

②实验测得的实际值比通过计算得到的理论值偏大,可能的原因为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】运用所学知识回答问题
(1)铁架车的表面刷油漆能防止锈蚀,其原因是_____ ;
(2)自来水的净化过程中常用_____ 吸附水中的色素,常用ClO2进行消毒,产生ClO2的化学反应方程式是2NaClO3+4HCl═2ClO2+Cl2+2X+2H2O,则X的化学式是_____ 。
(1)铁架车的表面刷油漆能防止锈蚀,其原因是
(2)自来水的净化过程中常用
您最近一年使用:0次
【推荐1】分类、类比、推理是初中学习化学常用的方法。
(1)水是地球上最常见的物质之一,如图所示实验中都用到水,根据水的用途,将___________ (填字母)归为一类,理由是___________ 。

(2)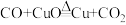

在这两个反应中,一氧化碳和木炭都体现了还原性,则氧化铜体现了___________ 性,其作用是___________ 。
(1)水是地球上最常见的物质之一,如图所示实验中都用到水,根据水的用途,将

(2)
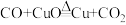

在这两个反应中,一氧化碳和木炭都体现了还原性,则氧化铜体现了
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】图中A~H是初中化学常见的物质。在通常情况下A、B是液体,F、E和G是固体,其余均是气体。F因其燃烧发出耀眼的白光可用来制作信号弹,G物质所含元素是生物细胞中含量第二位的元素。图中“—”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去。

(1)B的化学式______ ;
(2)写出F→E反应的化学方程式______ ;
(3)G→H反应的基本反应类型为______ 。

(1)B的化学式
(2)写出F→E反应的化学方程式
(3)G→H反应的基本反应类型为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A-I都是初中化学中常见的物质。其中 A、D是组成元素相同的无色液体,B 是黑色固体,E 是白色固体,它们之间的转换关系如图所示:
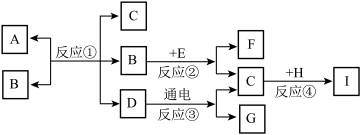
(1)写出下列物质的化学式:A_____________ C ______________ 。
(2)请写出反应③的符号表达式_____________________ 。
(3)若 H 是黑色固体,则物质I的名称是__________ ,若I是黑色固体,则反应④的现象是__________ 。

(1)写出下列物质的化学式:A
(2)请写出反应③的符号表达式
(3)若 H 是黑色固体,则物质I的名称是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】阅读材料,回答相关问题
Ⅰ、锂(Li)的用途:利用锂与水反应生成氢氧化锂(LiOH)和氢气,可制造海水电池。
(1)写出锂与水反应的化学方程式:______ 。
Ⅱ、锂矿石成分分析
(2)锂辉石的主要成分为LiAlSi2O6,其硅、氧原子的个数比为______ 。
Ⅲ、碳酸锂(Li2CO3)的制取
步骤1将锂辉石和石灰石混合磨细后,高温煅烧
步骤2向煅烧后的混合物中加水,浸取,分离得到氢氧化锂溶液和难溶性固体
步骤3蒸发浓缩氢氧化锂溶液,加入纯碱析出碳酸锂,分离、洗涤、干燥得碳酸锂成品。
碳酸锂的溶解度与温度的关系见下表
(3)写出氧化锂与水反应生成氢氧化锂的化学方程式______ ;步骤3中分离Li2CO3的实验操作是______ (填操作名称)。
(4)为减少碳酸锂因溶解而损失,选择______ (填“冰水”或“热水”)洗涤。
Ⅰ、锂(Li)的用途:利用锂与水反应生成氢氧化锂(LiOH)和氢气,可制造海水电池。
(1)写出锂与水反应的化学方程式:
Ⅱ、锂矿石成分分析
(2)锂辉石的主要成分为LiAlSi2O6,其硅、氧原子的个数比为
Ⅲ、碳酸锂(Li2CO3)的制取
步骤1将锂辉石和石灰石混合磨细后,高温煅烧
步骤2向煅烧后的混合物中加水,浸取,分离得到氢氧化锂溶液和难溶性固体
步骤3蒸发浓缩氢氧化锂溶液,加入纯碱析出碳酸锂,分离、洗涤、干燥得碳酸锂成品。
碳酸锂的溶解度与温度的关系见下表
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(4)为减少碳酸锂因溶解而损失,选择
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】小凡欲从含泥沙的粗盐(氯化钠和泥沙的混合物)中提纯氯化钠,试回答:
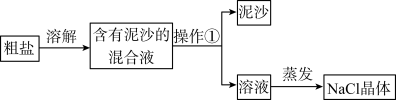
(1)溶解时,玻璃棒不断搅拌的作用是__ 。
(2)操作①常用于不溶于液体的固体物质与液体的分离。以下实验目的中可利用此实验方法达成的有__ (填序号)。
A双氧水制氧气实验后回收二氧化锰 B从蔗糖水中提取蔗糖
(3)操作①的名称是__ ,操作①需要用到的玻璃仪器有玻璃棒、烧杯、__ ,该步骤中玻璃棒的作用是__ 。
(4)操作①中需要将圆形滤纸折叠处理,如图所示图示中不该出现的情形是__ (填序号)。
A B
B  C
C  D
D
(5)若过滤后滤液仍浑浊,可能原因是__ (写一条),应如何操作__ 。

(1)溶解时,玻璃棒不断搅拌的作用是
(2)操作①常用于不溶于液体的固体物质与液体的分离。以下实验目的中可利用此实验方法达成的有
A双氧水制氧气实验后回收二氧化锰 B从蔗糖水中提取蔗糖
(3)操作①的名称是
(4)操作①中需要将圆形滤纸折叠处理,如图所示图示中不该出现的情形是
A
 B
B  C
C  D
D
(5)若过滤后滤液仍浑浊,可能原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】氧化铁(Fe2O3)在工业上又叫氧化铁红,是不溶于水的红棕色粉末,常用于油漆、油墨、橡胶等工业中,也是常用的催化剂,在空气中灼烧亚铁化合物或氢氧化铁等可得高纯氧化铁。以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁的生产工艺流程。
(1)在通入CO之前,需要将硫铁矿烧渣进行粉碎,目的是______ 。
(2)高温条件下硫铁矿烧渣中的Fe2O3与CO发生反应的化学方程式为______ 。
(3)操作1能得到硫酸亚铁晶体,说明硫酸亚铁的溶解度随温度的升高而______ 。
(4)实验室中完成操作2时,玻璃棒的作用是______ 。所得的滤液是硫酸亚铁的______ (填“饱和”或“不饱和”)溶液。

(1)在通入CO之前,需要将硫铁矿烧渣进行粉碎,目的是
(2)高温条件下硫铁矿烧渣中的Fe2O3与CO发生反应的化学方程式为
(3)操作1能得到硫酸亚铁晶体,说明硫酸亚铁的溶解度随温度的升高而
(4)实验室中完成操作2时,玻璃棒的作用是
您最近一年使用:0次



