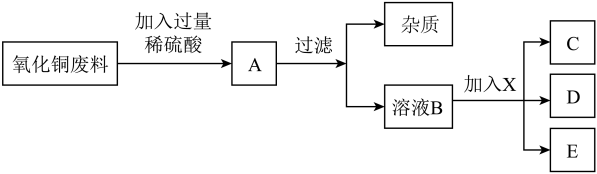
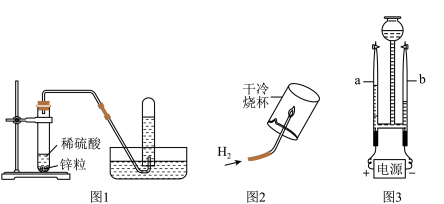
如图是初中化学中的一些常见的实验。请回答:
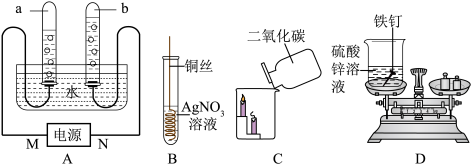
(1)A是电解水成功的实验:分析N端是电源的______ (选填“正极“或“负极”)。
(2)B是验证铜、银活动性的实验:该反应方程式是______ 。
(3)C是验证CO2的性质的实验:本实验得出CO2的化学性质是______ 。
(4)D是小欣设计的短时间内验证质量守恒定律的实验:请你分析,她的设计______ (选填“能”或“不能”)达到实验目的,原因是______ 。

(1)A是电解水成功的实验:分析N端是电源的
(2)B是验证铜、银活动性的实验:该反应方程式是
(3)C是验证CO2的性质的实验:本实验得出CO2的化学性质是
(4)D是小欣设计的短时间内验证质量守恒定律的实验:请你分析,她的设计
更新时间:2024/02/04 07:55:37
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
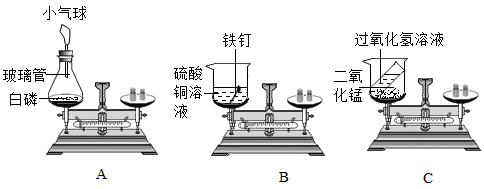
【推荐1】某校化学兴趣小组在老师的引导下进行“化学反应中,反应物与生成物的质量关系”的实验探究。他们使用的实验装置和选用药品如图所示,现分别以A、B、C表示如下:
(1)A实验:锥形瓶底放层细沙的原因是________________ 。引燃白磷待反应结束,锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。结论是:质量守恒。反应的化学方程式为 _______________ 。实验过程中小气球的变化是 ________ 。
(2)乙组同学认为B实验验证了质量守恒定律。此处化学反应的现象是_______________ 。请结合该反应表述质量守恒定律 _______________ 。
(3)丙组同学得到的错误结论是“C实验说明质量不守恒”。你认为C实验天平不平衡的原因是_______ 。该反应的化学方程式为 _______________ 。
(1)A实验:锥形瓶底放层细沙的原因是
(2)乙组同学认为B实验验证了质量守恒定律。此处化学反应的现象是
(3)丙组同学得到的错误结论是“C实验说明质量不守恒”。你认为C实验天平不平衡的原因是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】为验证质量守恒定律,小华设计如图所示装置进行实验。
(2)怎样改进实验才能达到实验目的。
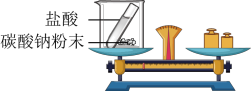
(2)怎样改进实验才能达到实验目的。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】小英同学从资料中得知:质量守恒定律的发现经历了漫长、曲折的过程。
【实验回顾】
1756年,俄国化学家罗蒙诺索素夫将金属锡放在密闭容器里煅烧,冷却后在密闭容器里称量,发现总质量和煅烧前没有变化。
1774年,拉瓦锡将45.0份质量的氧化汞加热分解,恰好得到了41.5份质量的汞和3.5份质量的氧气,得到了与罗蒙诺索夫相同的结论,拉瓦锡还通过这个实验研究了______ ,成就了化学史上的另一经典实验。
【实验重现】
小英同学在老师的指导下,将铁粉、活性炭粉、食盐按一定比例加水混合后,涂在用铁片折成的连续的Z形架表面,然后放入盛满氧气的集气瓶中、通过如图所示装置对“化学反应中,反应物与生成物的质量关系”进行实验探究,实验过程中做到操作规范,准确称量和细致观察。______ ,______ 。
(2)此实验用氧气替代空气的主要目的是______ 。
(3)实验室里现有过氧化氢溶液,二氧化锰粉末,以及下列仪器:______ 。
②利用上述药品,仪器:制取少量纯净氧气,其简易制取装置应选择的仪器有______ (填序号),反应的化学方程式为:______ 。
【总结与反思】
1663年,英国化学家波义耳将金属汞放在密闭容器里煅烧,冷却后称量时打开了盖,得出的结论是物质的总质量增加了,导致波义耳与质量守恒定律失之交臂,你认为质量增大的原因是:______ 。
【实验回顾】
1756年,俄国化学家罗蒙诺索素夫将金属锡放在密闭容器里煅烧,冷却后在密闭容器里称量,发现总质量和煅烧前没有变化。
1774年,拉瓦锡将45.0份质量的氧化汞加热分解,恰好得到了41.5份质量的汞和3.5份质量的氧气,得到了与罗蒙诺索夫相同的结论,拉瓦锡还通过这个实验研究了
【实验重现】
小英同学在老师的指导下,将铁粉、活性炭粉、食盐按一定比例加水混合后,涂在用铁片折成的连续的Z形架表面,然后放入盛满氧气的集气瓶中、通过如图所示装置对“化学反应中,反应物与生成物的质量关系”进行实验探究,实验过程中做到操作规范,准确称量和细致观察。
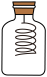
(2)此实验用氧气替代空气的主要目的是
(3)实验室里现有过氧化氢溶液,二氧化锰粉末,以及下列仪器:
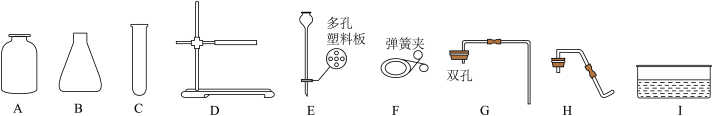
②利用上述药品,仪器:制取少量纯净氧气,其简易制取装置应选择的仪器有
【总结与反思】
1663年,英国化学家波义耳将金属汞放在密闭容器里煅烧,冷却后称量时打开了盖,得出的结论是物质的总质量增加了,导致波义耳与质量守恒定律失之交臂,你认为质量增大的原因是:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验装置,回答问题。
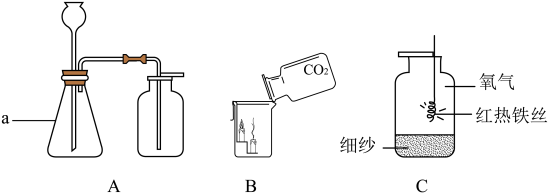
(1)装置A中,仪器a的名称是_____ 。
(2)实验室常用A制取二氧化碳,反应的化学方程式为_____ ;
(3)如图B所示,将二氧化碳慢慢倒入烧杯中,观察到蜡烛火焰由低到高依次熄灭,说明二氧化碳具有的性质是_____ 、_____ ;
(4)实验室用装置A制取氧气并用装置C做铁丝在氧气中燃烧的实验时,集气瓶中细沙的作用是_____ 。

(1)装置A中,仪器a的名称是
(2)实验室常用A制取二氧化碳,反应的化学方程式为
(3)如图B所示,将二氧化碳慢慢倒入烧杯中,观察到蜡烛火焰由低到高依次熄灭,说明二氧化碳具有的性质是
(4)实验室用装置A制取氧气并用装置C做铁丝在氧气中燃烧的实验时,集气瓶中细沙的作用是
您最近一年使用:0次
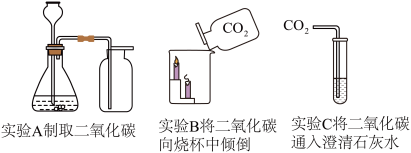
【推荐2】为了探究二氧化碳的性质,小华同学依次完成了如图所示的实验。______ (请用下列选项填空)。
a.放在瓶口 b.伸入瓶内 c.伸入瓶中部 d.伸入瓶底部
(2)实验B中的实验现象为蜡烛自下而上依次熄灭,该实验结论为:
①二氧化碳密度比空气______ 。
②二氧化碳______ 燃烧,也不支持燃烧,利用这一性质,二氧化碳可用于______ 。
(3)实验C中可观察到______ 现象,请写出相关化学方程式______ 。
(4)如果将二氧化碳通入紫色石蕊溶液中,溶液会变成______ 色。
a.放在瓶口 b.伸入瓶内 c.伸入瓶中部 d.伸入瓶底部
(2)实验B中的实验现象为蜡烛自下而上依次熄灭,该实验结论为:
①二氧化碳密度比空气
②二氧化碳
(3)实验C中可观察到
(4)如果将二氧化碳通入紫色石蕊溶液中,溶液会变成
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属及其化合物在生产生活中有广泛的应用。
(1)国产大飞机C919机壳采用了铝锂合金材料。铝锂合金的硬度比铝的硬度______ 。
(2)建造航母用到钛合金,钛合金属于______ (填“纯净物”或“混合物”)。工业制钛其中一步反应为:TiF4 + 2H2SO4=4HF + 2X + TiO2,X的化学式______ 。
(3)铁与硫酸铜溶液反应的微观示意图如下:
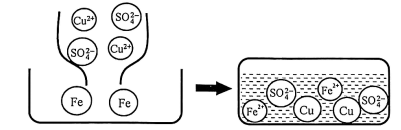
①反应过程中没有参与反应的微粒是______ 。
②根据图示,下列有关说法正确的是______
A.反应中每个铁原子得到2个电子,生成亚铁离子
B.从微观角度分析,该反应生成的新微粒是铜原子和亚铁离子
C.从反应的类型来看,该反应属于复分解反应
D.从化合价角度看,该反应有3种元素化合价发生变化
(1)国产大飞机C919机壳采用了铝锂合金材料。铝锂合金的硬度比铝的硬度
(2)建造航母用到钛合金,钛合金属于
(3)铁与硫酸铜溶液反应的微观示意图如下:

①反应过程中没有参与反应的微粒是
②根据图示,下列有关说法正确的是
A.反应中每个铁原子得到2个电子,生成亚铁离子
B.从微观角度分析,该反应生成的新微粒是铜原子和亚铁离子
C.从反应的类型来看,该反应属于复分解反应
D.从化合价角度看,该反应有3种元素化合价发生变化
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属的利用史成就卓越,是劳动人民生产、生活智慧的结晶。
(1)《天工开物》中记载:“凡铁一炉载土二千余斤,或用硬木柴,或用煤炭,或用木炭”(“土”为铁矿石),描述了古人冶炼金属的技法。请写出C还原赤铁矿石的化学方程式______ 。
(2)《黄白第十六》中记载:“曾青涂铁,铁赤如铜”,其中“曾青”是可溶性铜盐。该事实说明铁的活泼性______ (选填“>”、“<”或“=”)铜。
(3)为防止铁制品锈蚀,古人会对铁制品进行“烤蓝”处理,使其表面生成一层致密的氧化膜,其防锈原理是______ 。
(4)现代铸铜工艺中常常会通入氩气等保护气。否则铜器会变黑,变黑的原因是______ (用化学方程式表示)。
(1)《天工开物》中记载:“凡铁一炉载土二千余斤,或用硬木柴,或用煤炭,或用木炭”(“土”为铁矿石),描述了古人冶炼金属的技法。请写出C还原赤铁矿石的化学方程式
(2)《黄白第十六》中记载:“曾青涂铁,铁赤如铜”,其中“曾青”是可溶性铜盐。该事实说明铁的活泼性
(3)为防止铁制品锈蚀,古人会对铁制品进行“烤蓝”处理,使其表面生成一层致密的氧化膜,其防锈原理是
(4)现代铸铜工艺中常常会通入氩气等保护气。否则铜器会变黑,变黑的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是一切生命赖以生存的根本。没有水,就没有生命。
(1)保持水的化学性质的最小粒子是_______ 。
(2)天然水通过①过滤②沉淀③蒸馏等操作可以得到不同程度的净化。综合运用上述操作净水效果会更好,运用的先后顺序是_______ (填序号)。
(3)水的硬度过大,饮用时不但口感不好,而且对健康有害,生活中常用_______ 方法降低水的硬度,降低水的硬度实质上就是减少硬水中_______ 的含量。
(4)下列实验能证明水是由氢元素和氧元素组成的是(填字母序号)
(5)爱护水资源是每个公民应尽的义务,请你写出一条防止水污染的做法:_______ 。
(1)保持水的化学性质的最小粒子是
(2)天然水通过①过滤②沉淀③蒸馏等操作可以得到不同程度的净化。综合运用上述操作净水效果会更好,运用的先后顺序是
(3)水的硬度过大,饮用时不但口感不好,而且对健康有害,生活中常用
(4)下列实验能证明水是由氢元素和氧元素组成的是(填字母序号)
| A.氢气在氧气中燃烧 | B.水的蒸发 |
| C.水的电解 | D.水的净化 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】水在生产、生活中有着及其重要的作用。
①15%的氯化钠溶液具有消毒作用,其中溶剂是______ ,配置100g该溶液,需要氯化钠______ g。配置过程中会导致溶液质量分数偏大的可能原因是______ (写出一条即可)。
②对氯化钠溶液进行焰色反应,火焰呈______ 色;滴加硝酸银溶液,观察到生成白色沉淀,请写出该反应的化学方程式______ 。
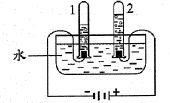
③下图电解水实验揭示了水的组成。实验中得到氢气的试管是______ (选填“1”“2”)。反应的化学方程式为______ 。2mol水中约含_____ 个水分子。
④ 、
、 、
、 在不同溶剂中的溶解度如下表所示。
在不同溶剂中的溶解度如下表所示。
表1 、
、 、
、 分别在水中的溶解度(g/100g水)
分别在水中的溶解度(g/100g水)
表2 常温下, 、
、 、
、 分别在100g乙醇中最多溶解的质量
分别在100g乙醇中最多溶解的质量
根据表1和表2提供的数据回答下列问题
Ⅰ. 在水中的溶解度随温度升高而
在水中的溶解度随温度升高而______ (选填“增大”“减小”)。
Ⅱ.20℃时,饱和食盐水中溶质质量分数为______ 。
Ⅲ.常温下,将 通入饱和
通入饱和 的乙醇溶液中,反应的方程式为
的乙醇溶液中,反应的方程式为______ ,可观察到的现象______ 。
①15%的氯化钠溶液具有消毒作用,其中溶剂是
②对氯化钠溶液进行焰色反应,火焰呈
③下图电解水实验揭示了水的组成。实验中得到氢气的试管是

④
 、
、 、
、 在不同溶剂中的溶解度如下表所示。
在不同溶剂中的溶解度如下表所示。表1
 、
、 、
、 分别在水中的溶解度(g/100g水)
分别在水中的溶解度(g/100g水)| t/℃ |  |  |  |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 122 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
 、
、 、
、 分别在100g乙醇中最多溶解的质量
分别在100g乙醇中最多溶解的质量 |  |  | |
| 最多溶解的质量(g) | 17.3 | <0.01 | 0.1 |
Ⅰ.
 在水中的溶解度随温度升高而
在水中的溶解度随温度升高而Ⅱ.20℃时,饱和食盐水中溶质质量分数为
Ⅲ.常温下,将
 通入饱和
通入饱和 的乙醇溶液中,反应的方程式为
的乙醇溶液中,反应的方程式为
您最近一年使用:0次

 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑