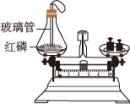
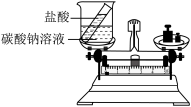
根据以下“探究参加化学反应前后各物质的质量总和是否相等”的实验,填空。
(1)完成实验报告中的内容。
【反思与评价】
(2)小松同学认为方案一与方案三天平均平衡,于是两个实验均可得出结论“参加化学反应前后各物质的质量总和相等”,但小雷同学不同意这一观点,小雷同学不同意的原因是___________ 。
【拓展和发现】小创同学在完成上面三个实验后,又完成了如下实验:
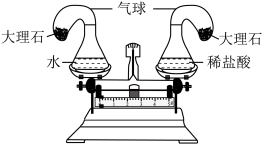
(3)他向两个锥形瓶中分别装入了等质量的水和稀盐酸,同时装入了等质量的大理石,实验开始时,将气球中的大理石分别倒入锥形瓶中,天平右侧观察到的现象是________ ,天平的指针_______ (填“偏左”、“偏右”或“在标尺中央”)。实验结束后,善于总结的小创同学发现,再利用天平右盘上药品进行质量守恒定律的验证实验时,除要注意方案二实验中的问题外,还要保证装置________ 。
(1)完成实验报告中的内容。
| 方案一 | 方案二 | 方案三 | |
| 装置 |
|
|
|
| 过程 | 分别将各组物质及反应容器放在托盘天平上用砝码平衡 | ||
| 如图所示装置,将橡胶塞上的玻璃管放到酒精灯火焰上灼烧至红热后,迅速用橡胶塞将锥形瓶塞紧,并将红磷引燃。待锥形瓶冷却后,重新放到托盘天平上天平仍然平衡。实验中玻璃管作用 | 取下烧杯并将其倾斜,使小试管中的盐酸进入烧杯中,充分反应后再放回托盘天平,天平的指针偏右。产生此现象的原因 | 取下烧杯并将其倾斜,使小试管中的水进入烧杯中,再放回托盘天平,天平的指针指向分度盘中央。 | |
【反思与评价】
(2)小松同学认为方案一与方案三天平均平衡,于是两个实验均可得出结论“参加化学反应前后各物质的质量总和相等”,但小雷同学不同意这一观点,小雷同学不同意的原因是
【拓展和发现】小创同学在完成上面三个实验后,又完成了如下实验:
(3)他向两个锥形瓶中分别装入了等质量的水和稀盐酸,同时装入了等质量的大理石,实验开始时,将气球中的大理石分别倒入锥形瓶中,天平右侧观察到的现象是
更新时间:2024-04-15 09:11:01
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某校化学兴趣小组的同学依据教材实验对化学反应前后物质的质量变化进行了探究。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【实验装置设计】甲、乙、丙三个小组的同学分别设计了如下图的装置:

【讨论与探究】
(1)甲小组实验中,白磷燃烧时,在锥形瓶底部铺少量_______ ,其目的是防止瓶底炸裂。
(2)请根据乙组和丙组设计的实验装置进行探究,并按要求完成填空。
①乙组实验结束后可观察到天平_______ (填“是”或“否”)平衡;此反应_______ (填“遵守”或“不遵守”)质量守恒定律。
②丙组进行过氧化氢溶液分解反应前后各物质质量总和的测定。该反应中二氧化锰起_______ 作用。
【实验结论】
(3)通过以上实验探究,你得到的结论是:参加化学反应的各物质的质量总和_______ (填“大于”、“等于”或“小于”)反应后生成的各物质的质量总和。
【实验分析】
(4)化学反应的过程是原子重新组合的过程,即反应前后原子的_______ 没有改变,原子的_______ 没有增减,原子的_______ 也没有变化,所以化学反应遵守质量守恒定律。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【实验装置设计】甲、乙、丙三个小组的同学分别设计了如下图的装置:

【讨论与探究】
(1)甲小组实验中,白磷燃烧时,在锥形瓶底部铺少量
(2)请根据乙组和丙组设计的实验装置进行探究,并按要求完成填空。
①乙组实验结束后可观察到天平
②丙组进行过氧化氢溶液分解反应前后各物质质量总和的测定。该反应中二氧化锰起
【实验结论】
(3)通过以上实验探究,你得到的结论是:参加化学反应的各物质的质量总和
【实验分析】
(4)化学反应的过程是原子重新组合的过程,即反应前后原子的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】84消毒液是生活中常用的一种消毒液,主要成分为次氯酸钠(NaClO)。实验小组对其进行研究。
【查阅资料】
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
【进行实验】
实验1:制备84消毒液
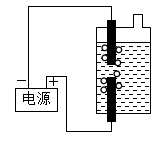
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。
实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
实验3:探究84消毒液漂白性的影响因素
【解释与结论】
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O 2NaOH+ Cl2↑+
2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
(2)实验2的目的是_______ 。
(3)实验3-1的结论是_______ 。
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有_________ 。
【反思与评价】
(5)由实验3可知,84消毒液储存时需注意________ 。
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是________ 。
【查阅资料】
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
【进行实验】
实验1:制备84消毒液
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。

实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
| 序号 | 2-1 | 2-2 | 2-3 | 2-4 |
| 实验 操作 | 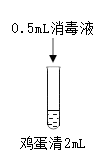 | 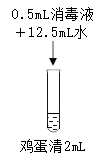 | 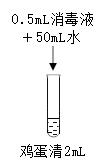 | 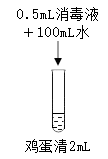 |
| 实验现象 | 液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
实验3:探究84消毒液漂白性的影响因素
| 序号 | 3-1 | 3-2 |
| 实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源 10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20°C、30°C、40°C、50°C水浴中加热,测量 ORP变化 |
| 测量数据 | 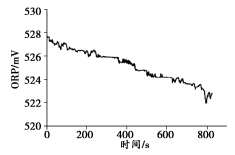 | 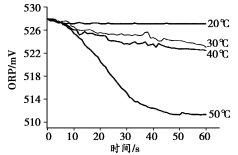 |
【解释与结论】
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O
 2NaOH+ Cl2↑+
2NaOH+ Cl2↑+(2)实验2的目的是
(3)实验3-1的结论是
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有
【反思与评价】
(5)由实验3可知,84消毒液储存时需注意
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐3】“江北水乡﹒运河古城”是今日枣庄的城市名片,而她又素以“煤城”著称。煤是一种重要的能源,工业上常把煤进行气化和液化处理,变为清洁能源。煤的气化和液化流程如下图所示:
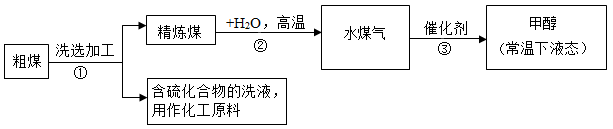
【查阅资料】水煤气是混合气体,由两种无色无味的气体组成,可以燃烧。
【提出问题】水煤气是什么?
【猜想假设】根据资料和反应物判断,水煤气可能是:①一氧化碳和氢气;②二氧化碳和氢气。
(1)提出以上猜想的依据是_____ 。
【设计实验】请从下列装置中选择一种,设计简单的实验证明猜想。
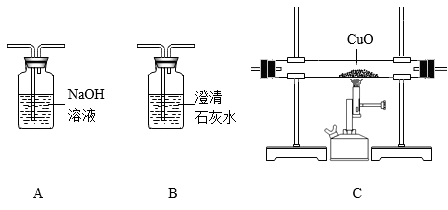
(2)你选择的装置是______ (填字母代号),可能的现象为_______ 。
【实验结论】(3)那么,猜想_____ (填序号)是合理的。

【查阅资料】水煤气是混合气体,由两种无色无味的气体组成,可以燃烧。
【提出问题】水煤气是什么?
【猜想假设】根据资料和反应物判断,水煤气可能是:①一氧化碳和氢气;②二氧化碳和氢气。
(1)提出以上猜想的依据是
【设计实验】请从下列装置中选择一种,设计简单的实验证明猜想。

(2)你选择的装置是
【实验结论】(3)那么,猜想
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】根据以下实验方案,“探究参加化学反应前后各物质的质量总和是否相等”,请将你的思考及实验结果写在短线处。(已知:Fe+CuSO4→FeSO4+Cu;Na2CO3+HCl→NaCl+H2O+CO2)
【猜想假设】:猜想1:相等;猜想2:___________ 。
【实验探究】:
【反思评价】你认为猜想___________ 是错误的,其原因是___________ 。
【猜想假设】:猜想1:相等;猜想2:
【实验探究】:
| 实验方案 | 方案一 | 方案二 |
| 实验装置 |  |  |
| 实验过程 | 分别将反应物及反应容器放在托盘天平上用砝码平衡 | |
| 取下烧杯,将铁钉浸到硫酸铜溶液中,观察到的现象是铁钉表面有红色物质析出、溶液由蓝色逐渐变为浅绿色;再将其放回托盘天平,天平的指针 | 取下烧杯并将其倾斜,使小试管中的盐酸进入烧杯中,充分反应后再放回托盘天平,天平的指针 | |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】大明同学在做探究质量守恒定律实验时,称取2.4g镁条在盛有足量空气的密闭容器中点燃,实验完毕后,大明称得所得固体的质量小于4.0g
【提出问题】
(1)镁条与氧气燃烧的化学方程式为___________ 。据此大明存在疑问:固体质量为什么会小于4.0g呢?
【查阅资料】①镁在空气中燃烧时,除了与氧气反应外,还可以与二氧化碳、氮气等发生反应:


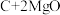
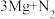


②氮化镁(Mg3N2)是淡黄色的固体。
【作出假设】假设1:镁条和空气中的CO2发生了反应导致固体质量小于4.0g:
假设2:镁条和空气中的N2发生了反应导致固体质量小于4.0g。
(2)【实验探究】
【实验结论】
(3)2.4g镁条在空气中完全反应后所得固体质量小于4.0g,是因为镁条与空气中的_______ (填化学式)反应造成的。
【实验拓展】
(4)除去空气中的氧气,得到较纯净的氨气(含少量稀有气体),应选择的物质是_______ (A 木炭 B 镁粉 C红磷,填序号),写出一条你选择该物质的理由___________ 。
【提出问题】
(1)镁条与氧气燃烧的化学方程式为
【查阅资料】①镁在空气中燃烧时,除了与氧气反应外,还可以与二氧化碳、氮气等发生反应:


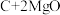
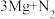


②氮化镁(Mg3N2)是淡黄色的固体。
【作出假设】假设1:镁条和空气中的CO2发生了反应导致固体质量小于4.0g:
假设2:镁条和空气中的N2发生了反应导致固体质量小于4.0g。
(2)【实验探究】
| 实验操作 | 实验数据 | 实验结论 |
| (1)取2.4g镁条在盛有足量CO2的密闭容器中点燃,用托盘天平称量实验后所得固体的质量 | 称得固体质量为4.6g | 假设1: |
| (2)取2.4g镁条在盛有足量N2的密闭容器中点燃,用托盘天平称量实验后所得固体的质量 | 称得固体质量为3.3g | 假设2: |
【实验结论】
(3)2.4g镁条在空气中完全反应后所得固体质量小于4.0g,是因为镁条与空气中的
【实验拓展】
(4)除去空气中的氧气,得到较纯净的氨气(含少量稀有气体),应选择的物质是
您最近一年使用:0次
【推荐3】甲、乙、丙三个兴趣小组同学依据教材实验对化学反应前后物质质量变化进行了如图所示的探究。
查阅资料:碳酸钠与稀盐酸反应生成二氧化碳气体。



(1)甲组实验中,反应前用天平称出装置的总质量,用滴管向盛有硫酸铜溶液的锥形瓶中加入氢氧化钠溶液,会发现有蓝色沉淀生成,反应后会观察到天平_________ 平衡(选填“仍保持”或“失去”)。
(2)乙组实验中,用过氧化氢溶液和二氧化锰进行了实验,反应前用天平称出装置的总质量,用滴管向锥形瓶中加入过氧化氢溶液,反应后会观察到天平_________ 平衡(选填“仍保持”或“失去”),该反应中二氧化锰起_________ 作用。
(3)通过甲、乙小组实验的探究,你得到的结论是参加化学反应的各物质的质量总和_________ (选填“大于”“等于”或“小于”)反应后生成的各物质的质量总和。
(4)丙组实验中,反应前用天平称出装置的总质量,然后将盐酸倒入烧杯中,反应后天平_________ 平衡(选填“仍保持”或“失去”),其原因是__________________ 。
(5)从微观角度对实验进行分析可知,化学反应的过程是_________ 重新组合的过程,在化学反应前后一定不变的是_________ (选填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
(6)对丙组实验进行反思,对该实验装置改进的方法是__________________ 。
查阅资料:碳酸钠与稀盐酸反应生成二氧化碳气体。



(1)甲组实验中,反应前用天平称出装置的总质量,用滴管向盛有硫酸铜溶液的锥形瓶中加入氢氧化钠溶液,会发现有蓝色沉淀生成,反应后会观察到天平
(2)乙组实验中,用过氧化氢溶液和二氧化锰进行了实验,反应前用天平称出装置的总质量,用滴管向锥形瓶中加入过氧化氢溶液,反应后会观察到天平
(3)通过甲、乙小组实验的探究,你得到的结论是参加化学反应的各物质的质量总和
(4)丙组实验中,反应前用天平称出装置的总质量,然后将盐酸倒入烧杯中,反应后天平
(5)从微观角度对实验进行分析可知,化学反应的过程是
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
(6)对丙组实验进行反思,对该实验装置改进的方法是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某实验小组进行影响化学反应速率因素的探究及二氧化碳性质的探究。
I、影响化学反应速率因素的探究:每次都加入相同质量的大理石(足量)和25mL的稀盐酸,并记录收集到100mL二氧化碳气体所需要的时间。下表是实验的记录:
(1)实验②和④研究了某因素时实验速率的影响,则W=______ ,分析数据可知______ 因素对反应速率的影响最大。
(2)从实验①②得出的探究结论是:______ 。
(3)为完成上述探究实验,从下图A-D装置中选出最适宜的发生装置______ (填字母),写出该反应方程式______ 。
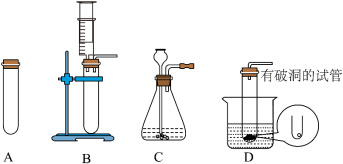
Ⅱ、CO2性质探究:
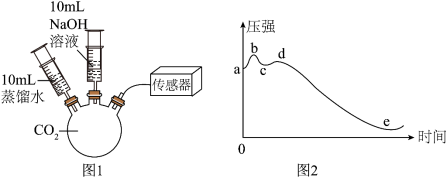
用如图1装置实验,测得三颈烧瓶内气压变化情况如图2所示。
(4)首先注入瓶中的药品是______ (填“水”或“氢氧化钠溶液”),“bc”变化的原因是______ 。
(5)对比曲线中“bc”段和“de”段,可证明______ 。
I、影响化学反应速率因素的探究:每次都加入相同质量的大理石(足量)和25mL的稀盐酸,并记录收集到100mL二氧化碳气体所需要的时间。下表是实验的记录:
| 编号 | 颗粒大小 | 实验温度 | 稀盐酸的质量 分数 | 加入稀盐酸 体积 | 时间 |
| ① | 粗颗粒 | 20℃ | 7.3% | 25 | 133 |
| ② | 粗颗粒 | 20℃ | W | 25 | 126 |
| ③ | 粗颗粒 | 35℃ | 7.3% | 25 | 61 |
| ④ | 细颗粒 | 20℃ | 14.6% | 25 | 79 |
(2)从实验①②得出的探究结论是:
(3)为完成上述探究实验,从下图A-D装置中选出最适宜的发生装置

Ⅱ、CO2性质探究:

用如图1装置实验,测得三颈烧瓶内气压变化情况如图2所示。
(4)首先注入瓶中的药品是
(5)对比曲线中“bc”段和“de”段,可证明
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】数字化实验设备含:传感器——数据采集器——计算机——应用软件,它可将实验过程中某些因素(酸碱性、浓度、气压等)的变化以数据、图像的形式呈现出来。
【查阅资料】在0℃,标准大气压下,1体积水可以溶解1体积的二氧化碳。
(一)探究二氧化碳与水反应
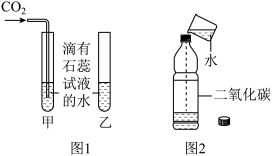
(1)图1中可观察到甲试管里的颜色变化______ ,该反应的化学方程式______ 。
(2)某兴趣小组的同学采取图2置探究CO2能与水反应。
①甲同学按如图2示的实验,打开瓶塞,迅速将烧杯中的水倒入瓶中并拧紧瓶塞,振荡,一会后发现软塑料瓶变瘪。得出结论:CO2能与水反应。请你解释塑料瓶变瘪的原因是______ 。
②乙同学认为甲同学的实验,还不足以证明CO2能与水反应。乙同学的理由______ 。
(二)比较块状碳酸钙、粉末状碳酸钙与稀盐酸反应的速度
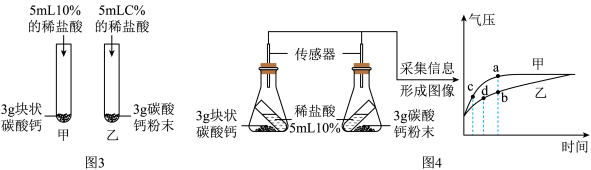
(3)图3中,乙试管里稀盐酸的溶质质量分数C%应为______ 。较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是______ 。
(4)按图4所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示。对比分析坐标图中的点______ (选填“a”、“b”、“c”、“d”) 可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短。
【查阅资料】在0℃,标准大气压下,1体积水可以溶解1体积的二氧化碳。
(一)探究二氧化碳与水反应

(1)图1中可观察到甲试管里的颜色变化
(2)某兴趣小组的同学采取图2置探究CO2能与水反应。
①甲同学按如图2示的实验,打开瓶塞,迅速将烧杯中的水倒入瓶中并拧紧瓶塞,振荡,一会后发现软塑料瓶变瘪。得出结论:CO2能与水反应。请你解释塑料瓶变瘪的原因是
②乙同学认为甲同学的实验,还不足以证明CO2能与水反应。乙同学的理由
(二)比较块状碳酸钙、粉末状碳酸钙与稀盐酸反应的速度

(3)图3中,乙试管里稀盐酸的溶质质量分数C%应为
(4)按图4所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示。对比分析坐标图中的点
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】某化学兴趣小组在刷洗试管时,用力过猛,造成试管底被穿通,留下圆形小孔。在老师的启发下,兴趣小组变废为宝,将细铜丝揉成小球垫在试管底部,配上带单孔橡皮塞的导管和烧杯,装配了一个在实验室制取气体的装置。

(1)若用此装置制取二氧化碳,在试管内的铜丝球上方应盛放块状_________ (填药品名称),发生反应的化学方程式为____________ 。
(2)在试管内的铜丝球上方盛放一定量金属锌。实验结束后,该兴趣小组同学想对烧杯中剩余溶液的成分进行探究。
【提出问题】烧杯中溶液的溶质是什么?
【提出猜想】根据该反应是否恰好完全进行,可能有以下两种猜想:
①小君同学猜想:溶质是ZnCl2和HCl; ②你的猜想:溶质是_________ 。
【实验验证】

(1)若用此装置制取二氧化碳,在试管内的铜丝球上方应盛放块状
(2)在试管内的铜丝球上方盛放一定量金属锌。实验结束后,该兴趣小组同学想对烧杯中剩余溶液的成分进行探究。
【提出问题】烧杯中溶液的溶质是什么?
【提出猜想】根据该反应是否恰好完全进行,可能有以下两种猜想:
①小君同学猜想:溶质是ZnCl2和HCl; ②你的猜想:溶质是
【实验验证】
| 步骤 | 现象 | 结论 |
| 取少许反应后的溶液于试管中,加入 | 小君的猜想正确 |
您最近一年使用:0次