分析处理图表中的信息是学习化学的种重要方法。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
①30℃时,KNO3溶液的最大浓度(溶质质量分数)为 ________ (只列计算式,不需要计算结果).
②根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是_____ 。
(2)根据电解水的实验,回答下列问题:
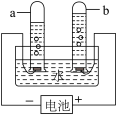
①从宏观上观察:图示a、b管中产生的体积比约为2:1,则他们的质量比为____ 。
②从微观上分析:下列说法错误的是_________ (填字母)。
a.水是由水分子构成的
b.水是由氢原子和氧原子构成的
c.每个水分子是由2个氢原子和1个氧原子构成的
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答。

①蒸发前原溶液是_______ (填“饱和”或“不饱和”)溶液,n的数值是 ______ 。
②依据上述实验,你认为甲的溶解度随温度变化的趋势是________ (填序号)。
a.随温度升高而增大 b.随温度升高面减小 c.无法判断。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
②根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是
(2)根据电解水的实验,回答下列问题:

①从宏观上观察:图示a、b管中产生的体积比约为2:1,则他们的质量比为
②从微观上分析:下列说法错误的是
a.水是由水分子构成的
b.水是由氢原子和氧原子构成的
c.每个水分子是由2个氢原子和1个氧原子构成的
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答。

①蒸发前原溶液是
②依据上述实验,你认为甲的溶解度随温度变化的趋势是
a.随温度升高而增大 b.随温度升高面减小 c.无法判断。
更新时间:2019/03/17 15:03:26
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】请按要求填空:
(1)如图是电解水的简易装置图。
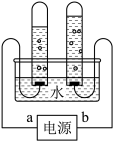
①电源的正极_______ (用a,b表示),正极与负极产生的气体体积比为_______ 。
②常向水中加入少量氢氧化钠或硫酸,目的是_______ 。
(2)师大附中的几位同学收集了一瓶浑浊的捞鱼河河水,他们要模拟自来水厂的净水过程,最终制成蒸馏水,其实验流程如下图所示:

①操作①用到的玻璃仪器除烧杯、漏斗外还要用到_______ 。
②操作②常加入活性炭,利用其具有_______ 作用。
③他们取少量的液体D于试管中,向其中加入肥皂水,泡沫较少,浮渣较多说明是_______ ;实验室里使硬水软化的方法是_______ 。
(3)金属钛广泛应用于航空航天工业。目前常用金红石(主要含TiO2)或TiO2为原料来制取金属钛,主要工艺流程如下:
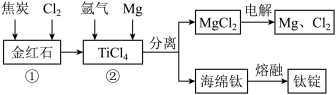
试回答下列问题:
a.在上述工艺流程中可以循环使用的物质是_______ ;
b.流程①中焦炭(符号为C)、Cl2和TiO2在一定条件下反应,生成TiCl4和物质A,物质A是绿色植物光合作用的一种原料,则流程①的化学反应方程式为_______ ;物质A属于_______ (填“化合物”或“单质”)。
(1)如图是电解水的简易装置图。

①电源的正极
②常向水中加入少量氢氧化钠或硫酸,目的是
(2)师大附中的几位同学收集了一瓶浑浊的捞鱼河河水,他们要模拟自来水厂的净水过程,最终制成蒸馏水,其实验流程如下图所示:

①操作①用到的玻璃仪器除烧杯、漏斗外还要用到
②操作②常加入活性炭,利用其具有
③他们取少量的液体D于试管中,向其中加入肥皂水,泡沫较少,浮渣较多说明是
(3)金属钛广泛应用于航空航天工业。目前常用金红石(主要含TiO2)或TiO2为原料来制取金属钛,主要工艺流程如下:

试回答下列问题:
a.在上述工艺流程中可以循环使用的物质是
b.流程①中焦炭(符号为C)、Cl2和TiO2在一定条件下反应,生成TiCl4和物质A,物质A是绿色植物光合作用的一种原料,则流程①的化学反应方程式为
您最近一年使用:0次
【推荐2】请利用学过的化学知识填空。
(1)规范的实验操作是实验成功的前提,试回答下列问题。
①从试剂瓶向试管中倾倒稀盐酸时,标签要__________________ 。
②连接玻璃导管和胶皮管时,要先将导管__________________ ,再将胶皮管挤套在玻璃导管上。
③使用胶头滴管后未经清洗就吸取别的试剂,后果是__________________ 。
④如果少量酒精洒在桌面上燃烧起来,应该立即用__________________ 扑灭。
(2)水是生命之源,研究“水”可从多角度展开,下图为某国际空间站的水气整合系统。
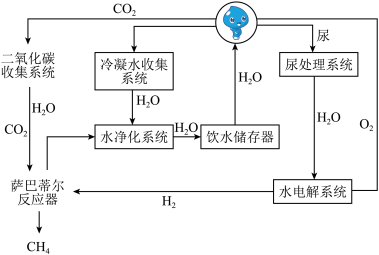
①水的电解:水电解系统发生反应,满足航天员供氧需求,反应的文字表达式或符号表达式为_________ ;若正极产生8mL气体,则负极产生气体的体积为_________ mL;该实验表明,水由_____ 组成。
②水的净化:水净化系统用到活性炭,利用活性炭的_________ 性;若要鉴别净化后的水是硬水还是软水,可加入_________ ;生活中可以采用_________ 的方法将硬水软化。
③水的用途:铁丝在氧气中燃烧,预先在集气瓶底部放少量水,水的作用是__________________ 。
④水的性质:水在常温下能和二氧化碳反应,文字表达式或符号表达式为__________________ ;水还能和二氧化碳通过光合作用生成葡萄糖和氧气。两个反应的反应物相同,但生成物不同,是因为__________________ 不同。
⑤水资源的保护:保护水资源是全人类的责任,请写出一条节水措施__________________ 。
(1)规范的实验操作是实验成功的前提,试回答下列问题。
①从试剂瓶向试管中倾倒稀盐酸时,标签要
②连接玻璃导管和胶皮管时,要先将导管
③使用胶头滴管后未经清洗就吸取别的试剂,后果是
④如果少量酒精洒在桌面上燃烧起来,应该立即用
(2)水是生命之源,研究“水”可从多角度展开,下图为某国际空间站的水气整合系统。

①水的电解:水电解系统发生反应,满足航天员供氧需求,反应的文字表达式或符号表达式为
②水的净化:水净化系统用到活性炭,利用活性炭的
③水的用途:铁丝在氧气中燃烧,预先在集气瓶底部放少量水,水的作用是
④水的性质:水在常温下能和二氧化碳反应,文字表达式或符号表达式为
⑤水资源的保护:保护水资源是全人类的责任,请写出一条节水措施
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】“水善利万物而不争”,水是人类的宝贵资源。
一、认识水的净化
(1)空气制水机可利用大气中的水分制出饮用水。结合图1示回答。_______ (填字母)。
②压缩冷凝时空气中水蒸气变为液态水,该过程中不发生变化的是_______ (填字母)。
A.分子的质量 B.分子的种类 C.分子的间隔
(2)离子交换法净水过程如图2所示。_______ (填“阳离子”或“阴离子”)交换树脂。
②将水样通过离子交换柱后,水中阴、阳离子所带电荷总数相等,交换后的水仍然呈电中性。水中阳离子总数_______ (填“增加”、“减少”或“不变”)。
二、探究水的组成
【实验步骤】i.连接好装置(如图3),检查装置气密性
iii.取下注射器,打开电源一段时间后关闭电源
iv.将注射器活塞推到顶后连接注射器,再次打开电源。当注射器II中活塞停留在10mL刻度时,关闭电源
v.检验气体
(3)实验开始时,先打开电源通电一段时间后再接上注射器的目的是_______ 。
(4)实验结束时注射器I中活塞停留在_______ 刻度处,将该注射器带上针头,移向燃着的木条旁,推动活塞,现象是_______ 。
三、研究影响电解水反应速率的因素
为研究影响电解水反应速率的因素,某兴趣小组利用12V直流电源进行了相关实验探究,数据如表:(水的导电能力很弱,加入少量NaOH可增强水的导电性)
(5)实验1和2研究的影响电解水反应速率的因素是_______ 。
(6)分析四组实验数据,实验3的电解时间“x”可能是_______(填字母序号)。
(7)查阅资料发现,当其他条件不变时,增大直流电的电压也能加快电解水的速率。在上述实验基础上证明电压对电解水速率的影响,下列方案可行的是:_______ (填字母序号)。
四、污水处理
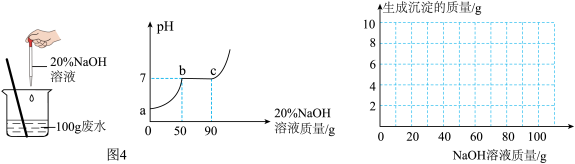
(8)某冶铜厂排放的废水中含有H2SO4和CuSO4两种污染物,为测定该废水中各污染物的含量,实验小组进行了以下实验:取100g废水,不断加入20%氢氧化钠溶液,通过数字传感器得到相关数据(图4)。请在坐标图画出加入氢氧化钠溶液的质量与产生沉淀质量的关系图。
一、认识水的净化
(1)空气制水机可利用大气中的水分制出饮用水。结合图1示回答。
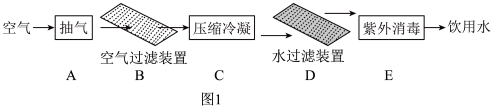
②压缩冷凝时空气中水蒸气变为液态水,该过程中不发生变化的是
A.分子的质量 B.分子的种类 C.分子的间隔
(2)离子交换法净水过程如图2所示。
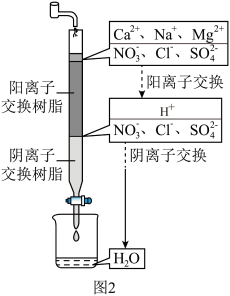
②将水样通过离子交换柱后,水中阴、阳离子所带电荷总数相等,交换后的水仍然呈电中性。水中阳离子总数
二、探究水的组成
【实验步骤】i.连接好装置(如图3),检查装置气密性
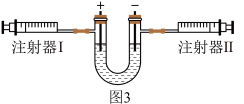
iii.取下注射器,打开电源一段时间后关闭电源
iv.将注射器活塞推到顶后连接注射器,再次打开电源。当注射器II中活塞停留在10mL刻度时,关闭电源
v.检验气体
(3)实验开始时,先打开电源通电一段时间后再接上注射器的目的是
(4)实验结束时注射器I中活塞停留在
三、研究影响电解水反应速率的因素
为研究影响电解水反应速率的因素,某兴趣小组利用12V直流电源进行了相关实验探究,数据如表:(水的导电能力很弱,加入少量NaOH可增强水的导电性)
| 编号 | 温度 | NaOH溶液浓度 | 负极气体体积 | 正极气体体积 | 电解时间 |
| 1 | 20℃ | 2% | 20mL | 9.8mL | 54.0s |
| 2 | 20℃ | 5% | 20mL | 9.8mL | 36.2s |
| 3 | 30℃ | 2% | 20mL | 9.9mL | x |
| 4 | 30℃ | 5% | 20mL | 9.9mL | 35.4s |
(5)实验1和2研究的影响电解水反应速率的因素是
(6)分析四组实验数据,实验3的电解时间“x”可能是_______(填字母序号)。
| A.32.4 | B.35.2 | C.50.2 | D.55.6 |
(7)查阅资料发现,当其他条件不变时,增大直流电的电压也能加快电解水的速率。在上述实验基础上证明电压对电解水速率的影响,下列方案可行的是:
| 序号 | 温度 | NaOH溶液浓度 | 电压 | 负极气体体积 | 正极气体体积 |
| A | 10℃ | 5% | 12V | 20mL | 9.8mL |
| B | 20℃ | 6% | 14V | 20mL | 9.8mL |
| C | 30℃ | 2% | 14V | 20mL | 9.9mL |
四、污水处理
(8)某冶铜厂排放的废水中含有H2SO4和CuSO4两种污染物,为测定该废水中各污染物的含量,实验小组进行了以下实验:取100g废水,不断加入20%氢氧化钠溶液,通过数字传感器得到相关数据(图4)。请在坐标图画出加入氢氧化钠溶液的质量与产生沉淀质量的关系图。
您最近一年使用:0次
【推荐1】海洋是个巨大的资源宝库。海水淡化、海水晒盐等对海洋资源的充分利用,体现了人类认识物质、改造物质的智慧。
(1)采用如图所示的膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池,从而得到淡水。下列说法中,不合理的是 (填选项序号之一)。

(2)采用盐田法晒盐,经日晒、风吹等,结晶池中会有氯化钠晶体析出,此时结晶池中的溶液为氯化钠的________ (填“饱和”或“不饱和”之一)溶液。该过程主要通过________ (选填“降温结晶”或“蒸发结晶”之一)使食盐析出。
(3)下图是粗盐在工业生产中的一种应用流程,请根据信息回答问题:
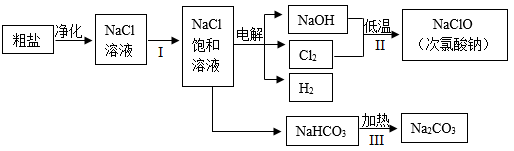
①除去粗盐中的难溶性杂质,可采用的操作是_________ (填选项序号A.蒸发 B.蒸馏 C.过滤D.溶解),该操作中玻璃棒的作用是______
②步骤 Ⅱ 中用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是_____ ,NaClO中氯元素的化合价为_________ 。
③氯化钠溶液在通电情况下生成NaOH、Cl2和H2,写出其反应的化学方程式:_____________ 。
(4)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,NaCl和KNO3的溶解度曲线如图所示,试回答下列问题:
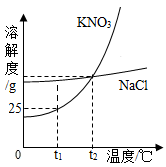
①在t2℃时,KNO3的溶解度_____ NaCl的溶解度(选填“大于”、“等于”或“小于”之一)。
②在t1℃时,KNO3饱和溶液的溶质质量分数是______ ,该温度下,将15g硝酸钾放入50g水中,可以得到 _______ g KNO3溶液。
③t1℃时分别将KNO3的饱和溶液及NaCl的饱和溶液升温到t2℃,此时KNO3溶质质量分数_________ (选填“大于”“小于”或“等于”之一)NaCl溶质质量分数。
(1)采用如图所示的膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池,从而得到淡水。下列说法中,不合理的是 (填选项序号之一)。

| A.膜分离法也是一种分离混合物的方法 |
| B.膜分离法较传统蒸馏法更节约能源 |
| C.加压后右侧海水中溶质质量分数增大 |
| D.加压后右侧海水的溶质质量增多 |
(3)下图是粗盐在工业生产中的一种应用流程,请根据信息回答问题:

①除去粗盐中的难溶性杂质,可采用的操作是
②步骤 Ⅱ 中用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是
③氯化钠溶液在通电情况下生成NaOH、Cl2和H2,写出其反应的化学方程式:
(4)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,NaCl和KNO3的溶解度曲线如图所示,试回答下列问题:

①在t2℃时,KNO3的溶解度
②在t1℃时,KNO3饱和溶液的溶质质量分数是
③t1℃时分别将KNO3的饱和溶液及NaCl的饱和溶液升温到t2℃,此时KNO3溶质质量分数
您最近一年使用:0次
【推荐2】如图为硝酸钾和氯化钠两种物质的溶解度曲线。
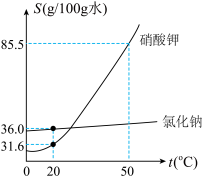
(1)20℃时,两种物质溶解度的大小关系:S(氯化钠)_______ S(硝酸钾)(选填“>”、“=”或“<”)。
(2)50℃时,将90g硝酸钾固体投入100g水中,充分溶解后可得到的硝酸钾溶液的质量是_______ 。
(3)氯化钠是一种非常重要的工业原料,人们通常通过海水晒盐的方法来得到粗盐。以下是同学用100g15%氯化钠溶液在20℃时恒温蒸发模拟晒盐过程,请回答下列问题。
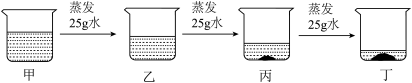
I.甲、乙、丙、丁中,一定是氯化钠饱和溶液的是_________ 。
II.关于甲、乙、丙、丁中,下列说法正确的是________ 。
A、甲和乙中的溶剂质量相等
B、整个过程中氯化钠的溶解度不断增大
C、丙和丁中溶液的溶质质量分数相同
D、丁中最终析出氯化钠11.4g
(4)工业上通常通过电解饱和食盐水来生产氢氧化钠,但是这样生产的氢氧化钠通常会含有氯化钠杂质,为了检验某氢氧化钠样品中是否含有氯化钠,某研究小组小李同学设计并进行了如下实验。
III.实验反思:小组成员小张同学提出:方案步骤一中使用足量的氯化镁溶液会导致无法检验氯化钠,应对步骤一进行改进。你是否同意?若同意,请写出改进方案。若不同意,请写出理由:______ 。

(1)20℃时,两种物质溶解度的大小关系:S(氯化钠)
(2)50℃时,将90g硝酸钾固体投入100g水中,充分溶解后可得到的硝酸钾溶液的质量是
(3)氯化钠是一种非常重要的工业原料,人们通常通过海水晒盐的方法来得到粗盐。以下是同学用100g15%氯化钠溶液在20℃时恒温蒸发模拟晒盐过程,请回答下列问题。

I.甲、乙、丙、丁中,一定是氯化钠饱和溶液的是
II.关于甲、乙、丙、丁中,下列说法正确的是
A、甲和乙中的溶剂质量相等
B、整个过程中氯化钠的溶解度不断增大
C、丙和丁中溶液的溶质质量分数相同
D、丁中最终析出氯化钠11.4g
(4)工业上通常通过电解饱和食盐水来生产氢氧化钠,但是这样生产的氢氧化钠通常会含有氯化钠杂质,为了检验某氢氧化钠样品中是否含有氯化钠,某研究小组小李同学设计并进行了如下实验。
| 操作步骤 | 实验现象 | 反应化学方程式/实验结论 |
| I.取少量固体,溶解。滴加足量的氯化镁溶液。 | 产生白色沉淀 | 反应化学方程式: |
| II.过滤,向滤液中滴加硝酸银溶液。 | 说明有氢氧化钠样品中有氯化钠。 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】水和溶液在日常生活、科学研究中具有广泛的用途。
(1)生活中为了降低水的硬度并杀菌消毒,常用的方法是______ 。
(2)甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答。
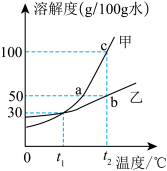
①t1℃时,在50g水中加入20g乙固体,充分搅拌后得到______ (填“饱和或不饱和”)溶液。
②t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须恒温蒸发掉较多水的是______ (填“甲”或“乙”)物质的饱和溶液。
③使甲物质的溶液状态发生如下改变,对应操作正确的是______ 。
A.a点→c点:加水 B.b点→c点:恒温蒸发
C.a点→b点:升温 D.c点→a点:降温、过滤
(3)生理盐水是医疗上常用的一种溶液,取出其中的任意一部分进行比较,发现它们的组成完全相同,说明溶液具有______ 性。
(4)实验室常用过氧化氢溶液制取氧气,若要制取6.4g氧气,则同时产生水的质量是多少?(写出计算过程)
(1)生活中为了降低水的硬度并杀菌消毒,常用的方法是
(2)甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答。

①t1℃时,在50g水中加入20g乙固体,充分搅拌后得到
②t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须恒温蒸发掉较多水的是
③使甲物质的溶液状态发生如下改变,对应操作正确的是
A.a点→c点:加水 B.b点→c点:恒温蒸发
C.a点→b点:升温 D.c点→a点:降温、过滤
(3)生理盐水是医疗上常用的一种溶液,取出其中的任意一部分进行比较,发现它们的组成完全相同,说明溶液具有
(4)实验室常用过氧化氢溶液制取氧气,若要制取6.4g氧气,则同时产生水的质量是多少?(写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】60℃时,将固体X加入不同质量的水中达到饱和状态时所溶解的质量绘制成如图斜线。

(1)60℃时,固体X的溶解度为______ 。
(2)固体X的溶解度随温度的升高而______ 。(填“增大”,“减小”,“不变”或“无法确定”)
(3)下列说法正确的是______ ;
①a点处固体X的溶液中溶质与溶液的质量比为1:4
②从b点溶液得到d点溶液,需增加固体X 2.0g
③从a点溶液得到b点溶液,可以增加溶质或者蒸发溶剂
④图中4个点表示的溶液中溶质的质量分数的大小关系是:d=c>a>b
(4)配制一定质量分数的X溶液的操作步骤如下,其中操作错误的是______ 。
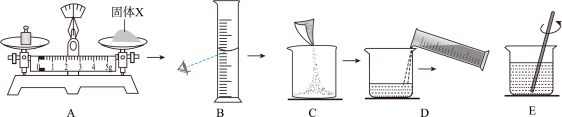

(1)60℃时,固体X的溶解度为
(2)固体X的溶解度随温度的升高而
(3)下列说法正确的是
①a点处固体X的溶液中溶质与溶液的质量比为1:4
②从b点溶液得到d点溶液,需增加固体X 2.0g
③从a点溶液得到b点溶液,可以增加溶质或者蒸发溶剂
④图中4个点表示的溶液中溶质的质量分数的大小关系是:d=c>a>b
(4)配制一定质量分数的X溶液的操作步骤如下,其中操作错误的是

您最近一年使用:0次
【推荐2】氯化铵( )是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。
)是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。
项目一:氯化铵的性质
(1)氯化铵是一种白色固体粉末,描述的是氯化铵的_____ (填“物理”或“化学”)性质。
(2)鉴别尿素[ ]和氯化铵
]和氯化铵_____ (填“能”或“不能”)用加熟石灰研磨的方法。
项目二:氯化铵的制备
(3)如图,两集气瓶中分别装满氨气 和氯化氢
和氯化氢 气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
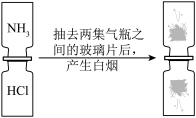
该实验可以说明分子在_____ 。
项目三:氯化铵的用途
(4)用氯化铵固体配制无土栽培营养液。 时,取
时,取 固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:
固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:

①甲、乙溶液的溶质质量分数大小关系为_____ 。丙溶液是_____ (填“饱和”或“不饱和”)溶液。
② 时
时 的溶解度为
的溶解度为_____ g。
 )是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。
)是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。项目一:氯化铵的性质
(1)氯化铵是一种白色固体粉末,描述的是氯化铵的
(2)鉴别尿素[
 ]和氯化铵
]和氯化铵项目二:氯化铵的制备
(3)如图,两集气瓶中分别装满氨气
 和氯化氢
和氯化氢 气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
该实验可以说明分子在
项目三:氯化铵的用途
(4)用氯化铵固体配制无土栽培营养液。
 时,取
时,取 固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:
固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:
①甲、乙溶液的溶质质量分数大小关系为
②
 时
时 的溶解度为
的溶解度为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】已知M、N两种固体物质的溶解度曲线如图所示。据图回答问题:
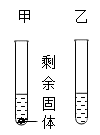
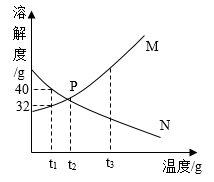
(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质____ (M、N),若将温度升高至t3℃,则乙试管中的现象是___ ,甲试管中溶液的溶质质量分数是___ (保留小数点后一位),若将此溶液浓缩成40%的溶液,则需蒸发掉__ 水。
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是____


(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是
您最近一年使用:0次



